SUBiecte de biochimie
Unghiuri diedrale (sau de torsiune)
Definiții ale unghiului de legătură și ale unghiului diedral (de torsiune). Unghiuri diedrale ale lanțului principal al polipeptidelor, φ, ψ și ω. Graficele Ramachandran.
Conformațiile pe care le adoptă moleculele biologice determină proprietățile fizice și chimice pe care le prezintă în sistemele biologice. Prin urmare, avem nevoie de o modalitate de a descrie conformațiile observate pentru tipurile de molecule studiate în biochimie. Accentul principal în această secțiune va fi pus pe conformațiile polipeptidelor, ca pregătire pentru înțelegerea relațiilor structură-funcție în proteine
Un unghi diedru – numit și unghi de torsiune – este definit de patru atomi legați secvențial. Acesta este reprezentat în figura de mai jos prin structura A-B-C-D (al doilea panou; rețineți distincția dintre unghiul de legătură și unghiul de torsiune). Imaginați-vă că priviți de-a lungul legăturii dintre atomii B și C (așa cum este indicat de săgeată). Aceasta este legătura centrală dintre cele trei legături definite. La început, vedem legătura B-C în planul figurii, cu legătura B-A îndreptată spre stânga și în sus, în afara planului, iar legătura C-D îndreptată în jos și spre dreapta. Apoi, luăm această structură și începem să o întoarcem astfel încât să putem privi direct în jos legătura B-C (al treilea panou). În cele din urmă, vederea noastră este echivalentă cu proiecția Newman din ultimul panou. Din această vedere, unghiul diedru τ este unghiul aparent subînțeles de D în raport cu A, așa cum se arată. Definim intervalul de valori al unghiurilor diedrale ca fiind , iar valoarea lui τ este de aproximativ -150° (Partea negativă a intervalului corespunde atunci când D este în sens invers acelor de ceasornic în raport cu A.)
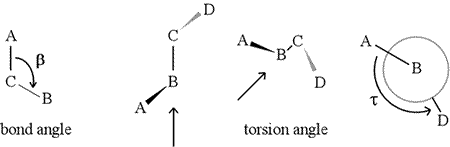
Desigur, alți atomi pot fi legați de B și C – și de obicei sunt. Ar trebui să specificăm ce atomi corespund lui A, B, C și D pentru a defini fără ambiguitate unghiul diedru. Pentru polimerii lungi și neramificați, cum ar fi proteinele, este logic să se ceară ca A până la D să fie toți atomii lanțului principal. Mai jos este o imagine de grafică moleculară care corespunde schiței de mai sus și care ilustrează definiția unghiului diedru Phi (φ) al lanțului principal al polipeptidelor.
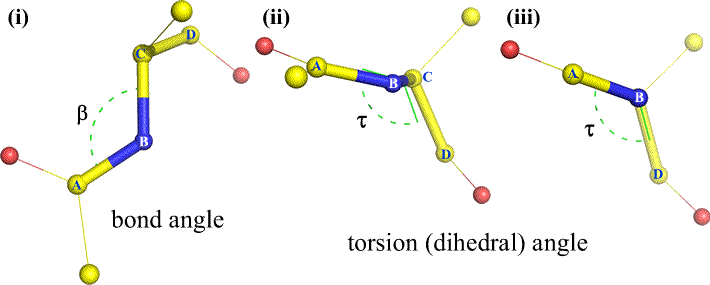
Unghiurile diedru ale lanțului principal al polipeptidelor: Phi (φ), Psi (ψ) și Omega (ω)
Un unghi diedru este definit de patru atomi. El poate fi vizualizat privind în jos legătura centrală (adică legătura de la atomul 2 la atomul 3). Unghiurile diedrice de-a lungul unui lanț polipeptidic sunt de trei tipuri:
Phi (φ) – legătura centrală dintre N(i) și C(alfa, i) . Priviți în jos legătura N(i)-Cα(i), observați unghiul subînțeles de carbonul acil C(i) în raport cu C(i-1) – carbonul acil din reziduul anterior.
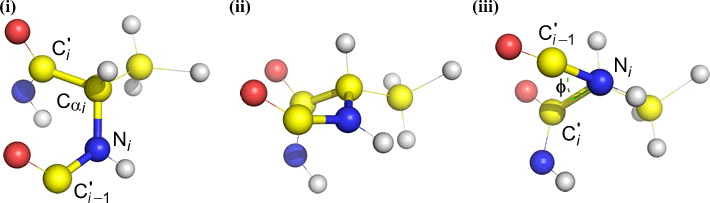
Psi (ψ) – legătura centrală între C(alfa, i) și C(i) . Priviți în jos legătura Cα(i)-C(i), observați unghiul subînțeles de N(i + 1) în raport cu N(i).
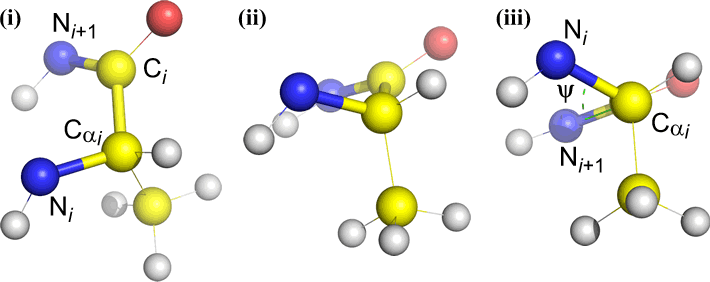
Omega (ω) – legătura peptidică dintre carbonul acil C(i) și N(i+1) este legătura centrală.
Phi (φ) și psi (ψ) sunt uneori denumite unghiuri Ramachandran, deoarece sunt utilizate într-un grafic bidimensional al unghiurilor diedrului lanțului principal numit grafic Ramachandran (vezi mai jos).
Pratgraficul Ramachandran
Graficul Ramachandran este un grafic al unghiurilor diedre ale lanțului principal phi (φ) și psi (ψ) pentru un lanț polipeptidic, cu valorile phi (φ) de-a lungul axei x și valorile psi (ψ) de-a lungul axei y.
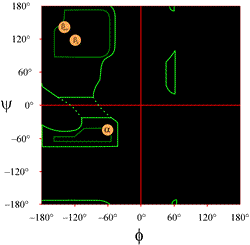
Schema unui grafic Ramachandran, așa cum este prezentat de obicei în manualele școlare, este prezentată în stânga (faceți clic pe figură pentru a afișa o versiune mai mare). Contururile indică întinderea combinațiilor permise (verde deschis) și a celor mai favorizate (verde închis) de (φ, ψ). Cercurile portocalii arată locațiile valorilor ideale phi, psi pentru cele mai comune caracteristici structurale secundare regulate, firele beta (în foițe antiparalele și paralele) și elicele alfa. În afara contururilor, conformațiile corespunzătoare sunt defavorizate sau nepermise. Locațiile exacte ale contururilor nu trebuie luate prea literal, deoarece regiunile favorabile și permise depind de identitatea reziduurilor. Glicina, în special, are regiuni permise mult mai mari decât cele prezentate aici. Acest aspect este discutat mai jos.
Un grafic Ramachandran „real”
În „jocul final” al determinării structurii proteice, modelul determinat experimental trebuie analizat pentru calitatea sa stereochimică. Probleme serioase cu modelul pot fi indicate dacă există cazuri de reziduuri non-Gly ale căror unghiuri diedrale ale lanțului principal se află în afara regiunilor permise sau dacă o proporție prea mare de reziduuri se află în afara regiunii celei mai favorizate. Un exemplu de grafic Ramachandran pentru o proteină de 190 de reziduuri este prezentat în figura alăturată.
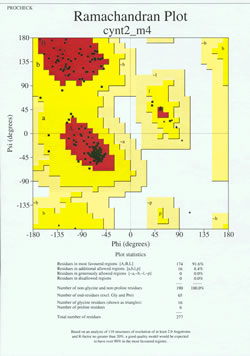
Figura prezintă un grafic Ramachandran pentru o structură proteică determinată prin cristalografie cu raze X. (Faceți clic pe ea pentru a vizualiza o versiune mai mare într-o fereastră nouă.) Fiecare pătrat negru reprezintă conformația lanțului principal la un reziduu al proteinei. Observați cum valorile phi, psi pentru reziduuri se grupează în regiunile roșii „cele mai favorizate”. Regiunea roșie din stânga sus (etichetată „B” în figură) corespunde reziduurilor dintr-o conformație beta a lanțului principal, în timp ce zona mare din apropierea mijlocului (etichetată „A”) corespunde helixului alfa. Cea de-a treia zonă mică, de culoare roșie, din grafic, este cea în care se află reziduurile care adoptă o helix alfa stângaci („L”). Unele dintre aceste reziduuri se află în „regiuni permise suplimentare” (galben strălucitor) care mărginesc regiunile cele mai favorizate. Observați cum reziduurile de glicină (indicate ca triunghiuri) se află în unele cazuri în „regiuni nepermise”. Acest lucru se datorează faptului că Gly, având ca „lanț lateral” doar un mic atom de hidrogen, este mult mai puțin îngreunat din punct de vedere steric decât alți aminoacizi. Gly este capabil să adopte perechi de unghiuri phi, psi care nu sunt permise pentru niciun alt reziduu.
.