Även vid extremt låga koncentrationer skadas vattenlevande organismer av ammoniak. Ammoniak förekommer naturligt i miljön. En liten mängd ammoniak bildas när blixten slår ner och når jorden i nederbörd. Men den mesta ammoniaken produceras av bakterier i vatten och jord som en slutprodukt av nedbrytning av växt- och djuravfall. Den finns i relativt låga, icke-toxiska koncentrationer i mark, luft och vatten och utgör en kvävekälla för växter.
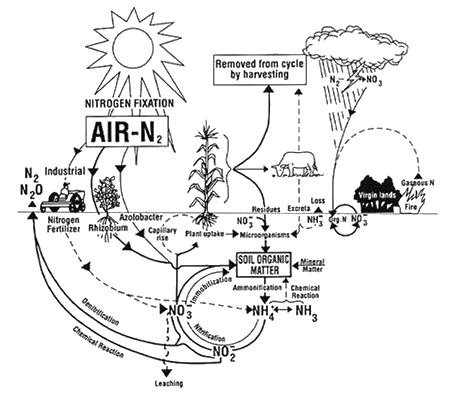
Även vid extremt låga koncentrationer skadas vattenlevande organismer av ammoniak. Ammoniak förekommer naturligt i miljön. En liten mängd ammoniak bildas när blixten slår ner och når jorden i nederbörd. Men den mesta ammoniaken produceras av bakterier i vatten och jord som en slutprodukt av nedbrytning av växt- och djuravfall. Den finns i relativt låga, icke-toxiska koncentrationer i mark, luft och vatten och utgör en kvävekälla för växter.I mark och vatten genomgår ammoniak många komplexa biokemiska omvandlingar. Dessa omvandlingar utgör det som allmänt kallas för kvävecykeln. För en mer ingående diskussion om kvävecykeln se relaterade länkar.
Ammoniak i vatten
Vatten reagerar med ammoniak för att bilda ammonium- och hydroxidjoner. Ammoniak kallas ofta för ”unioniserad ammoniak”. Ammoniak är giftigt för vattenlevande organismer men ammonium är giftfritt. Det finns en jämvikt i vatten mellan den giftiga ammoniaken och det ogiftiga ammoniumet. Jämvikten skiftar fram och tillbaka beroende på befintliga eller införda miljöförändringar
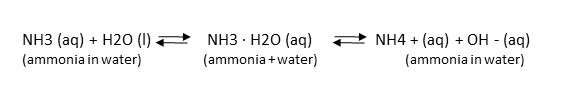
Den dynamiska jämvikten mellan NH3 och NH4 + påverkas av vattentemperatur och pH (surhet). Vid ett pH på sex är förhållandet mellan ammoniak och ammonium 1 till 3000 men minskar till 1 till 30 när pH stiger till åtta (blir mindre surt). Varmt vatten innehåller mer giftig ammoniak än kallare vatten. Vid provtagning av vatten för ammoniakanalys måste både temperaturen och pH-värdet i ytvattenförekomsten mätas samtidigt som vattenproverna samlas in. (Se Ammoniak, pH & Temperaturkalkylator)
Om ammoniak direkt sprids ut i ytvatten eller om vatten som används av en brandkår för att trycka ner ett ammoniakångmoln tillåts nå ytvatten, kan vattenlevande organismer skadas. Även vid en koncentration på 0,02 mg/L (48 timmars LC50) är unioniserad ammoniak dödlig för vissa känsliga sötvattenfiskar. Det motsvarar ungefär en halv kopp unioniserad ammoniak i en miljon liter vatten. Ammoniak är också mycket giftigt för ryggradslösa sötvattendjur med ett 48-timmars LC50 på 0,66 mg/L för Daphnia magna . Återigen, vatten som förorenats med ammoniak från gödselmedel bör inte tillåtas komma in i dagvattenledningar, floder, dräneringsdiken, våtmarker eller sjöar.
Ammoniak i luft och jord
När ammoniak släpps ut kommer ångorna att skingras och reagera med luftens fukt för att bilda ammonium och så småningom återvända till jorden i nederbörd. Ammonium binder då snabbt till det negativt laddade organiska materialet och leran i marken. Ammonium ackumuleras sällan i marken eftersom bakterier snabbt omvandlar det ammonium som inte tas upp av växtrötter till nitrater (nitrifikation). Nitrat kan också tas upp av rötterna eller läcka ut genom markprofilen. Eftersom ammonium är jordbundet kommer föroreningen sannolikt att stanna kvar horisontellt om inte jorden sköljs bort av regnhändelser, men läcka vertikalt som nitrater genom rotzonen.
Om brandkåren undertrycker ett ammoniakångmoln med vatten under en längre tidsperiod kan det applicerade vattnet kontaminera jorden. I detta fall kan marken kräva någon metod för sanering för att förhindra negativa miljöeffekter.
Ammoniak som påverkar växter

Plantor, träd och grödor består till största delen av vatten. Om ett stort utsläpp av ammoniak sker kommer ångorna sannolikt att bränna bladen på närliggande vegetation i vindriktningen. Ammoniak drar vatten från bladen men påverkar inte rötterna så skadade växter kommer förmodligen att återhämta sig helt även om drabbade grödor kan drabbas av skördeförluster.
Ammoniak som påverkar boskap
Var medveten om att ammoniakångor är giftiga för boskap. Mjölk-, svin- och fjäderfäproducenter som arbetar i närheten och i vindriktningen av ett utsläpp eller ett potentiellt utsläpp måste underrättas för att vidta lämpliga åtgärder.
The Nitrogen Cycle in Soil from The Ohio State University Extension Fact Sheet AEX-463-96