Az ammónia még rendkívül alacsony koncentrációban is károsítja a vízi életet. Az ammónia természetes módon fordul elő a környezetben. Kis mennyiségű ammónia keletkezik villámcsapáskor, és a csapadékkal a földbe jut. A legtöbb ammóniát azonban a vízben és a talajban lévő baktériumok termelik a növényi és állati hulladékok lebomlásának végtermékeként. Viszonylag alacsony, nem mérgező koncentrációban található meg a talajban, a levegőben és a vízben, és nitrogénforrást biztosít a növények számára.
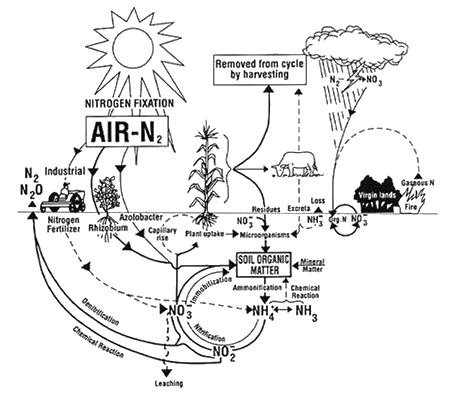
Az ammónia még rendkívül alacsony koncentrációban is károsítja a vízi életet. Az ammónia természetes módon fordul elő a környezetben. Kis mennyiségű ammónia keletkezik villámcsapáskor, és a csapadékkal a földbe jut. A legtöbb ammóniát azonban a vízben és a talajban lévő baktériumok termelik a növényi és állati hulladékok lebomlásának végtermékeként. Viszonylag alacsony, nem mérgező koncentrációban található meg a talajban, a levegőben és a vízben, és nitrogénforrást biztosít a növények számára.A talajban és a vízben az ammónia számos összetett biokémiai átalakuláson megy keresztül. Ezek az átalakulások alkotják azt, amit általában nitrogénciklusnak neveznek. A nitrogénciklus részletesebb tárgyalását lásd a kapcsolódó linkeken.
Az ammónia a vízben
A víz ammóniával reagálva ammónium- és hidroxidionokat képez. Az ammóniát gyakran nevezik “egyesített ammóniának”. Az ammónia mérgező a vízi szervezetekre, az ammónium azonban nem mérgező. A vízben egyensúly áll fenn a mérgező ammónia és a nem mérgező ammónium között. Az egyensúly oda-vissza változik a meglévő vagy bevezetett környezeti változások függvényében
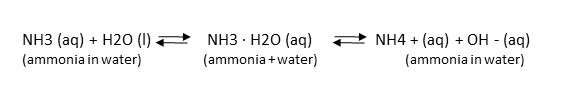
Az NH3 és az NH4+ közötti dinamikus egyensúlyt a víz hőmérséklete és pH-ja (savassága) befolyásolja. Hatos pH-nál az ammónia és ammónium aránya 1:3000, de 1:30-ra csökken, amikor a pH nyolcra emelkedik (kevésbé savas lesz). A meleg víz több mérgező ammóniát tartalmaz, mint a hidegebb víz. Amikor ammóniaelemzés céljából vízmintát veszünk, a vízmintavétellel egy időben meg kell mérni a felszíni víztest hőmérsékletét és pH-értékét is. (Lásd Ammónia, pH & Hőmérséklet kalkulátor)
Ha az ammónia közvetlenül a felszíni vízbe kerül, vagy ha a tűzoltóság által az ammónia gőzfelhő lefojtására használt víz a felszíni vízbe kerül, a vízi élővilág károsodhat. Az egyesített ammónia már 0,02 mg/L (48 órás LC50) koncentrációban is halálos egyes érzékeny édesvízi halakra. Ez körülbelül ½ csésze egyesített ammóniának felel meg egymillió gallon vízben. Az ammónia az édesvízi gerinctelenekre is rendkívül mérgező, 48 órás LC50 értéke 0,66 mg/l a Daphnia magna esetében. Ismétlem, a műtrágya ammóniával szennyezett víz nem kerülhet csapadékcsatornákba, folyókba, vízelvezető árkokba, vizes élőhelyekre vagy tavakba.
Az ammónia a levegőben és a talajban
Az ammónia kibocsátása után a gőzök eloszlanak, a levegő nedvességével reagálva ammóniumot képeznek, és végül az esővel visszatérnek a földbe. Az ammónium ezután gyorsan kötődik a talaj negatív töltésű szerves anyagához és a talaj agyagjához. Az ammónium ritkán halmozódik fel a talajban, mivel a baktériumok a növényi gyökerek által fel nem vett ammóniumot gyorsan nitrátokká alakítják (nitrifikáció). A nitrátok a gyökerek által is felszívódhatnak, vagy a talajprofilon keresztül kimosódhatnak. Mivel az ammónium talajhoz kötött, hacsak a talajt nem mossák el a csapadékesemények, a szennyeződés valószínűleg vízszintesen a helyén marad, de függőlegesen nitrátként a gyökérzónán keresztül kioldódik.
Ha a tűzoltóság hosszabb ideig vízzel elnyomja az ammónia gőzfelhőt, az alkalmazott víz szennyezheti a talajt. Ebben az esetben a talajban valamilyen helyreállítási módszerre lehet szükség a káros környezeti hatások megelőzése érdekében.
A növényekre ható ammónia

A növények, fák és termények nagyrészt vízből állnak. Ha nagy mennyiségű ammónia szabadul fel, a gőz valószínűleg megégeti a közeli, széllel szemben lévő növényzet leveleit. Az ammónia vizet von el a levelekből, de a gyökerekre nem hat, így a sérült növények valószínűleg teljesen felépülnek, bár az érintett növények terméskiesést szenvedhetnek.
Az ammónia hatása az állatállományra
Tudnia kell, hogy az ammónia gőzei mérgezőek az állatállományra. A tej-, sertés- és baromfitenyésztőket, akik a kibocsátás vagy potenciális kibocsátás közelében vagy széllel szemben tevékenykednek, értesíteni kell a megfelelő intézkedések megtétele érdekében.
The Nitrogen Cycle in Soil from The Ohio State University Extension Fact Sheet AEX-463-96