 Nawet w bardzo niskich stężeniach amoniak szkodzi życiu wodnemu. Amoniak występuje naturalnie w środowisku. Niewielka ilość amoniaku powstaje podczas uderzeń pioruna i dociera do ziemi w opadach deszczu. Jednak większość amoniaku jest wytwarzana przez bakterie w wodzie i glebie jako produkt końcowy rozkładu odpadów roślinnych i zwierzęcych. Występuje on w stosunkowo niskich nietoksycznych stężeniach w glebie, powietrzu i wodzie i stanowi źródło azotu dla roślin.
Nawet w bardzo niskich stężeniach amoniak szkodzi życiu wodnemu. Amoniak występuje naturalnie w środowisku. Niewielka ilość amoniaku powstaje podczas uderzeń pioruna i dociera do ziemi w opadach deszczu. Jednak większość amoniaku jest wytwarzana przez bakterie w wodzie i glebie jako produkt końcowy rozkładu odpadów roślinnych i zwierzęcych. Występuje on w stosunkowo niskich nietoksycznych stężeniach w glebie, powietrzu i wodzie i stanowi źródło azotu dla roślin.W glebach i wodzie amoniak przejdzie przez wiele złożonych przemian biochemicznych. Te transformacje stanowią to, co jest powszechnie znane jako cykl azotowy. Aby uzyskać bardziej dogłębną dyskusję na temat cyklu azotowego zobacz powiązane linki.
Ammoniak w wodzie
Woda reaguje z amoniakiem tworząc jony amonowe i wodorotlenkowe. Amoniak jest często określany jako „amoniak zunifikowany”. Amoniak jest toksyczny dla organizmów wodnych, ale amon jest nietoksyczny. W wodzie istnieje równowaga pomiędzy toksycznym amoniakiem a nietoksycznym amonem. Równanie to przesuwa się tam i z powrotem w zależności od istniejących lub wprowadzonych zmian środowiskowych
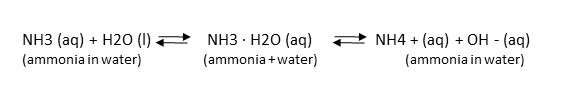
Na dynamiczną równowagę między NH3 i NH4 + wpływa temperatura wody i pH (kwasowość). Przy pH 6 stosunek amoniaku do amonu wynosi 1 do 3000, ale zmniejsza się do 1 do 30, gdy pH wzrasta do 8 (staje się mniej kwaśne). Ciepła woda będzie zawierać więcej toksycznego amoniaku niż chłodniejsza. Podczas pobierania próbek wody do analizy amoniaku, zarówno temperatura jak i pH wody powierzchniowej muszą być mierzone w tym samym czasie, w którym pobierane są próbki wody. (Patrz Amoniak, pH & Kalkulator temperatury)
Jeśli amoniak jest bezpośrednio rozlany do wód powierzchniowych lub jeśli woda używana przez straż pożarną do obniżenia chmury oparów amoniaku jest dopuszczona do wód powierzchniowych, życie wodne może zostać uszkodzone. Nawet w stężeniu 0,02 mg/L (48-godzinne LC50) amoniak jest śmiertelny dla niektórych wrażliwych ryb słodkowodnych. Odpowiada to około ½ filiżanki amoniaku związkowego w jednym milionie galonów wody. Amoniak jest również bardzo toksyczny dla bezkręgowców słodkowodnych, a jego 48-godzinne LC50 wynosi 0,66 mg/l dla Daphnia magna. Ponownie, woda zanieczyszczona amoniakiem z nawozu nie powinna być dopuszczona do kanalizacji burzowej, rzek, rowów melioracyjnych, terenów podmokłych lub jezior.
Ammoniak w powietrzu i glebie
Po uwolnieniu amoniaku opary rozpraszają się reagując z wilgocią w powietrzu tworząc amon i ostatecznie wracają na ziemię w opadach deszczu. Amonu następnie szybko wiąże się z ujemnie naładowanych materii organicznej gleby i gliny gleby. Amon rzadko gromadzi się w glebie, ponieważ bakterie szybko przekształcają amon, który nie jest pobierany przez korzenie roślin, w azotany (nitryfikacja). Azotany mogą być również wchłaniane przez korzenie lub mogą być wypłukiwane przez profil glebowy. Ponieważ amon jest związany z glebą, o ile gleba nie zostanie zmyta przez opady deszczu, skażenie prawdopodobnie pozostanie umieszczone poziomo, ale będzie wymywane pionowo jako azotany przez strefę korzeniową.
Jeśli straż pożarna tłumi chmurę oparów amoniaku wodą przez dłuższy okres czasu, zastosowana woda może skazić glebę. W tym przypadku gleba może wymagać jakiejś metody rekultywacji, aby zapobiec niekorzystnemu wpływowi na środowisko.
Amoniak wpływający na rośliny

Rośliny, drzewa i uprawy składają się głównie z wody. Jeśli dojdzie do dużego uwolnienia amoniaku, opary prawdopodobnie spalą liście pobliskich roślin rosnących pod wiatr. Amoniak pobierze wodę z liści, ale nie wpłynie na korzenie, więc uszkodzone rośliny prawdopodobnie w pełni się odrodzą, chociaż dotknięte uprawy mogą ponieść straty w plonach.
Amoniak wpływający na zwierzęta gospodarskie
Uważaj, że opary amoniaku są toksyczne dla zwierząt gospodarskich. Producenci mleka, trzody chlewnej i drobiu działający w pobliżu i pod wiatr od miejsca uwolnienia lub potencjalnego uwolnienia muszą zostać powiadomieni w celu podjęcia odpowiednich działań.
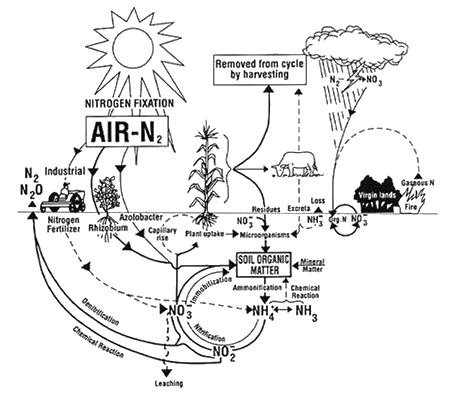
The Nitrogen Cycle in Soil from The Ohio State University Extension Fact Sheet AEX-463-96
.