Mark B. Abelson, MD, CM FRCSC, Daniel Dewey-Mattia, and Aron Shapiro, North Andover, Mass.
Ceratita acanthamoeba este o boală rară care amenință vederea și care, în Statele Unite și Europa, este întâlnită cu precădere în rândul purtătorilor de lentile de contact.1,2 Afecțiunea este cauzată de infecția cu protozoarul Acanthamoeba și este frecvent identificată greșit ca fiind una dintre cele mai frecvente forme fungice sau virale de cheratită, în special herpesul ocular.3 Traumatismele corneenei accidentale, care sunt mai frecvente în țările în curs de dezvoltare, și purtarea lentilelor de contact sunt principalii factori de risc pentru AK. Metodele de tratament au cel mai mare succes în stadii incipiente, astfel încât diagnosticarea promptă este crucială pentru a stopa progresia bolii. Pacienții aflați în stadii mai avansate se confruntă adesea cu un transplant de cornee ca unic mijloc de a-și recăpăta o acuitate vizuală mai mare decât simpla mișcare a mâinilor;4 astfel, AK ar trebui să fie o preocupare semnificativă în rândul purtătorilor de lentile de contact și al persoanelor care au suferit recent abraziuni corneene chirurgicale sau accidentale. Prevenirea este cea mai bună armă împotriva AK, deoarece majoritatea cazurilor pot fi atribuite în mod direct unei igiene deficitare a lentilelor de contact sau contactului direct al ochilor cu apa contaminată.
EcologiaAcanthamoeba
Acanthamoeba este unul dintre cele mai abundente protozoare de pe pământ. Membrii genului Acanthamoeba sunt aproape omniprezenți și au fost izolați din sol, praf, aer, apă de la robinet tratată și netratată, piscine, aparate de aer condiționat și numeroase alte medii domestice și exterioare.5 Ciclul de viață al protozoarelor constă într-o fază de trofozoit activ care se hrănește și o fază de chist latent, care este activată de condiții nefavorabile, cum ar fi expunerea la temperaturi extreme, pH ridicat sau scăzut, uscăciune sau înfometare.5 Rezistența în condiții nefavorabile (chisturile pot rămâne viabile timp de 24 de ani sau mai mult)6 îi permite lui Acanthamoeba o gamă ecologică largă și, de asemenea, o face un parazit formidabil la om.
Din moment ce Acanthamoeba este atât de răspândită în mediul nostru, este surprinzător faptul că infecțiile sunt atât de puțin frecvente. Nu se cunoaște modul în care sistemul nostru imunitar ne protejează de infecție, deși la om au fost descoperiți anticorpi specifici pentru Acanthamoeba.3 Au fost găsite dovezi ale prezenței Acanthamoeba în țesutul pulmonar și nazal atât la persoane bolnave, cât și la persoane sănătoase7 și, ca agent patogen oportunist, Acanthamoeba a fost cunoscută ca fiind cauza encefalitei fatale la pacienții imunocompromiși.5 Cu toate acestea, în cazul AK, infecția apare de obicei la persoanele imunocompetente, deși unele cercetări sugerează că unii pacienți cu AK pot fi susceptibili la agentul patogen din cauza lipsei de anticorpi specifici antigenului.3
Ceratita Acanthamoeba
Se estimează că au apărut 5.000 de cazuri de cheratită Acanthamoeba în Statele Unite începând cu anul 2006, dar din moment ce AK este atât de frecvent diagnosticată greșit și boala nu trebuie să fie raportată la Centrele pentru Controlul și Prevenirea Bolilor, numărul real ar putea fi mult mai mare.3 Națiunile în curs de dezvoltare din Asia și Africa, unde AK nu este, de obicei, asociată cu purtarea lentilelor, au o rată excepțional de ridicată de cheratită infecțioasă. Un studiu asupra pacienților purtători de lentile fără contact din India a raportat un rezultat vizual final foarte slab în comparație cu cercetările anterioare în rândul purtătorilor de lentile din țările occidentale.8 Acest lucru se poate datora variației între tulpinile de Acanthamoeba distincte din punct de vedere geografic sau pur și simplu statutului socio-economic inferior și lipsei de resurse medicale disponibile pentru participanții la studiu.8
AK a fost documentată pentru prima dată în Statele Unite în 1973, după ce un fermier și-a zgâriat corneea cu sârmă și fân, apoi a spălat rana cu apă de irigare.5 Informațiile diagnostice și clinice referitoare la boală au rămas puține până în anii 1980; cu toate acestea, au început să apară cercetări care implicau purtarea lentilelor de contact ca factor de risc predominant. Din 208 cazuri de AK raportate în Statele Unite între 1973 și 1988, 85 la sută erau purtători de lentile de contact.9 Primele cazuri documentate de AK legate de lentile au fost descoperite exclusiv în rândul persoanelor care își păstrau lentilele de contact în soluții saline făcute în casă cu sare de masă.9 De atunci, infecția a fost descoperită în rândul purtătorilor de lentile care foloseau soluții multifuncționale și dezinfectante cumpărate din magazine, majoritatea acestora omorând în mod eficient trofozoiții Acanthamoeba, dar nu și chisturile.10
Începând de la mijlocul anilor 1990, Statele Unite au înregistrat o creștere bruscă a numărului de cazuri de AK legate de lentile, în special în cadrul anumitor populații. Între iulie 1993 și decembrie 1994, un focar a dus la 43 de cazuri prezentate la University of Iowa Hospitals and Clinics.11 S-a crezut că epidemia a fost asociată cu inundațiile regionale și cu contaminarea ulterioară a rezervei de apă, deoarece 29 din cei 30 de pacienți dintr-un studiu au locuit în comitatele afectate de inundații.2 În mod similar, zona Chicago a înregistrat o creștere semnificativă a numărului de cazuri de AK începând cu iunie 2003, cu 63 de cazuri raportate până la sfârșitul anului 200611 în rândul unei populații care s-ar aștepta să aibă doar aproximativ două cazuri pe an.12 Numărul pacienților cu AK a crescut, de asemenea, în Portland,13 San Francisco,14 Boston4 și Philadelphia.4 Cercetările epidemiologice au constatat că aproximativ jumătate dintre pacienții cu AK din zona Chicago au folosit soluția „fără frecare” Complete Moisture Plus Multi-Purpose (Advanced Medical Optics) pentru curățarea și depozitarea lentilelor de contact.15 Această constatare a dus la o investigație a U.S. Food and Drug Administration și la o retragere voluntară de către AMO. Cercetările privind soluțiile comerciale „fără frecare” pentru contacte au arătat că aceste produse au o eficacitate minimă în ceea ce privește uciderea Acanthamoeba.16 S-a demonstrat că atât soluțiile de peroxid de hidrogen într-o singură etapă, cât și soluțiile de peroxid de hidrogen în două etape, care implică o a doua soluție de neutralizare, reprezintă o alternativă mai sigură la o soluție de depozitare „fără frecare”.10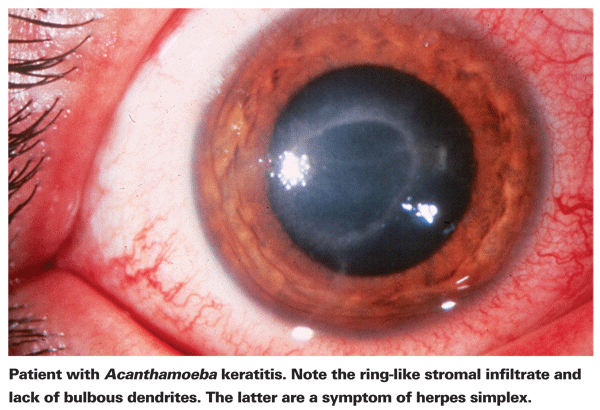
Studiile au început să arate că depozitarea și tratarea apei în comunitate pot juca, de asemenea, un rol important în apariția focarelor de AK. În Anglia, unde incidența AK este de 15 ori mai mare decât cea din Statele Unite, rezervoarele de apă de pe acoperișuri, care nu sunt spălate frecvent, pot servi ca medii excelente pentru dezvoltarea Acanthamoeba și pot explica ratele umflate de AK din această țară.17 Investigațiile efectuate după epidemia din zona Chicago au constatat că nu numai că creșterea AK a corespuns unei scăderi a clorării apei din oraș ca urmare a unui mandat al Agenției de Protecție a Mediului cu privire la subprodusele cancerigene, dar distanțele excepțional de lungi pe care se deplasează apa municipală în zonă ar fi putut lăsa timp pentru o declorinare suplimentară și colonizarea Acanthamoeba.12 Chiar dacă multe proceduri de tratare a apei nu sunt eficiente în distrugerea chisturilor, dezinfectanții, cum ar fi clorul, distrug în mod eficient trofozoiții liberi și inhibă creșterea și reproducerea protozoarelor.12
Utilizarea lentilelor de contact și a lacrimei corneene
Traumatismele corneene, intervențiile chirurgicale oculare și utilizarea lentilelor de contact sunt toți factori de risc pentru dezvoltarea cheratitei infecțioase.17 Atunci când stratul epitelial al corneei este deteriorat, acesta rămâne susceptibil la infecții provocate de ciuperci, bacterii sau protozoare.18 Înainte de utilizarea pe scară largă a lentilelor de contact, abraziunile corneene și expunerea la apă sau sol contaminat erau cei mai distinși factori de risc pentru AK.
Lentilele de contact pot ajuta Acanthamoeba să ajungă la nivelul corneei și să exacerbeze progresia bolii. Lentilele servesc ca o cale fizică de trecere de la o sursă contaminată (de exemplu, carcasa de depozitare a lentilelor sau apa de la robinet) direct la cornee. Lentilele, în special atunci când sunt purtate în mod necorespunzător sau pentru o perioadă mai lungă decât cea recomandată, erodează epiteliul corneei, permițând pătrunderea microbienelor.19
Utilizarea lentilelor este, de asemenea, asociată cu reglarea în sus a proteinelor receptoare manosilate de pe suprafața epitelială care sporesc capacitatea Acanthamoeba de a roade țesutul corneei.19 Biofilmele și depozitele de proteine mannosilate care se acumulează pe suprafața lentilelor determină trofozoiții să producă cantități crescute de mediatori ai apoptozei epiteliale și de proteaze care degradează matricea stromei corneene.19
Susceptibilitatea la infecția cu Acanthamoeba depinde, de asemenea, de tipul de lentile de contact pe care îl folosește o persoană. Lentilele de noapte îi expun pe utilizatori la un risc drastic mai mare de a dezvolta AK, deoarece o analiză a constatat o prevalență de 30 la sută a bolii în rândul utilizatorilor.20 În timp ce lentilele de unică folosință zilnică sunt tipul de lentile cel mai puțin susceptibile de a duce la infecție,21 persoanele care poartă lentile rigide sunt mai puțin predispuse la AK decât utilizatorii de lentile moi.22 Aproximativ 88 la sută din cazurile de AK legate de lentilele de contact apar la purtătorii de lentile de contact moi și 12 la sută la purtătorii de lentile rigide.23 Lentilele din ce în ce mai populare cu hidrogel de silicon cu purtare continuă sunt, de asemenea, o țintă mai ușoară pentru atașarea Acanthamoeba decât hidrogelurile convenționale.21
Semne și simptome clinice
Suferinzii de AK se plâng de obicei de roșeață, durere, scăderea acuității vizuale și sensibilitate la lumină.5 Cea mai distinctivă caracteristică clinică a AK este un pronunțat infiltrat stromal asemănător unui inel, despre care se crede că este compus din celule inflamatorii.5 Semnele de sclerită, inflamație corneană și hiperemie conjunctivală încep să apară pe măsură ce boala avansează.5 Dacă nu este tratată, Acanthamoeba se poate răspândi înapoi în retină și poate provoca corioretinită gravă,5 iar pacienții sunt adesea reduși la o acuitate vizuală de mișcare a mâinii sau orbire în aceste stadii ulterioare. Diagnosticul tardiv, un infiltrat inelar pronunțat și o infecție stromală profundă sunt toate asociate cu un rezultat vizual final mai slab.24 Pacienții care dezvoltă cheratită stromală sunt, de asemenea, mai susceptibili de a avea un rezultat vizual slab după tratament decât cei cu o infecție epitelială mai superficială.4
Diagnostic
Diagnosticul corect în stadii incipiente este esențial înainte ca Acanthamoeba să invadeze mai adânc în cornee și să provoace leziuni tisulare permanente. Din nefericire, la prima vizită, boala este mai frecvent diagnosticată drept cheratită herpetică simplex decât AK. Această identificare greșită poate duce la utilizarea de medicamente antivirale, ceea ce nu face decât să înrăutățească simptomele pentru pacient. În timpul diagnosticării, Acanthamoeba este adesea luată în considerare ca o cauză a infecției atunci când ulcerele corneene nu răspund la antibiotice. Această întârziere în diagnosticarea corectă permite parazitului să aibă timp suficient pentru a progresa mai departe în ochi.
Primul pas spre un diagnostic corect este o examinare precisă cu lampa cu fantă. Lampa cu fantă poate arăta dovezi ale Acanthamoeba fie prin prezența directă a acesteia, fie prin răspunsul imun asociat.24 Lipsa dendritelor bulboase tipice la pacienții cu herpes este un bun indicator că un pacient ar putea avea AK. Examinarea precoce și precisă cu lampa cu fantă este importantă la pacienții cu ulcer cornean, deoarece stadiul bolii în momentul diagnosticării AK este un predictor puternic al rezultatului vizual final.24
Dacă este disponibil, diagnosticul direct in-vivo poate fi efectuat cu ajutorul unui microscop confocal cu scanare în tandem avansat și al tomografului de retină Heidelberg II (HRT-II) cu modul cornee.7 Reacția în lanț a polimerazei poate fi, de asemenea, utilizată ca instrument de diagnosticare atunci când sunt disponibile prea puține celule pentru o determinare vizuală precisă.5 Dacă examinarea in-vivo și PCR nu sunt fezabile, cultivarea răzuielilor corneene poate fi un instrument neprețuit în diagnosticarea Acanthamoeba și diferențierea acesteia de herpesul ocular.
Răzuirea corneei cu un preparat de montaj umed cu hidroxid de potasiu trebuie utilizată dacă este posibilă examinarea microscopică.25 Trebuie efectuate răzuieli suplimentare folosind echipamente sterile până când există suficient material pentru plăci de cultură. Probele trebuie incubate la aproximativ 37 C pe o placă de agar non-nutrient acoperită cu Escherichia coli.24 În câteva zile, o cultură pozitivă va fi acoperită cu Acanthamoeba care se hrănește pe suprapunerea bacteriană.3
Tratament
Acanthamoeba este dificil de tratat, dar un management eficient poate împiedica un pacient să rămână orb la (cel puțin) un ochi. Antiinfecțioasele topice funcționează de obicei doar la pacienții în stadii incipiente, în timp ce intervenția chirurgicală este necesară în stadiile ulterioare. În 1985, a fost raportat primul tratament de succes al AK cu utilizarea propamidinei 0,1% și a neomicinei 1%.26 De atunci, terapia combinată a rămas pilonul principal al tratamentului, cu aplicarea a două sau mai multe antiamoebice topice pe tot parcursul zilei.
Antisepticele cationice eficiente, mai ales polihexametilen biguanida (PHMB, 0,02%) și clorhexidina (0,02%), au demonstrat eficacitate atât în monoterapie, cât și în terapia combinată cu o diamidină26 , cum ar fi Brolene (izetionat de propamidină și izetionat de dibromopropamidină).8 Antisepticele cationice sunt baze puternice al căror potențial antiamoebic provine din capacitatea lor de a liza celulele prin legarea la bistratul fosfolipidic și provocând leziuni mortale ale membranei27. Utilizarea acestor antiseptice a adus mari îmbunătățiri atât în rândul pacienților cu AK purtători de lentile de contact, cât și în rândul pacienților purtători de lentile de contact.8 Diamidinele acționează fie prin interferența cu transferul grupării metil, fie prin perturbarea directă a acizilor nucleici amibieni.28 Aplicarea orară a 0,1% de propamidină izetionat și 0,15% de dibromopropamidină a prezentat succese doar în stadiile incipiente ale bolii. Corticosteroizii sunt, de asemenea, prescrise uneori pentru a reduce inflamația și durerea, dar pot crește simultan patogenitatea amibelor prin suprimarea răspunsului imunitar al pacientului.29
Tratamentul chirurgical rămâne o opțiune necesară atunci când infecția a progresat dincolo de punctul de viabilitate antiinfecțioasă. Keratoplastia penetrantă este utilizată pentru a îndepărta și înlocui țesutul infectat și se continuă un regim antiseptic/ diamidină.
Ceratita cu acanthamoeba este o boală rară care, dacă nu este detectată, poate afecta permanent corneea și țesuturile anterioare, lăsând pacientul orb la unul sau la ambii ochi. Amenințarea AK trebuie luată în considerare atunci când se ia decizia de a folosi sau nu lentile de contact, precum și ce tip de lentile să se folosească. Importanța îngrijirii corespunzătoare a lentilelor nu poate fi supraestimată, deoarece este o modalitate sigură de a preveni nu numai infecția cu Acanthamoeba, ci și o serie de alte infecții neplăcute și mai comune. Conștientizarea comunității cu privire la pericolele asociate cu declorurarea și depozitarea apei stagnante, adoptarea pe scară mai largă a unor obiceiuri corecte în ceea ce privește lentilele de contact și diagnosticarea în cunoștință de cauză sunt singurele modalități de a trata în mod eficient Acanthamoeba și de a stopa prevalența sa în creștere.
Dr. Abelson, profesor clinic asociat de oftalmologie la Harvard Medical School și cercetător clinic senior la Schepens Eye Research Institute, este consultant în domeniul produselor farmaceutice oftalmologice. Dl Dewey-Mattia este redactor medical la ORA Clinical Research and Development din North Andover, iar dl. Shapiro este director de antiinfecțioase și antiinflamatoare la ORA.
1. Moore MB, McCulley JP, Luckenbach M, Gelender H, Newton C, McDonald MB, Visvesvara GS. Cheratită acanthamoeba asociată cu lentile de contact moi. Am J Ophthalmol 1985;100:3:396.
2. Meier PA, Mathers WD, Sutphin JE, Folberg R, Hwang T, Wenzel RP. O epidemie de presupusă cheratită Acanthamoeba care a urmat inundațiilor regionale. Arch Ophthalmol 1998;116:8:1090-4.
3. Visvesvara GS, Moura H, Schuster FL. Amibele patogene și oportuniste cu viață liberă: Acanthamoeba spp., Balamuthia mandrillaris, Naegleria fowleri și Sappinia diploidea. FEMS Immunol Med Microbiol 2007;50:1-26.
4. Thebpatiphat N, Hammersmith KM, Rocha FN, Rapuano CJ, Ayres BD, Laibson PR, Eagle RC, Cohen EJ. Acanthamoeba keratitis: Un parazit în creștere. Cornea 2007;26:6:6:701-6.
5. Marciano-Cabral F, Cabral G. Acanthamoeba spp. ca agenți de boală la om. Clin Microbiol Rev 2003;16:2:273-307.
6. Mazur T, Hadás E, Iwanicka I. The duration of the cyst stage and the viability and virulence of Acanthamoeba isolates. Trop Med and Parasitol 1995;46:2:106-8.
7. Schuster FL, Visvesvara GS. Amibele cu viață liberă ca agenți patogeni oportuniști și neoprotestanți ai oamenilor și animalelor. Int J Parasitology 2004;34:9:1001-27.
8. Sharma S, Garg P, Rao GN. Caracteristicile pacienților, diagnosticul și tratamentul cheratitei Acanthamoeba legate de lentilele fără contact. Br J Ophthalmol 2000;84:1103-8.
9. Stehr-Green JK, Bailey TM, Brandt FH, Carr JH, Bond WW, Visvesvara GS. Cheratita acanthamoeba la purtătorii de lentile de contact moi. Un studiu caz-control. JAMA 1987;258:1:57-60.
10. Hiti K, Walochnik J, Haller-Schober EM, Faschinger C, Aspöck H. Viabilitatea Acanthamoeba după expunerea la o soluție dezinfectantă multifuncțională pentru lentile de contact și la două sisteme de peroxid de hidrogen. Br J Ophthalmol 2002;86:2:144-6.
11. Shoff ME, Joslin CE, Tu EY, Kubatko L, Fuerst PA. Eficacitatea sistemelor de lentile de contact împotriva izolatelor recente de Acanthamoeba clinice și de apă de la robinet. Cornea 2008;27:6:713-9.
12. Joslin CE, Tu EY, McMahon TT, Passaro DJ, Stayner LT, Sugar J. Caracteristici epidemiologice ale unui focar de cheratită Acanthamoeba din zona Chicago. Am J Ophthalmol 2006;142:2:212-217.
13. Mathers W. Utilizarea unor concentrații mai mari de medicamente în tratamentul cheratitei Acanthamoeba. Arch Ophthalmol 2006;124:6:923.
14. Sansanayudh W, Cevallos V, Porco TC, Margolis TP, Lietman TM, Acharya NR. Cheratita cu Fusarium și Acanthamoeba: Poate un singur centru să detecteze focarele? Br J Ophthalmol 2008;95:5:720-1.
15. Joslin CE, Tu EY, Shoff ME, Booton GC, Fuerst PA, Mchahon TT, Anderson RJ, Dworkin MS, Sugar J, Davis FG, Stayner LT. Asocierea dintre utilizarea soluției pentru lentile de contact și cheratita Acanthamoeba. Am J Ophthalmol 2007;144:2:169-180.
16. Butcko V, McMahon TT, Joslin CE, Jones L. Cheratita microbiană și rolul frecării și clătirii. Eye Contact Lens 2007;33:6:421-3.
17. Kilvington S, Gray T, Gray T, Dart J, Morlet N, Beeching JR, Frazer DG, Matheson M. Acanthamoeba keratitis: Rolul apei domestice de la robinet în Regatul Unit. IOVS 2004;45:1:165-169.
18.Thomas PA, Geraldine P. Cheratită infecțioasă. Curr Opin Infect Dis 2007;20:2:129-41.
19.Alizadeth H, Neelam S, Hurt M, Niederkorn JY. Rolul purtării lentilelor de contact, al florei bacteriene și al proteazei patogene induse de mannoză în patogeneza cheratitei amibiene. Infect Immun 2005;73:2:1061-8.
20.Watt K, Swarbrick HA. Cheratita microbiană în ortokeratologia de noapte: Revizuirea primelor 50 de cazuri. Eye Contact Lens 2005;31:5:201-8.
21. Hammersmith KM. Diagnosticul și managementul cheratitei Acanthamoeba. Curr Opin Ophthalmol 2006;17:4:327-31.
22. Lam DS, Houang E, Fan DS, Lyon D, Seal D, Wong E; Grupul de studiu al cheratitei microbiene din Hong Kong. Incidența și factorii de risc pentru cheratita microbiană în Hong Kong: Comparație cu Europa și America de Nord. Eye 2002;16:5:608-18.
23. Seal DV. Acanthamoeba keratitis update – incidență, epidemiologie moleculară și noi medicamente pentru tratament. Eye 2003;17:8:8:893-905.
24. Tu EY, Joslin CE, Sugar J, Booton GC, Shoff ME, Fuerst PA. Valoarea relativă a microscopiei confocale și a raclajelor corneene superficiale în diagnosticul cheratitei Acanthamoeba. Cornea 2008;27:7:764-72.
25. Gupta N, Tandom R. Modalități de investigare în cheratita infecțioasă. Indian Journal of Ophthalmology 2008;56:3:209-1.3
26. Wright P, Warhurst D, Jones BR. Cheratita acanthamoeba tratată cu succes pe cale medicală. Br J Ophthalmol 1985;69:778-782.
27. Lim N, Goh D, Bunce C, Xing W, Fraenkel G, Poole TRG, Ficker L. Compararea polihexametilen biguanidei și a clorhexidinei ca agenți monoterapici în tratamentul cheratitei Acanthamoeba. Amer J Ophthalmol 2008;145:130.
28. Wysenbeek YS, Blank-Porat D, Harizman N, Wygnanski-Jaffe T, Keller N, Avni I. Tehnica recultivării: Individualizarea tratamentului cheratitei acanthamoeba. Cornea 2000;19:4:464-7.
29. Berger ST, Mondino BJ, Hoft RH, Donzis PB, Holland GN, Farley MK, Levenson JE, Managementul medical de succes al cheratitei Acanthamoeba. Amer J Ophthalmol 1990;110:4:395-403.
.