Mark B. Abelson, MD, CM FRCSC, Daniel Dewey-Mattia, e Aron Shapiro, North Andover, Mass.
Acanthamoeba keratitis é uma doença rara que ameaça a visão e que, nos Estados Unidos e na Europa, é encontrada predominantemente entre os utilizadores de lentes de contacto.1,2 A condição é causada pela infecção do protozoário Acanthamoeba e é comumente mal identificada como uma das formas mais comuns de ceratite fúngica ou viral, especialmente o herpes ocular.3 Traumatismos acidentais da córnea, mais comuns em países em desenvolvimento, e o uso de lentes de contato são os principais fatores de risco para AK. Os métodos de tratamento são mais bem sucedidos durante os estágios iniciais, portanto, o diagnóstico imediato é crucial para interromper a progressão da doença. Pacientes em estágios mais tardios são frequentemente confrontados com um transplante de córnea como seu único meio de recuperar uma acuidade visual de mais do que simplesmente movimentos da mão;4 assim, as AK devem ser uma preocupação significativa entre os usuários de lentes de contato e indivíduos que experimentaram recentemente abrasões corneanas cirúrgicas ou acidentais. A prevenção é a melhor arma contra as AK, pois a maioria dos casos pode ser atribuída directamente a uma má higiene das lentes de contacto ou ao contacto visual directo com água contaminada.
Acanthamoeba Ecologia
Acanthamoeba é um dos protozoários mais abundantes na Terra. Os membros do gênero Acanthamoeba são quase ubíquos e foram isolados do solo, poeira, ar, água de torneira tratada e não tratada, piscinas, unidades de ar condicionado e inúmeros outros ambientes domésticos e ao ar livre.5 O ciclo de vida dos protozoários consiste em uma fase ativa de trofozoite e fase de cisto dormente, que é ativado por condições desfavoráveis, tais como exposição a temperaturas extremas, pH alto ou baixo, secura ou inanição.5 A resiliência através de condições adversas (os cistos podem permanecer viáveis por 24 anos ou mais)6 permite ao Acanthamoeba uma ampla faixa ecológica e também o torna um parasita formidável em humanos.
Desde que o Acanthamoeba é tão prevalente no nosso ambiente, é surpreendente que as infecções sejam tão invulgares. Não se sabe como nossos sistemas imunológicos nos protegem contra infecções, embora anticorpos específicos do Acanthamoeba tenham sido descobertos em humanos.3 Evidências de Acanthamoeba foram encontradas em tecidos pulmonares e nasais de indivíduos doentes e saudáveis7 e como um patógeno oportunista Sabe-se que o Acanthamoeba tem causado encefalite fatal em pacientes imunocomprometidos.5 No entanto, em AK, a infecção ocorre tipicamente em indivíduos imunocompetentes, embora algumas pesquisas sugiram que alguns pacientes com AK podem ser suscetíveis ao patógeno devido à falta de anticorpos específicos para antígenos.3
Ceratite amebica
Estima-se que 5.000 casos de Acanthamoeba keratitis tenham ocorrido nos Estados Unidos em 2006, mas como a AK é tão comumente mal diagnosticada e a doença não precisa ser notificada aos Centros de Controle e Prevenção de Doenças, o número real pode ser muito maior.3 Nações em desenvolvimento na Ásia e África, onde a AK normalmente não está associada ao uso de lentes, têm uma taxa excepcionalmente alta de ceratite infecciosa. Um estudo de pacientes sem contato com lentes na Índia relatou um resultado visual final muito ruim em comparação com pesquisas anteriores entre os usuários de lentes nos países ocidentais.8 Isso pode ser devido à variação entre as linhagens de Acanthamoeba geograficamente distintas ou simplesmente ao status socioeconômico mais baixo e à falta de recursos médicos disponíveis para os participantes do estudo.8
AK foi documentado pela primeira vez nos Estados Unidos em 1973, após um agricultor ter arranhado sua córnea com arame e feno, depois lavou a ferida com água de irrigação.5 Informações diagnósticas e clínicas sobre a doença permaneceram esparsas até a década de 1980; entretanto, a pesquisa começou a surgir implicando o uso de lentes de contato como fator de risco predominante. Dos 208 casos de AK notificados nos Estados Unidos entre 1973 e 1988, 85% eram portadores de lentes de contacto.9 Casos documentados precocemente de AK relacionadas com lentes de contacto foram encontrados exclusivamente entre indivíduos que armazenavam os seus contactos em soluções salinas caseiras feitas com sal de mesa.9 Desde então, foi encontrada infecção entre os usuários de lentes usando soluções multiuso e desinfetantes, a maioria dos quais mata efetivamente os trofozoítos Acanthamoeba, mas não os cistos.10
A partir de meados dos anos 90, os Estados Unidos observaram um pico no número de casos de AK relacionados com lentilhas, especialmente dentro de certas populações. Entre julho de 1993 e dezembro de 1994, um surto levou a 43 casos apresentados à Universidade de Hospitais e Clínicas de Iowa.11 Acreditava-se que a epidemia estava associada a inundações regionais e subsequente contaminação do abastecimento de água, já que 29 dos 30 pacientes de um estudo viviam em condados afetados pelas inundações.2 Da mesma forma, a área de Chicago tem visto um aumento significativo de casos de AK desde junho de 2003, com 63 casos relatados até o final de 200611 entre uma população que deveria ter apenas cerca de dois casos por ano.12 O número de pacientes com AK também tem crescido em Portland,13 São Francisco,14 Boston4 e Filadélfia.4 Pesquisas epidemiológicas descobriram que cerca da metade de todos os pacientes com AK na área de Chicago tinha estado usando a solução “no-rub” Complete Moisture Plus Multi-Purpose (Advanced Medical Optics) para limpeza e armazenamento de seus contatos.15 Esta descoberta levou a uma investigação da U.S. Food and Drug Administration e a um recall voluntário pela AMO. Pesquisas relativas a soluções comerciais de contato “no-rub” mostraram que esses produtos têm eficácia mínima para matar o Acanthamoeba.16 Tanto o peróxido de hidrogênio em uma etapa quanto as soluções de peróxido de hidrogênio em duas etapas, que envolvem uma segunda solução neutralizante, mostraram ser uma alternativa mais segura para uma solução de armazenamento “no-rub”.10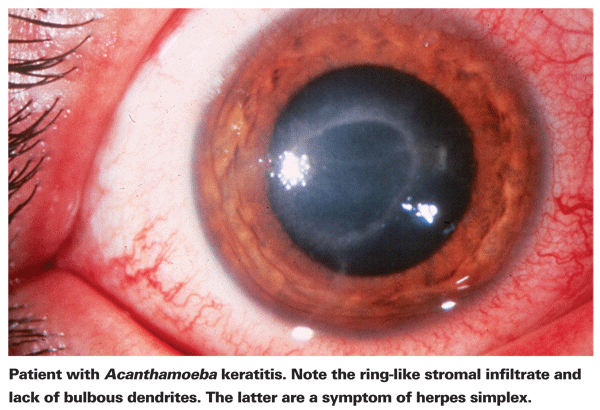
Estudos começaram a mostrar que o armazenamento e tratamento de água na comunidade também pode desempenhar um grande papel nos surtos de AK. Na Inglaterra, onde a incidência de AK é 15 vezes maior do que nos Estados Unidos, raramente os tanques de água de telhado com descarga podem servir como excelente meio para o crescimento de Acanthamoeba e podem explicar as taxas inchadas de AK do país.17 A investigação após o surto na área de Chicago descobriu que o aumento de AK não só correspondeu a uma diminuição da cloração da água da cidade, seguindo um mandato da Agência de Proteção Ambiental em relação aos subprodutos carcinogênicos, mas as distâncias excepcionalmente longas das viagens de água municipal na área podem ter dado tempo para a descloração adicional e colonização de Acanthamoeba.12 Apesar de muitos procedimentos de tratamento de água não serem eficazes na destruição de cistos, desinfetantes como o cloro destroem efetivamente os trofozoítos livres e inibem o crescimento e reprodução de protozoários.12
>
Desgaste de Contato e Lágrima Corneana
Traumatismo corneal, cirurgia ocular e uso de lentes de contato são fatores de risco para o desenvolvimento de ceratite infecciosa.17 Quando a camada epitelial da córnea é danificada, é deixada susceptível a infecção por fungos, bactérias ou protozoários.18 Antes do uso generalizado de lentes de contacto, as abrasões da córnea e a exposição a água ou solo contaminados eram os factores de risco mais distinguíveis para as AK.
Lentes de contacto podem ajudar o Acanthamoeba a alcançar a córnea e exacerbar a progressão da doença. As lentes servem como uma via física de passagem de uma fonte contaminada (isto é, estojo de armazenamento de lentes ou água da torneira) directamente para a córnea. As lentes, especialmente quando usadas indevidamente ou por mais tempo do que o recomendado, corroem o epitélio córneo, permitindo a entrada microbiana.19
O desgaste das lentes também está associado à upregulação das proteínas receptoras manosiladas na superfície epitelial que aumentam a capacidade do Acanthamoeba de comer o tecido córneo.19 Biofilmes e depósitos de proteínas manosiladas que se acumulam na superfície do cristalino fazem com que os trofozoítos produzam maiores quantidades de mediadores de apoptose epitelial e proteases que degradam a matriz do estroma corneano.19
Susceptibilidade à infecção por Acanthamoeba também depende do tipo de lente de contato que um indivíduo usa. Lentes para uso noturno colocam os usuários em um risco drasticamente maior de desenvolver AK, já que uma revisão encontrou uma prevalência de 30% da doença entre os usuários.20 Embora as lentes descartáveis diárias sejam o tipo de lente menos susceptível de levar à infecção,21 os indivíduos que usam lentes rígidas são menos propensos a AK do que os usuários de lentes macias.22 Aproximadamente 88% dos casos de AK relacionados a lentes de contato ocorrem em usuários de lentes de contato macias e 12% em usuários de lentes rígidas.23 As lentes de silicone hidrogel de uso contínuo, cada vez mais populares, também são um alvo mais fácil para a fixação de Acanthamoeba do que os hidrogéis convencionais.21
Sinais e Sintomas Clínicos
Sufferers de AK tipicamente queixam-se de vermelhidão, dor, diminuição da acuidade visual e sensibilidade à luz.5 A característica clínica mais distintiva de AK é um pronunciado infiltrado de estroma semelhante a um anel, que se acredita ser composto de células inflamatórias.5 Sinais de esclerite, inflamação corneana e hiperemia conjuntival começam a aparecer à medida que a doença progride.5 Se não for tratada, Acanthamoeba pode se espalhar de volta para a retina e causar corioretinite grave,5 e os pacientes são frequentemente reduzidos a uma acuidade visual de movimento da mão ou cegueira nestes estágios posteriores. O diagnóstico tardio, um pronunciado infiltrado anular e uma infecção profunda do estroma estão todos associados a um pior resultado visual final.24 Os pacientes que desenvolvem ceratite do estroma também têm maior probabilidade de ter um mau resultado visual após o tratamento do que aqueles com uma infecção epitelial mais superficial.4
Diagnóstico
Deve-se proceder a um diagnóstico precoce antes que o Acanthamoeba invada mais profundamente a córnea e cause danos permanentes nos tecidos. Infelizmente, na visita inicial a doença é mais comumente diagnosticada como herpes simplex keratitis do que AK. Esta identificação errada pode levar ao uso de medicamentos antivirais, o que só piora os sintomas para o paciente. Durante o diagnóstico, o Acanthamoeba é frequentemente considerado como uma causa de infecção quando as úlceras da córnea não respondem aos antibióticos. Este atraso no diagnóstico adequado permite que o parasita tenha tempo suficiente para progredir ainda mais no olho.
O primeiro passo para o diagnóstico adequado é o exame preciso da lâmpada-de-fenda. A lâmpada de fenda pode mostrar evidência de Acanthamoeba através de sua presença direta ou pela resposta imune associada.24 A falta de dendritos bulbosos típicos em pacientes com herpes é um bom indicador de que um paciente pode ter AK. O exame precoce e preciso da lâmpada de fenda é importante em pacientes com úlcera corneana, já que o estágio da doença no momento do diagnóstico de AK é um forte preditor do resultado visual final.24
Quando disponível, o diagnóstico direto in-vivo pode ser realizado usando um microscópio confocal avançado de varredura em tandem e o tomógrafo de retina II de Heidelberg (HRT-II) com módulo de córnea.7 A reação em cadeia da polimerase também pode ser usada como uma ferramenta de diagnóstico quando há muito poucas células disponíveis para uma determinação visual precisa.5 Se o exame in-vivo e a PCR não forem viáveis, o cultivo de raspas da córnea pode ser uma ferramenta inestimável no diagnóstico do Acanthamoeba e diferenciá-lo do herpes ocular.
Raspagem da córnea com um preparado de montagem úmida de hidróxido de potássio deve ser usado se o exame microscópico for possível.25 Raspagens adicionais devem ser realizadas usando equipamento estéril até que haja material suficiente para placas de cultura. As amostras devem ser incubadas a aproximadamente 37 C em uma placa de ágar não-nutriente revestida com Escherichia coli.24 Dentro de dias, uma cultura positiva será coberta com Acanthamoeba alimentando-se da cobertura bacteriana.3
Tratamento
Acanthamoeba é difícil de tratar, mas um tratamento eficaz pode impedir um paciente de ficar cego em (pelo menos) um olho. Os anti-infecciosos tópicos normalmente só funcionam em pacientes em estágio inicial, enquanto que a intervenção cirúrgica é necessária em estágios posteriores. Em 1985, o primeiro tratamento bem sucedido de AK foi relatado com o uso de propamidina 0,1% e neomicina 1%.26 Desde então, a terapia combinada tem permanecido a base do tratamento, com a aplicação de dois ou mais antiamoebicos tópicos ao longo do dia.
Antisépticos catiónicos eficazes, sobretudo o poli-hexametilenoglicol biguanida (PHMB, 0,02%) e a clorexidina (0,02%), mostraram eficácia tanto na monoterapia como na terapia combinada com uma diamidina26 como o Brolene (isotionato de propamidina e isotionato de dibromopropamidina).8 Os anti-sépticos catiónicos são bases fortes cujo potencial anti-amoebico deriva da sua capacidade de lise das células, ligando-se ao bocal fosfolípido e causando danos fatais à membrana.27 O uso desses antissépticos trouxe grandes melhorias tanto entre os pacientes com lentes sem contato quanto entre os que usam lentes de contato.8 As diamidinas funcionam interferindo na transferência do grupo metilo ou perturbando diretamente os ácidos nucleicos amebicos.28 A aplicação horária de 0,1% de isotionato de propamidina e 0,15% de dibromopropamidina tem apresentado sucesso apenas nos estágios iniciais da doença. Corticosteróides também são prescritos algumas vezes para reduzir a inflamação e a dor, mas podem simultaneamente aumentar a patogenicidade da ameba, suprimindo a resposta imunológica do paciente.29
O tratamento cirúrgico continua sendo uma opção necessária quando a infecção tiver progredido além do ponto de viabilidade antiinfecciosa. A queratoplastia penetrante é usada para remover e substituir o tecido infectado, e um regime anti-séptico/diamidínico é continuado.
Acanthamoeba keratitis é uma doença rara que, se não for detectada, pode danificar permanentemente a córnea e os tecidos anteriores, deixando o paciente cego em um ou ambos os olhos. A ameaça de AK deve ser considerada quando se toma a decisão de usar ou não lentes de contato, bem como o tipo de lente a ser usada. A importância de cuidar bem das lentes não pode ser exagerada, pois é uma forma segura de prevenir não só a infecção por Acanthamoeba, mas também uma série de outras infecções desagradáveis, e mais comuns. A consciência da comunidade sobre os perigos associados à descloração e ao armazenamento de água estagnada, a adopção mais generalizada de hábitos adequados de lentes de contacto e o diagnóstico conhecedor são as únicas formas de tratar o Acanthamoeba de forma eficaz e de travar a sua crescente prevalência.
Dr. Abelson, professor clínico associado de oftalmologia na Harvard Medical School e cientista clínico sénior no Schepens Eye Research Institute, consulta em fármacos oftálmicos. O Sr. Dewey-Mattia é escritor médico na ORA Pesquisa e Desenvolvimento Clínico em North Andover, e o Sr. Shapiro é director de anti-infecciosos e anti-inflamatórios na ORA.
1. Moore MB, McCulley JP, Luckenbach M, Gelender H, Newton C, McDonald MB, Visvesvara GS. Acanthamoeba keratitis associada a lentes de contato gelatinosas. Am J Ophthalmol 1985;100:3:396.
2. Meier PA, Mathers WD, Sutphin JE, Folberg R, Hwang T, Wenzel RP. Uma epidemia de presumível Acanthamoeba keratitis que se seguiu a uma inundação regional. Arch Ophthalmol 1998;116:8:1090-4.
3. Visvesvara GS, Moura H, Schuster FL. Amoebae patogênica e oportunista de vida livre: Acanthamoeba spp., Balamuthia mandrillaris, Naegleria fowleri, e Sappinia diploidea. FEMS Immunol Med Microbiol 2007;50:1-26.
4. Thebpatiphat N, Hammersmith KM, Rocha FN, Rapuano CJ, Ayres BD, Laibson PR, Eagle RC, Cohen EJ. Acanthamoeba keratitis: Um parasita em ascensão. Cornea 2007;26:6:701-6.
5. Marciano-Cabral F, Cabral G. Acanthamoeba spp. como agentes de doença em humanos. Clin Microbiol Rev 2003;16:2:273-307.
6. Mazur T, Hadás E, Iwanicka I. A duração do estágio do cisto e a viabilidade e virulência do Acanthamoeba isola. Trop Med e Parasitol 1995;46:2:106-8.
7. Schuster FL, Visvesvara GS. Amoebae livre como patógenos oportunistas e não esportistas de humanos e animais. Int J Parasitology 2004;34:9:1001-27.
8. Sharma S, Garg P, Rao GN. Características do paciente, diagnóstico e tratamento da Acanthamoeba keratitis sem contacto com as lentes. Br J Ophthalmol 2000;84:1103-8.
9. Stehr-Green JK, Bailey TM, Brandt FH, Carr JH, Bond WW, Visvesvara GS. Acanthamoeba keratitis em usuários de lentes de contato gelatinosas. Um estudo de caso-controle. JAMA 1987;258:1:57-60.
10. Hiti K, Walochnik J, Haller-Schober EM, Faschinger C, Aspöck H. Viabilidade do Acanthamoeba após exposição a uma solução polivalente de desinfecção de lentes de contacto e dois sistemas de peróxido de hidrogénio. Br J Ophthalmol 2002;86:2:144-6.
11. Shoff ME, Joslin CE, Tu EY, Kubatko L, Fuerst PA. Eficácia dos sistemas de lentes de contato contra os recentes isolados Acanthamoeba de água potável e clínica. Cornea 2008;27:6:713-9.
12. Joslin CE, Tu EY, McMahon TT, Passaro DJ, Stayner LT, Sugar J. Características epidemiológicas de um surto de Acanthamoeba keratitis da área de Chicago-área. Am J Ophthalmol 2006;142:2:212-217.
13. Mathers W. Uso de maiores concentrações de medicamentos no tratamento da Acanthamoeba keratitis. Arco Ophthalmol 2006;124:6:923.
14. Sansanayudh W, Cevallos V, Porco TC, Margolis TP, Lietman TM, Acharya NR. Fusarium e Acanthamoeba keratitis: Um único centro pode detectar surtos? Br J Ophthalmol 2008;95:5:720-1.
15. Joslin CE, Tu EY, Shoff ME, Booton GC, Fuerst PA, Mchahon TT, Anderson RJ, Dworkin MS, Sugar J, Davis FG, Stayner LT. A associação do uso de soluções de lentes de contato e Acanthamoeba keratitis. Am J Ophthalmol 2007;144:2:169-180.
16. Butcko V, McMahon TT, Joslin CE, Jones L. Ceratite microbiana e o papel da fricção e do enxaguamento. Lente de contacto visual 2007;33:6:421-3.
17. Kilvington S, Gray T, Dart J, Morlet N, Beeching JR, Frazer DG, Matheson M. Acanthamoeba keratitis: O papel da água da torneira doméstica no Reino Unido. IOVS 2004;45:1:165-169.
18.Thomas PA, Geraldine P. Ceratite infecciosa. Curr Opinião Infect Dis 2007;20:2:129-41.
19.Alizadeth H, Neelam S, Hurt M, Niederkorn JY. Papel do desgaste das lentes de contato, da flora bacteriana, e da protease patogênica induzida pelo homem na patogênese da ceratite amebica. Infect Immun 2005;73:2:1061-8.
20.Watt K, Swarbrick HA. Ceratite microbiana em orthokeratologia nocturna: Revisão dos primeiros 50 casos. Lente de contacto visual 2005;31:5:201-8.
21. Hammersmith KM. Diagnóstico e gestão da Acanthamoeba keratitis. Curr Opinião Ophthalmol 2006;17:4:327-31.
22. Lam DS, Houang E, Fan DS, Lyon D, Seal D, Wong E; Hong Kong Microbial Keratitis Study Group. Incidência e factores de risco para a ceratite microbiana em Hong Kong: Comparação com a Europa e América do Norte. Eye 2002;16:5:608-18.
23. Selo DV. Acanthamoeba keratitis update – incidência, epidemiologia molecular e novos medicamentos para tratamento. Olho 2003;17:8:893-905.
24. Tu EY, Joslin CE, Sugar J, Booton GC, Shoff ME, Fuerst PA. O valor relativo da microscopia confocal e raspagens superficiais da córnea no diagnóstico de Acanthamoeba keratitis. Córnea 2008;27:7:764-72.
25. Gupta N, Tandom R. Modalidades de investigação em queratites infecciosas. Indian Journal of Ophthalmology 2008;56:3:209-1.3
26. Wright P, Warhurst D, Jones BR. Acanthamoeba keratitis tratada medicamente com sucesso. Br J Ophthalmol 1985;69:778-782.
27. Lim N, Goh D, Bunce C, Xing W, Fraenkel G, Poole TRG, Ficker L. Comparação de poli-hexametileno biguanida e clorexidina como agentes monoterápicos no tratamento da ceratite Acanthamoeba. Amer J Ophthalmol 2008;145:130.
28. Wysenbeek YS, Blank-Porat D, Harizman N, Wygnanski-Jaffe T, Keller N, Avni I. A técnica de recultura: Individualizar o tratamento da acanthamoeba keratitis. Córnea 2000;19:4:464-7.
29. Berger ST, Mondino BJ, Hoft RH, Donzis PB, Holland GN, Farley MK, Levenson JE, Gestão médica bem sucedida da ceratite acanthamoeba. Amer J Ophthalmol 1990;110:4:395-403.