Auch bei extrem niedrigen Konzentrationen wird das Leben im Wasser durch Ammoniak geschädigt. Ammoniak kommt natürlich in der Umwelt vor. Eine geringe Menge Ammoniak entsteht bei Blitzeinschlägen und gelangt mit dem Niederschlag auf die Erde. Der größte Teil des Ammoniaks wird jedoch von Bakterien im Wasser und im Boden als Endprodukt der Zersetzung von pflanzlichen und tierischen Abfällen produziert. Es kommt in relativ geringen, ungiftigen Konzentrationen im Boden, in der Luft und im Wasser vor und stellt eine Stickstoffquelle für Pflanzen dar.
Auch bei extrem niedrigen Konzentrationen wird das Leben im Wasser durch Ammoniak geschädigt. Ammoniak kommt natürlich in der Umwelt vor. Eine geringe Menge Ammoniak entsteht bei Blitzeinschlägen und gelangt mit dem Niederschlag auf die Erde. Der größte Teil des Ammoniaks wird jedoch von Bakterien im Wasser und im Boden als Endprodukt der Zersetzung von pflanzlichen und tierischen Abfällen produziert. Es kommt in relativ geringen, ungiftigen Konzentrationen im Boden, in der Luft und im Wasser vor und stellt eine Stickstoffquelle für Pflanzen dar.Im Boden und im Wasser durchläuft Ammoniak viele komplexe biochemische Umwandlungen. Diese Umwandlungen bilden das, was gemeinhin als Stickstoffkreislauf bekannt ist. Eine ausführlichere Erörterung des Stickstoffkreislaufs finden Sie unter den entsprechenden Links.
Ammoniak im Wasser
Wasser reagiert mit Ammoniak und bildet Ammonium- und Hydroxidionen. Ammoniak wird oft als „gewerkschaftliches Ammoniak“ bezeichnet. Ammoniak ist für Wasserorganismen giftig, während Ammonium ungiftig ist. Im Wasser besteht ein Gleichgewicht zwischen dem giftigen Ammoniak und dem ungiftigen Ammonium. Das Gleichgewicht verschiebt sich je nach bestehenden oder eingeführten Umweltveränderungen hin und her
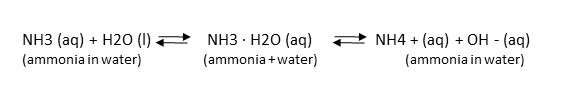
Das dynamische Gleichgewicht zwischen NH3 und NH4 + wird durch die Wassertemperatur und den pH-Wert (Säuregehalt) beeinflusst. Bei einem pH-Wert von sechs beträgt das Verhältnis von Ammoniak zu Ammonium 1 zu 3000, sinkt aber auf 1 zu 30, wenn der pH-Wert auf acht ansteigt (weniger sauer wird). Warmes Wasser enthält mehr giftiges Ammoniak als kühleres Wasser. Bei der Entnahme von Wasserproben für die Ammoniakanalyse müssen sowohl die Temperatur als auch der pH-Wert des Oberflächengewässers gleichzeitig mit der Entnahme der Wasserproben gemessen werden. (Siehe Ammoniak, pH & Temperaturrechner)
Wenn Ammoniak direkt in Oberflächengewässer gelangt oder wenn Wasser, das von der Feuerwehr verwendet wird, um eine Ammoniakdampfwolke zu verdrängen, in Oberflächengewässer gelangt, kann das Leben im Wasser geschädigt werden. Selbst bei einer Konzentration von 0,02 mg/L (48 Stunden LC50) ist gewerkschaftlich gebundenes Ammoniak für einige empfindliche Süßwasserfische tödlich. Das entspricht etwa ½ Tasse Ammoniak in einer Million Liter Wasser. Ammoniak ist auch hochgiftig für wirbellose Süßwassertiere mit einer 48-Stunden-LC50 von 0,66 mg/L für Daphnia magna . Auch hier gilt, dass Wasser, das mit Ammoniak aus Düngemitteln verunreinigt ist, nicht in Regenwasserabflüsse, Flüsse, Entwässerungsgräben, Feuchtgebiete oder Seen gelangen darf.
Ammoniak in Luft und Boden
Nach der Freisetzung von Ammoniak verflüchtigen sich die Dämpfe und reagieren mit der Feuchtigkeit in der Luft zu Ammonium, das schließlich mit dem Regen auf den Boden zurückkehrt. Ammonium bindet sich dann schnell an die negativ geladene organische Substanz und den Ton im Boden. Ammonium sammelt sich nur selten im Boden an, da Bakterien das Ammonium, das nicht von den Pflanzenwurzeln aufgenommen wird, rasch in Nitrate umwandeln (Nitrifikation). Nitrate können auch von den Wurzeln absorbiert werden oder durch das Bodenprofil versickern. Da Ammonium im Boden gebunden ist, wird die Verunreinigung wahrscheinlich horizontal verbleiben, aber vertikal als Nitrate durch die Wurzelzone versickern, es sei denn, der Boden wird durch Regenfälle weggespült.
Wenn die Feuerwehr eine Ammoniakdampfwolke über einen längeren Zeitraum mit Wasser unterdrückt, kann das eingesetzte Wasser den Boden kontaminieren. In diesem Fall muss der Boden möglicherweise saniert werden, um schädliche Auswirkungen auf die Umwelt zu verhindern.
Ammoniak wirkt sich auf Pflanzen aus

Pflanzen, Bäume und Nutzpflanzen bestehen größtenteils aus Wasser. Wenn Ammoniak in großem Umfang freigesetzt wird, verbrennt der Dampf wahrscheinlich die Blätter der in der Nähe befindlichen Pflanzen im Wind. Ammoniak entzieht den Blättern Wasser, wirkt sich aber nicht auf die Wurzeln aus, so dass sich geschädigte Pflanzen wahrscheinlich wieder vollständig erholen, auch wenn die betroffenen Pflanzen Ertragseinbußen erleiden können.
Ammoniak wirkt sich auf den Viehbestand aus
Achten Sie darauf, dass Ammoniakdämpfe giftig für das Vieh sind. Milchvieh-, Schweine- und Geflügelhalter, die in der Nähe oder im Windschatten einer Freisetzung oder einer möglichen Freisetzung arbeiten, müssen benachrichtigt werden, damit sie entsprechende Maßnahmen ergreifen können.
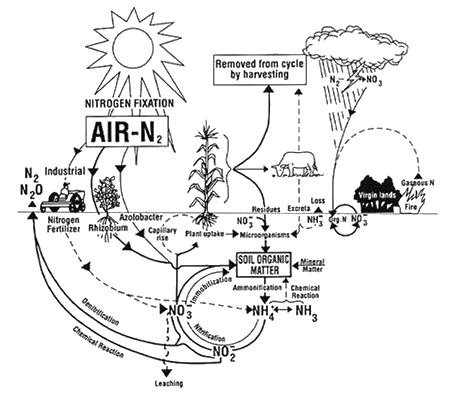
Der Stickstoffkreislauf im Boden aus dem Informationsblatt AEX-463-96 der Ohio State University