 Even at extremely low concentrations aquatic life will be harmed by ammonia.アンモニアは極めて低い濃度であっても、水生生物に害を及ぼします。 アンモニアは環境中に自然に存在します。 落雷の際に少量のアンモニアが発生し、降雨で地上に到達します。 しかし、ほとんどのアンモニアは、水中や土壌中のバクテリアによって、植物や動物の排泄物の分解の最終産物として生成されます。 土壌、空気、水中に比較的低い無毒性濃度で存在し、植物に窒素源を提供する。
Even at extremely low concentrations aquatic life will be harmed by ammonia.アンモニアは極めて低い濃度であっても、水生生物に害を及ぼします。 アンモニアは環境中に自然に存在します。 落雷の際に少量のアンモニアが発生し、降雨で地上に到達します。 しかし、ほとんどのアンモニアは、水中や土壌中のバクテリアによって、植物や動物の排泄物の分解の最終産物として生成されます。 土壌、空気、水中に比較的低い無毒性濃度で存在し、植物に窒素源を提供する。土壌や水中でアンモニアは多くの複雑な生化学的変換を経ることになる。 これらの変換は、一般に窒素サイクルとして知られているものを構成しています。
水中のアンモニア
水はアンモニアと反応して、アンモニウムイオンと水酸化物イオンを形成します。 アンモニアはしばしば「組合されたアンモニア」と呼ばれます。 アンモニアは水生生物に毒性があるが、アンモニウムは無毒である。 水中では、有毒なアンモニアと無毒なアンモニウムの間に平衡が存在します。 この平衡は、既存の、または導入された環境変化
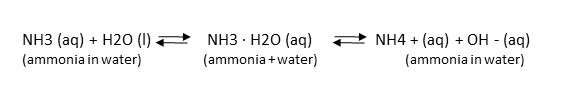
NH3とNH4 +の間の動的平衡は、水温とpH(酸性度)に影響されます。 pH6ではアンモニアとアンモニウムの比率は1対3000であるが、pHが8まで上昇すると1対30に減少する(酸性度が低くなる)。 水温が高いほど有毒なアンモニアが多く含まれ、水温が低いほど有毒なアンモニアが多く含まれます。 アンモニア分析のために水を採取する場合は、水サンプルを採取すると同時に、表流水の温度とpHの両方を測定する必要があります。 (アンモニア、pH & 温度計算機を参照)
アンモニアが地表水に直接こぼれた場合、または消防署がアンモニアの蒸気雲を抑えるために使用した水が地表水に到達した場合、水生生物に害を与える可能性があります。 0.02 mg/L (48 時間 LC50) の濃度であっても、組合されたアンモニアは、一部の敏感な淡水魚にとって致死的です。 これは、100万ガロンの水にカップ1/2杯のアンモニアが含まれることになります。 また、アンモニアは淡水の無脊椎動物にも強い毒性を示し、ミジンコの48時間LC50は0.66 mg/Lです。 5292>
Ammonia in Air and Soil
アンモニアを放出した後、蒸気は空気中の水分と反応してアンモニウムを形成し、最終的には降雨で地上に戻ってきます。 そして、アンモニウムはマイナスに帯電した土壌有機物や土壌粘土に素早く結合します。 植物の根に取り込まれなかったアンモニウムは、バクテリアによって速やかに硝酸塩に変換されるため(硝化)、アンモニウムが土壌に蓄積されることはほとんどない。 硝酸塩は、根から吸収されたり、土壌中に浸出したりすることもある。 アンモニウムは土壌と結合しているので、降雨によって土壌が洗い流されない限り、汚染は水平方向にとどまり、根域を通じて硝酸塩として垂直方向に浸出する可能性があります。
消防署がアンモニアの蒸気雲を長期間にわたって水で抑えた場合、適用した水が土壌を汚染する可能性があります。 この場合、環境への悪影響を防ぐために、土壌を何らかの方法で修復する必要があるかもしれません。
Ammonia Affecting Plants

植物、木、作物は、ほとんどが水でできています。 アンモニアの大量放出が起こった場合、蒸気はおそらく近くの風下の植物の葉を燃やすでしょう。 アンモニアは葉から水を引き抜きますが、根には影響しないので、被害を受けた作物は収量が減るかもしれませんが、おそらく完全に回復します。
Ammonia Affecting Livestock
アンモニアの蒸気は家畜に有害であることを認識しておいてください。
The Nitrogen Cycle in Soil from The Ohio State University Extension Fact Sheet AEX-463-96
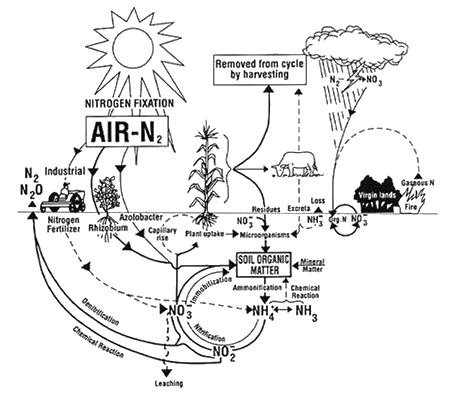
(英語版のみ。