 Même à des concentrations extrêmement faibles, la vie aquatique sera endommagée par l’ammoniac. L’ammoniac est présent naturellement dans l’environnement. Une petite quantité d’ammoniac est générée lorsque la foudre frappe et atteint la terre dans les précipitations. Mais la majeure partie de l’ammoniac est produite par des bactéries dans l’eau et le sol comme produit final de la décomposition des déchets végétaux et animaux. On le trouve en concentrations non toxiques relativement faibles dans le sol, l’air et l’eau et il constitue une source d’azote pour les plantes.
Même à des concentrations extrêmement faibles, la vie aquatique sera endommagée par l’ammoniac. L’ammoniac est présent naturellement dans l’environnement. Une petite quantité d’ammoniac est générée lorsque la foudre frappe et atteint la terre dans les précipitations. Mais la majeure partie de l’ammoniac est produite par des bactéries dans l’eau et le sol comme produit final de la décomposition des déchets végétaux et animaux. On le trouve en concentrations non toxiques relativement faibles dans le sol, l’air et l’eau et il constitue une source d’azote pour les plantes.Dans les sols et l’eau, l’ammoniac va subir de nombreuses transformations biochimiques complexes. Ces transformations constituent ce qui est communément appelé le cycle de l’azote. Pour une discussion plus approfondie du cycle de l’azote, voir les liens connexes.
L’ammoniac dans l’eau
L’eau réagit avec l’ammoniac pour former des ions ammonium et hydroxyde. L’ammoniac est souvent appelé « ammoniac syndiqué ». L’ammoniac est toxique pour les organismes aquatiques mais l’ammonium ne l’est pas. Il existe un équilibre dans l’eau entre l’ammoniac toxique et l’ammonium non toxique. L’équation se déplace d’avant en arrière en fonction des changements environnementaux existants ou introduits
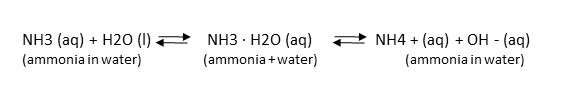
L’équilibre dynamique entre NH3 et NH4 + est affecté par la température de l’eau et le pH (acidité). À un pH de six, le rapport entre l’ammoniac et l’ammonium est de 1 à 3000, mais il diminue à 1 à 30 lorsque le pH s’élève à huit (devient moins acide). L’eau chaude contient plus d’ammoniac toxique que l’eau plus froide. Lors de l’échantillonnage de l’eau pour l’analyse de l’ammoniac, la température et le pH de la masse d’eau de surface doivent être mesurés en même temps que les échantillons d’eau sont prélevés. (Voir Ammoniac, pH & Calculateur de température)
Si l’ammoniac est directement déversé dans les eaux de surface ou si l’eau utilisée par un service d’incendie pour déprimer un nuage de vapeur d’ammoniac peut atteindre les eaux de surface, la vie aquatique peut être endommagée. Même à une concentration de 0,02 mg/L (CL50 sur 48 heures), l’ammoniac syndiqué est mortel pour certains poissons d’eau douce sensibles. Cela équivaut à environ ½ tasse d’ammoniac syndiqué dans un million de gallons d’eau. L’ammoniac est également très toxique pour les invertébrés d’eau douce, avec une CL50 sur 48 heures de 0,66 mg/l pour Daphnia magna. Encore une fois, l’eau contaminée par l’ammoniac des engrais ne doit pas être autorisée à pénétrer dans les collecteurs d’eaux pluviales, les rivières, les fossés de drainage, les zones humides ou les lacs.
L’ammoniac dans l’air et le sol
Après un rejet d’ammoniac, les vapeurs vont se dissiper en réagissant avec l’humidité de l’air pour former de l’ammonium et finalement retourner à la terre dans les précipitations. L’ammonium se lie alors rapidement à la matière organique et aux argiles du sol, chargées négativement. L’ammonium s’accumule rarement dans le sol car les bactéries transforment rapidement en nitrates (nitrification) l’ammonium qui n’est pas absorbé par les racines des plantes. Les nitrates peuvent également être absorbés par les racines ou être lessivés à travers le profil du sol. Comme l’ammonium est lié au sol, à moins que le sol ne soit emporté par des événements pluvieux, la contamination restera probablement en place horizontalement mais sera lessivée verticalement sous forme de nitrates à travers la zone racinaire.
Si le service d’incendie supprime un nuage de vapeur d’ammoniac avec de l’eau pendant une période prolongée, l’eau appliquée peut contaminer le sol. Dans ce cas, le sol peut nécessiter une certaine méthode de remédiation pour prévenir les effets néfastes sur l’environnement.
L’ammoniac affecte les plantes

Les plantes, les arbres et les cultures sont principalement constitués d’eau. Si un important rejet d’ammoniac se produit, la vapeur brûlera probablement les feuilles de la végétation voisine sous le vent. L’ammoniac arrachera l’eau des feuilles mais n’affectera pas les racines, de sorte que les plantes endommagées se rétabliront probablement complètement, bien que les cultures touchées puissent subir une perte de rendement.
L’ammoniac affectant le bétail
Sachez que les vapeurs d’ammoniac sont toxiques pour le bétail. Les éleveurs de vaches laitières, de porcs et de volailles opérant à proximité et sous le vent d’un rejet ou d’un rejet potentiel doivent être avertis pour prendre les mesures appropriées.
Le cycle de l’azote dans le sol à partir de la fiche de vulgarisation AEX-463-96 de l’Université de l’État de l’Ohio
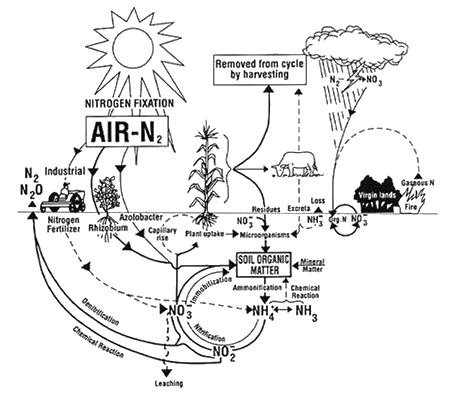
.