Introduktion
Enligt Världshälsoorganisationen påverkar depression uppskattningsvis 350 miljoner människor världen över (Organization, 2017). Patienter med depression uppvisar symtom på ångeststörningar och åtföljs av en oförmåga att uppleva glädje och intresse, koncentrationsförlust, självtvivel, social ångest, sömn- och aptitstörningar (Namola et al., 2015). De viktigaste faktorerna som orsakar depression är kemikalier eller hormoner i obalans i hjärnan. Det viktigaste hormonet som förknippas med depression är serotonin. Andra hormoner är noradrenalin och dopamin (Yi et al., 2008). Dessa hormoner är nödvändiga för normal hjärnfunktion och för att kontrollera känslor. Förstörelse av dessa hormoner kan orsaka kemisk obalans i hjärnan vilket resulterar i depression.
Depression kan behandlas beroende på dess svårighetsgrad, med psykoterapi eller medicinering. Antidepressiva medel är de viktigaste typerna av läkemedel som används för att behandla depression. Det finns många olika typer av antidepressiva läkemedel tillgängliga, och de skiljer sig endast åt i hur de verkar på hjärnan, deras kostnad och deras biverkningsprofil. I första linjens behandling förskrivs de flesta patienter antingen ett tricykliskt antidepressivt läkemedel (TCA) eller en selektiv serotoninåterupptagshämmare (SSRI; McCarthy et al., 2016). De läkemedel som vanligtvis används för ångestbehandlingar är bensodiazepiner. Även om det finns många antidepressiva läkemedel på marknaden som används för att behandla depression är efterverkningarna av användningen av dessa läkemedel ett stort bekymmer (Binfaré et al., 2009). En alternativ behandling av depression är användningen av växtbaserade läkemedel (Fajemiroye et al., 2016). Användningen av växtbaserade extrakt får allt större acceptans bland läkarkåren och patienterna. Majoriteten av de växtbaserade läkemedel som används för behandling av depression är råa eller halvpurifierade extrakt (Calixto et al., 2000; Carlini, 2003; Guan och Liu, 2016).
Det råder brist på rapporter om forskning som involverar den aktiva principen som kan framkalla aktivitet på det centrala nervsystemet (CNS). En översikt av Carlini (2003) innehåller information av endast om psykoanaleptiska, psykoleptiska och psykodysleptiska effekter. I en nyligen publicerad översikt av Guan och Liu (2016) diskuteras struktur-aktivitetsförhållandet för de antidepressiva effekterna av flavonoider som isolerats från naturliga och syntetiska källor. Syntetiska indolalkaloider, deras aktivitet och potentiella användning inom medicinen har redan granskats i flera artiklar (de Sa et al., 2009). Det har dock inte publicerats någon översiktsartikel som korrelerar växtindolalkaloider som isolerats med antidepressiv aktivitet. Denna översikt ger information om potentialen hos naturliga indolalkaloider för behandling av neurologiska störningar, studier av struktur-aktivitetssamband och omfattningen av dessa till andra bioaktiva metaboliter som potentiella antidepressiva läkemedelsspår utifrån den kemiska strukturen. Den är sammanställd genom bibliografisk undersökning av vetenskapliga tidskrifter och relevant litteratur som identifierats genom de elektroniska databaserna Web of Science.
Antidepressiva växter
Denna översiktsartikel handlar om växter som besitter aktivitet på CNS. Även om många typer av växter faller in i denna kategori kommer vi endast att lyfta fram växter som uppvisar antidepressiva egenskaper. Två växter som innehåller indolalkaloider är Passiflora incarnata L. (passionsblomma) och Mitragyna speciosa (Korth.) Havil (kratom), medan de andra två växterna som inte visade på förekomst av indolalkaloider är Piper methysticum G. Forst (kava) och Valeriana officinalis L., förtjänar särskild uppmärksamhet. Kemisk struktur av isolerade föreningar från dessa växter kan användas som grund för utveckling av nya läkemedel.
Passiflora incarnata och andra arter som P. alata Curtis, P. coerulea L. och P. edulis Sims används i stor utsträckning som lugnande medel i den traditionella medicinen i de flesta europeiska länder och i Amerika (Houghton och Seth, 2003). Strukturen hos bensodiazepinläkemedel består av en bensenring som är fusionerad med ett diazepinsystem som består av en sjuklöverig heterocyklisk enhet med två kväveatomer i positionerna 1 och 2 i ringen. Indolalkaloider som isolerats från P. incarnata nämligen harman, harmol, harmin, harmalol och harmalin består av en bensenring som är fusionerad med en femledad heterocykel som innehåller en kväveatom.
Flera studier har indikerat att P. incarnata har en farmakologisk profil som liknar bensodiazepiner och verkar genom GABA-receptorer (gamma-aminosmörsyra (GABA)) (Jawna-Zboiñska et al., 2016). Bladen av M. speciosa har använts som traditionell medicin för att behandla diarré, diabetes och för att förbättra blodcirkulationen (Vicknasingam et al., 2010). Mitragynin är den viktigaste indolalkaloiden som finns i M. speciosa med dess analoger, speciogynin, paynanthein och speciociliatin (León et al., 2009). Två studier som utfördes på vattenhaltigt extrakt och alkaloidalt extrakt av M. speciosa inducerade antidepressiv liknande effekt på musmodeller av beteendemässig förtvivlan (Kumarnsit et al., 2007). En studie utförd av Idayu et al. (2011) på mitragynin visar effekten av antidepressiva medel i djurens beteendemässiga modell av depression genom interaktion med hypotalamus-hypofys-binjureaxeln (HPA-axeln) i det neuroendokrina systemet (Idayu et al., 2011).
Piper methysticum G. Forst konsumeras som en dryck som kallas kava och som inducerar ett behagligt mentalt tillstånd mot att man känner sig glad samtidigt som trötthet och ångest minskas (Bilia et al., 2002). Studien visar att de flesta farmakologiska aktiviteterna bibehålls från det lipidlösliga extraktet jämfört med det vattenhaltiga extraktet. Det lipidlösliga extraktet innehåller minst sju pyroner, kända som kavalakton. Kavalaktoner interagerar i allmänhet med de dopaminerga, serotonin, gammaaminosmörsyra (GABA), glutamatergiska neurotransmissionerna, förhindrar monoaminoxidas B (MOB) och ger också en mängd olika effekter på jonkanaler (Grunze et al., 2001). Dihydrometysticin är en av de sex viktigaste kavalaktonerna som finns i kavaplantan. Strukturen hos dihydrometysticin består av en aryletylen-α-pyron som är bunden till en indolliknande enhet som omfattar två oxygener i stället för nitrogener. Det bidrar till anxiolytisk aktivitet och fungerar som antidepressiva läkemedel. Dubbelblinda placebokontrollerade studier visade att kavalaktoner ger anxiolytiska effekter utan att deprimera mentala och motoriska funktioner och förbättrar sömnkvaliteten. Kavalaktoner är ett alternativ för att ersätta användningen av bensodiazepiner i depressionsbehandling (Malsch och Kieser, 2001).
Valeriana officinalis L., även känd som valerian, används i stor utsträckning av många länder som ett lugnande medel, antikonvulsivt medel, för hypnotiska effekter och anxiolytisk aktivitet (Ghaderi och Jafari, 2014). Valereniksyra och valepotriater har rapporterats som aktiva ingredienser i farmaceutiska preparat och kommersiella råextrakt av valerian har registrerat användning i många länder (Bos et al., 2002). Valepotriater som består av triestrar av polyhydroxycyclopenta-(c)-pyraner med karboxylsyrorna: ättiksyra, valeransyra, isovaleransyra, α-isovaleroxy-isovaleransyra, β-metylvaleransyra, β-acetoxy-isovaleransyra, β-hydroxyisovaleransyra och β-acetoxy-β-metylvaleransyra, används som sedativa medel. Valepotriater är instabila, termolabila och sönderfaller snabbt under sura eller alkaliska förhållanden i vatten samt i alkoholiska lösningar (Bos et al., 2002). Valepotriater är användbara för att förbättra djurens och människans tillstånd vid bensodiazepinavvänjning (Poyares et al, 2002).
Och även om det finns en mängd olika kemiska beståndsdelar rapporteras verkningsmekanismen som interaktion mellan valerian och GABA-systemet i hjärnan genom hämning av GABA-transaminas, interaktion med GABA-receptorn/benzodiazepin och störning av upptag och intag rekrytering av GABA i synaptosomerna (Sichardt et al., 2007). Olika modeller har använts för att undersöka växters antidepressiva effekter. Farmakodynamiska modeller inkluderar in vitro, in vivo och kliniska modeller har använts för att bedöma effekterna (tabell 1). En majoritet av de utvalda växtarter som granskades studerades på in vivo-nivå, några få studerade in vitro och endast kava hade genomgått kliniska prövningar. I samtliga fall måste mer forskning utföras för att fastställa de aktiva substanserna, den mest effektiva dosen och för att avgöra om detta varierar mellan olika typer av depressioner.

TABELL 1. Information om farmakologiska studier av granskade växter.
Indolalkaloider
Indolalkaloider har en bicyklisk struktur som består av en sexdelad bensenring som är fusionerad med en femdelad kväveinnehållande pyrrolring. Denna pyrrolring med kväveatom ger upphov till indolalkaloidernas grundläggande egenskaper som gör dem särskilt farmakologiskt aktiva (El-Sayed och Verpoorte, 2007). Indolalkaloider är allmänt spridda i växter som tillhör familjerna Apocynaceae, Loganiaceae, Rubiaceae och Nyssaceae. Viktiga indolalkaloider som har isolerats från växter är bland annat det blodtryckssänkande läkemedlet reserpin från Rauvolfia serpentina (Sagi et al., 2016) och de kraftfulla antitumörläkemedlen vinblastin och vincristin från Catharanthus roseus (El-Sayed och Verpoorte, 2007). Studier om indolalkaloiders effektivitet vid behandling av depression är inte nya och har utförts sedan 1952, men för närvarande har det vetenskapliga samfundet ägnat mycket liten uppmärksamhet åt fördelarna med den terapeutiska användbarheten av växter utrustade med antidepressiva egenskaper.
Indolalkaloider förknippas ofta med funktionen av G-proteinreceptorer, särskilt för neuronal signalöverföring genom receptorer för serotonin (5-HT/hydroxytryptamin). Bortsett från vätedonatorn via fritt N-H bidrar närvaron av π-elektrontäthet till den högsta ockuperade molekylära orbitalenergin (HOMO) hos det plana indolskelettet. Detta möjliggör interaktion med nukleobaser, särskilt protonerade atomer samt målproteiner (de Sa et al., 2009). Den kemiska strukturen hos neurotransmittorn serotonin bygger på en elektronrik aromatisk indolring. Närvaron av kväveatomen i indolringen är till för att upprätthålla det aromatiska systemet och gör bindande N-H surt snarare än kvävebaserat. Indolringen kan bilda vätebindningar genom N-H-delen och π-π-stapling eller kation-π-interaktioner, via den aromatiska delen (Shimazaki et al., 2009). Indolringarnas hydrofobicitet är nästan densamma som fenylunderenheten och mindre hydrofobisk än den klassiska isosteriska bensothiofen- och bensofuranringen. N-H-indolgruppen spelar en avgörande roll i interaktionen med målbioreceptorn medan syntetiserade bensotiophen- och bensofuranderivat visar måttlig till begränsad affinitet för målbioreceptorn (de Sa et al., 2009). Reserpin är ett exempel på indolalkaloider som isolerats under de senaste 60 åren och som har en lugnande verkan på CNS. För övrigt är två kemikalier, nämligen tryptamin och serotonin som finns i hjärnan, också indolalkaloidderivat.
För närvarande är det fortfarande oklart vilka aktiva beståndsdelar från växtextrakt som är ansvariga för den antidepressiva effekten. Därför försöker vi identifiera några viktiga kemiska strukturer som isolerats från växtextrakt som uppvisar antidepressiva aktiviteter och fastställa den likhet i skelettmönstret som kan bidra till den antidepressiva aktiviteten. Tidiga försök har gjorts för att identifiera strukturella likheter mellan serotonin och indolalkaloider. Den tydligaste likheten består av sexledade heterocykliska ringar som är fusionerade med femledade ringar. Skillnaden är närvaron av en kväveatom eller fördelningen av π-elektroner (figur 1). Genom en struktur-aktivitetsrelationsstudie rapporterade Nichols (2012) att variationen i aktivitet hos olika typer av molekyler tyder på att receptorn är mycket känslig för tryptaminets karaktär. Andra kemiska föreningar som framgångsrikt isolerats från antidepressiva växter nämns i denna översiktsartikel eftersom de kanske är specifika agonister med särskilda substitutionsmönster som kan selektivt aktivera en undergrupp av effektorer. Detta fenomen är numera känt som funktionell selektivitet.
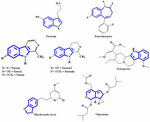
FIGUR 1. Kemiska strukturer för serotonin, bensodiazepin och isolerade föreningar från antidepressiva växter. Likhet i skelettmönstret, som består av sexledade heterocykliska ringar, fäst med femledade ringar.
Serotonin, används i stor utsträckning i hjärnans funktion och kognition som endogen receptoragonist (Fink och Göthert, 2007). Serotonin utövar sina funktioner genom sju familjer av receptorer (5-HT1-5-HT7) som tillhör den G-proteinkopplade receptorfamiljen. Ett antal föreningar med indolmolekyl har beskrivits ha affinitet för olika serotoninreceptorer (Kochanowska-Karamyan och Hamann, 2010). Den strukturella likheten mellan indolalkaloider (exogena agonister) och endogena neurotransmittorer som serotonin har fått forskare att förutsäga den potentiella neurologiska aktiviteten hos dessa molekyler. En schematisk bild av processer i samband med neurotransmission av exogena agonister beskrivs i figur 2.
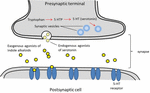
FIGUR 2. Schematisk bild av de processer som är förknippade med neurotransmission. Exogena agonister av indolalkaloider från växter som delar strukturella likheter med serotonin som gör att de kan binda in i serotoninreceptorer (5-HT-receptorer).
Indolringen är också känd som bioisosterer och har liknande kemiska och fysiska som biologiska molekyler. Denna likhet används vid utvecklingen av prototypläkemedlet som syftar till att förbättra den farmakologiska aktiviteten och optimera den farmakokinetiska profilen. I en annan studie av farmakologisk bedömning av bensofuraner och tiopyrrol ledde till bioisosteriska molekyler som har dimetyltryptaminliknande aktivitet. Tidigt arbete med bensotiophener och 3-indenalkylaminer visade att för föreningar som saknar ringsubstituenter var förmågan att verka som agonister i råttans fundus ungefär densamma som för tryptaminer. Resultaten visade att indol-NH inte var nödvändigt för att aktivera 5-HT2-receptorn i råttans fundus (Nichols, 2012). En serie 2-arylindol NK1-receptorantagonister och deras derivat är bra ligander men har låg oral biotillgänglighet hos råttor. För att öka lösligheten och absorptionen infördes det basiska kvävet, vilket ledde till den analoga azaindolen och besläktade föreningar som uppvisar samma NK1-bindningsaffinitet som serien av 2-arylindol-NK1-receptorantagonister (Cooper et al., 2001). Molekylär dockning av två fenylindolbaserade ligander med serotonin 5-HT6- och melanocortin-4-receptorer tyder på att den privilegierade ställningen kan anpassas beroende på den naturkonserverade subpocket och den icke-konserverade bindningsfickan. Interaktioner mellan icke-konserverade delar av bindningsfickan är ansvariga för viktiga skillnader i det molekylära erkännandet av motsvarande målreceptor (Bondensgaard et al, 2004).
Enligt de Sa et al. (2009) är vanliga indolalkaloider som finns i naturliga källor tryptofanaminosyror i människans näring och upptäckten av växthormoner som har terapeutiska effekter som t.ex. antiinflammatoriska, en fosfodiesterashämmare, 5-HT-receptoragonister och -antagonister, cannabinoidreceptoragonister och HMG-CoA-reduktashämmare. Indolställningen har bindningsfickor och har en gemensam komplementär bindningsdomän till målreceptorn, som tillhör en klass av GPCR:er (G-proteinviktiga membranreceptorer som är kopplade). De flesta läkemedel på marknaden innehåller indolunderstrukturen. Dessa inkluderar indometacin, ergotamin, frovatriptan, ondansetron och tadalafil.
Slutsats
Denna genomgång visade att majoriteten av de växtbaserade botemedel som anges för behandling av psykiatriska besvär var råa eller halvpurifierade. Resultaten för in vivo och in vitro varierar och var inte reproducerbara eftersom växternas innehåll av sekundära metaboliter i olika biogeografiska regioner korrelerar med tillgången på näringsämnen, klimat och ekologiska förhållanden. Dessutom kan växternas bioaktivitet komma från en enskild förening eller en blandning av föreningar. Författarna föreslår att ansträngningarna för att få fram aktiva principer, identifiering av fytokemikalier och metabolomikstudier bör genomföras med inspektioner in vitro och in vivo för en bättre karakterisering av växtbaserade läkemedel. I de flesta fall inspirerades syntesen av indolalkaloider av de naturligt förekommande molekylerna och deras likhet med serotonin.
Indolalkaloiderna från växtkällor är ganska komplexa jämfört med syntetiska. Betydelsen av syntetiska indolalkaloider är redan etablerad eftersom strukturen finns tillgänglig i olika ligandreceptorer, enzymhämmare och modulatorer bioreceptorer. Vissa av de naturligt förekommande indolalkaloiderna kan inte syntetiseras med hjälp av de metoder som för närvarande är kända. Dessutom har de flesta uppgifter om indolalkaloiders effektivitet rapporterats från syntetiska indolalkaloider. Därför är potentialen hos många naturligt förekommande indolalkaloider som nya läkemedel för olika psykiatriska sjukdomar fortfarande outnyttjad. Historiskt sett har växtbaserade föreningar varit källan till flera av de mest framgångsrika läkemedelsspåren eller läkemedel som används inom medicinen. Detta tyder på att mer kan ligga i beredskap att upptäckas.
Sammanfattningsvis har flera indolalkaloider använts som antidepressiva medel eller utgör ledande strukturer för dess utveckling. Baserat på våra resultat innehåller växter en reservoar av indolalkaloider som är värdefulla utgångspunkter för utveckling av framtida antidepressiva medel.
Författarbidrag
HHH: Förberedelse av manuskript. MY: Redigera det engelska språket och föreslå viss viktig information för att förbättra manuskriptet. AR: Bidra till förståelsen av schemat för processer i samband med neurotransmission.
Finansiering
Stöd för detta arbete tillhandahölls av Universiti Malaysia Pahang via forskningsanslag UMP RDU170302 till HH.
Intressekonfliktförklaring
Författarna förklarar att forskningen utfördes i avsaknad av kommersiella eller finansiella relationer som skulle kunna tolkas som en potentiell intressekonflikt.
Bilia, A. R., Gallori, S., and Vincieri, F. F. (2002). Kava-kava och ångest: växande kunskap om effekt och säkerhet. Life Sci. 70, 2581-2597. doi: 10.1016/S0024-3205(02)01555-2
PubMed Abstract | CrossRef Full Text | Google Scholar
Binfaré, R. W., Rosa, A. O., Lobato, K. R., Santos, A. R., and Rodrigues, A. L. S. (2009). Administrering av askorbinsyra ger en antidepressiv liknande effekt: bevis för inblandning av monoaminerga neurotransmissioner. Prog. Neuropsychopharmacol. Biol. Psychiatry 33, 530-540. doi: 10.1016/j.pnpbp.2009.02.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Bondensgaard, K., Ankersen, M., Thøgersen, H., Hansen, B. S., Wulff, B. S. och Bywater, R. P. (2004). G-proteinkopplade receptorers erkännande av privilegierade strukturer. J. Med. Chem. 47, 888-899. doi: 10.1021/jm0309452
PubMed Abstract | CrossRef Full Text | Google Scholar
Bos, R., Woerdenbag, H. J. och Pras, N. (2002). Bestämning av valepotriater. J. Chromatogr. A 967, 131-146. doi: 10.1016/S0021-9673(02)00036-5
CrossRef Full Text | Google Scholar
Calixto, J. B., Beirith, A., Ferreira, J., Santos, A. R. och Yunes, R. A. (2000). Naturligt förekommande antinociceptiva ämnen från växter. Phytother. Res. 14, 401-418. doi: 10.1002/1099-1573(200009)14:6<401::AID-PTR762>3.0.CO;2-H
PubMed Abstract | CrossRef Full Text | Google Scholar
Carlini, E. (2003). Växter och det centrala nervsystemet. Pharmacol. Biochem. Behav. 75, 501-512. doi: 10.1016/S0091-3057(03)00112-6
CrossRef Full Text | Google Scholar
Cooper, L. C., Chicchi, G. G., Dinnell, K., Elliott, J. M., Hollingworth, G. J., Kurtz, M. M., et al. (2001). 2-Arylindol NK 1-receptorantagonister: optimering av indolsubstitutionen. Bioorg. Med. Chem. Lett. 11, 1233-1236. doi: 10.1016/S0960-894X(01)00182-2
CrossRef Full Text | Google Scholar
de Sa, A., Fernando, R., Barreiro, E. J., Fraga, M. och Alberto, C. (2009). Från naturen till läkemedelsupptäckt: indolställningen som en ”privilegierad struktur”. Mini Rev. Med. Chem. 9, 782-793. doi: 10.2174/138955709788452649
CrossRef Full Text | Google Scholar
El-Sayed, M., and Verpoorte, R. (2007). Catharanthus terpenoida indolalkaloider: biosyntes och reglering. Phytochem. Rev. 6, 277-305. doi: 10.1007/s11101-006-9047-8
CrossRef Full Text | Google Scholar
Fajemiroye, J. O., Silva, D. M., Oliveira, D. R. och Costa, E. A. (2016). Behandling av ångest och depression: medicinalväxter i efterhand. Fundam. Clin. Pharmacol. 30, 198-215. doi: 10.1111/fcp.12186
PubMed Abstract | CrossRef Full Text | Google Scholar
Fiebich, B. L., Knörle, R., Appel, K., Kammler, T. och Weiss, G. (2011). Farmakologiska studier i en växtbaserad läkemedelskombination av johannesört (Hypericum perforatum) och passionsblomma (Passiflora incarnata): in vitro och in vivo bevis för synergi mellan Hypericum och Passiflora i antidepressiva farmakologiska modeller. Fitoterapia 82, 474-480. doi: 10.1016/j.fitote.2010.12.006
PubMed Abstract | CrossRef Full Text | Google Scholar
Fink, K. B., and Göthert, M. (2007). 5-HT-receptorreglering av neurotransmittorfrisättning. Pharmacol. Rev. 59, 360-417. doi: 10.1124/pr.59.07103
CrossRef Full Text | Google Scholar
Ghaderi, N. och Jafari, M. (2014). Effektiv växtförnyelse, genetisk trohet och ackumulering på hög nivå av två farmaceutiska föreningar i regenererade plantor av Valeriana officinalis L. S. Afr. J. Bot. 92, 19-27. doi: 10.1016/j.sajb.2014.01.010
CrossRef Full Text | Google Scholar
Grunze, H., Langosch, J., Schirrmacher, K., Bingmann, D., Von Wegerer, J. och Walden, J. (2001). Kava-pyroner utövar effekter på neuronal överföring och transmembranösa katjonströmmar som liknar etablerade stämningsstabiliserande medel – en översikt. Prog. Neuropsychopharmacol. Biol. Psychiatry 25, 1555-1570.
Google Scholar
Guan, L.-P. och Liu, B.-Y. (2016). Antidepressiva liknande effekter och mekanismer hos flavonoider och relaterade analoger. Eur. J. Med. Chem. 121, 47-57. doi: 10.1016/j.ejmech.2016.05.026
PubMed Abstract | CrossRef Full Text | Google Scholar
Hattesohl, M., Feistel, B., Sievers, H., Lehnfeld, R., Hegger, M. och Winterhoff, H. (2008). Extrakt av Valeriana officinalis L. sl visar anxiolytiska och antidepressiva effekter men varken sedativa eller myorelaxerande egenskaper. Phytomedicine 15, 2-15. doi: 10.1016/j.phymed.2007.11.027
PubMed Abstract | CrossRef Full Text | Google Scholar
Houghton, P. J., and Seth, P. (2003). Växter och det centrala nervsystemet. Pharmacol. Biochem. Behav. 75, 497-499. doi: 10.1016/S0091-3057(03)00161-8
CrossRef Full Text | Google Scholar
Idayu, N. F., Hidayat, M. T., Moklas, M., Sharida, F., Raudzah, A. N., Shamima, A., et al. (2011). Antidepressiv liknande effekt av mitragynin isolerat från Mitragyna speciosa Korth i musmodellen för depression. Phytomedicine 18, 402-407. doi: 10.1016/j.phymed.2010.08.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Jawna-Zboiñska, K., Blecharz-Klin, K., Joniec-Maciejak, I., Wawer, A., Pyrzanowska, J., Piechal, A., et al. (2016). Passiflora incarnata L. Förbättrar rumsligt minne, minskar stress och påverkar neurotransmission hos råttor. Phytother. Res. 30, 781-789. doi: 10.1002/ptr.5578
PubMed Abstract | CrossRef Full Text | Google Scholar
Kochanowska-Karamyan, A. J., and Hamann, M. T. (2010). Marina indolalkaloider: potentiella nya läkemedelsspår för kontroll av depression och ångest. Chem. Rev. 110, 4489-4497. doi: 10.1021/cr900211p
PubMed Abstract | CrossRef Full Text | Google Scholar
Kumarnsit, E., Vongvatcharanon, U., Keawpradub, N. och Intasaro, P. (2007). Fos-liknande immunoreaktivitet i råttans dorsala raphekärnor inducerad av alkaloidextrakt från Mitragyna speciosa. Neurosci. Lett. 416, 128-132. doi: 10.1016/j.neulet.2007.01.061
PubMed Abstract | CrossRef Full Text | Google Scholar
León, F., Habib, E., Adkins, J. E., Furr, E. B., McCurdy, C. R. och Cutler, S. J. (2009). Fytokemisk karakterisering av blad av Mitragyna speciosa som odlas i USA. Nat. Prod. Commun. 4, 907-910.
PubMed Abstract | Google Scholar
Malsch, U. och Kieser, M. (2001). Effekt av kava-kava vid behandling av icke-psykotisk ångest, efter förbehandling med bensodiazepiner. Psychopharmacology 157, 277-283. doi: 10.1007/s002130100792
PubMed Abstract | CrossRef Full Text
McCarthy, A., Wafford, K., Shanks, E., Ligocki, M., Edgar, D. M., and Dijk, D.-J. (2016). REM-sömnens homeostas i frånvaro av REM-sömn: Effekter av antidepressiva medel. Neuropharmacology 108, 415-425. doi: 10.1016/j.neuropharm.2016.04.047
PubMed Abstract | CrossRef Full Text | Google Scholar
Namola, V., Ratan, P., and Kothiyal, P. (2015). Depression och roll för marina biomaterial: en översikt. Eur. J. Biomed. Pharm. Sci. 2, 137-148.
Nichols, D. E. (2012). Struktur-aktivitetsförhållanden för serotonin 5-HT 2A-agonister. WIREs Membr. Transp. Signaling 1, 559-579. doi: 10.1002/wmts.42
CrossRef Full Text | Google Scholar
Organisation, W. H. (2017). Faktablad om depression 2016. Tillgänglig på: http://www.who.int/mediacentre/factsheets/fs369/en/
Google Scholar
Poyares, D. R., Guilleminault, C., Ohayon, M. M. och Tufik, S. (2002). Kan valerian förbättra sömnen hos sömnlösa efter bensodiazepinavvänjning? Prog. Neuropsychopharmacol. Biol. Psychiatry 26, 539-545.
PubMed Abstract | Google Scholar
Sagi, S., Avula, B., Wang, Y.-H. och Khan, I. A. (2016). Kvantifiering och karakterisering av alkaloider från rötter av Rauwolfia serpentina med hjälp av ultrahögpresterande vätskekromatografi-foto diode array-masspektrometri. Anal. Bioanal. Chem. 408, 177-190. doi: 10.1007/s00216-015-9093-4
PubMed Abstract | CrossRef Full Text | Google Scholar
Sarris, J., Kavanagh, D., Byrne, G., Bone, K., Adams, J. och Deed, G. (2009). The Kava Anxiety Depression Spectrum Study (KADSS): en randomiserad, placebokontrollerad crossover-studie med ett vattenhaltigt extrakt av Piper methysticum. Psychopharmacology 205, 399-407. doi: 10.1007/s00213-009-1549-9
PubMed Abstract | CrossRef Full Text | Google Scholar
Shimazaki, Y., Yajima, T., Takani, M. och Yamauchi, O. (2009). Metallkomplex som involverar indolringar: strukturer och effekter av metallindolinteraktioner. Coord. Chem. Rev. 253, 479-492. doi: 10.1016/j.ccr.2008.04.012
CrossRef Full Text | Google Scholar
Sichardt, K., Vissiennon, Z., Koetter, U., Brattström, A. och Nieber, K. (2007). Modulation av postsynaptiska potentialer i kortikala neuroner hos råttor av valerianextrakt som macererats med olika alkoholer: inblandning av adenosin A1- och GABAA-receptorer. Phytother. Res. 21, 932-937. doi: 10.1002/ptr.2197
PubMed Abstract | CrossRef Full Text | Google Scholar
Vicknasingam, B., Narayanan, S., Beng, G. T. och Mansor, S. M. (2010). Den informella användningen av ketum (Mitragyna speciosa) för opioidavvänjning i de norra delstaterna på halvön i Malaysia och konsekvenser för substitutionsterapi. Int. J. Drug Policy 21, 283-288. doi: 10.1016/j.drugpo.2009.12.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Vijeepallam, K., Pandy, V., Kunasegaran, T., Murugan, D. D. och Naidu, M. (2016). Mitragyna speciosa bladextrakt uppvisar antipsykotikaliknande effekt med potential att lindra positiva och negativa symtom på psykos hos möss. Front. Pharmacol. 7:464. doi: 10.3389/fphar.2016.00464
PubMed Abstract | CrossRef Full Text | Google Scholar
Yi, L.-T., Li, J.-M., Li, Y.-C., Pan, Y., Xu, Q. och Kong, L.-D. (2008). Antidepressiva-liknande beteendemässiga och neurokemiska effekter av den citrusassocierade kemikalien apigenin. Life Sci. 82, 741-751. doi: 10.1016/j.lfs.2008.01.007
PubMed Abstract | CrossRef Full Text | Google Scholar