Bakgrund
Artemisia annua är en kinesisk medicinalväxt (även känd som ”qing hao” eller ”söt malört”) med välbeprövad anti-malariaaktivitet (1). Artemisininbaserade kombinationsterapier (ACT) rekommenderas av Världshälsoorganisationen (WHO) för behandling av okomplicerad malaria i kombination med effektiva antimalariamedel (2). Kemoprofylax för resenärer beror på vilket resmål som är malariaendemiskt och omfattar en kombination av atovaquon/proguanil, klorokin, doxycyklin, mefloquin eller primaquin (3, 4). Fall av malariainfektion under kemoprofylax med artemisininderivat har beskrivits (5) och WHO rekommenderar inte användning av A. annua växtmaterial, i någon form, inklusive te, för behandling eller förebyggande av malaria (6).
Herbal and dietary supplements (HDS) används i allt större utsträckning över hela världen och HDS-inducerade leverskador blir ett växande problem (7). Trots den omfattande användningen av ACT i malariaendemiska områden är leverskador orsakade av artemisininderivat sällsynta (8, 9). Kumar rapporterade ett fall av en patient som utvecklade en kolestatisk leverskada 6 veckor efter att ha tagit ett växtbaserade kosttillskott som innehåller artemisinin oralt för allmänt hälsobevarande (10). Det finns några andra publikationer som rör Artemisia annua-inducerad leverskada (9, 11-14). En klinisk riktlinje för att utvärdera kausaliteten och ställa diagnosen av örtinducerad leverskada har nyligen föreslagits av Chinese Association of Chinese Medicine (15). Vi presenterar ett fall av akut kolestatisk hepatit på grund av intag av Artemisia-te som kemoprofylax hos en patient som återvände från Etiopien.
Fallbeskrivning
En 51-årig man presenterade sig på akutmottagningen vid universitetssjukhuset i Basel, Schweiz, med sjukdomskänsla, bukbesvär, flytande gula avföringsämnen, gulsot och koluri som varat i fyra dagar och med en viktnedgång på 6-8 kg under de senaste sex veckorna. Han hade återvänt från en fyra veckors resa till Etiopien tre veckor innan han sökte vård. Under vistelsen i Etiopien konsumerade han dagligen 1,25 g Artemisia annua-tepulver som kemoprofylax mot malaria. I cirka 90 % av fallen spädde han ut pulvret i kokande vatten, i de resterande 10 % intogs pulvret blandat med mat. Tillägget hade köpts via Internet. Patienten gav oss behållaren, som ursprungligen hade innehållit 50 g av ett mörkgrönt pulver (figur 1). Vid presentationen fanns 2 g i behållaren, vilket tyder på att han hade konsumerat totalt 48 g. Under sin vistelse i Etiopien hade han också konsumerat andra te-liknande preparat . Såvitt vi vet finns det ingen beskriven hepatotoxicitet i samband med dessa ämnen. Han förnekade att han tog några andra receptbelagda, receptfria eller växtbaserade läkemedel. Han hade ingen tidigare eller familjär historia av leversjukdom, alkohol- eller drogmissbruk eller riskfaktorer för virushepatit. Han rapporterade att hans fru, som följde med honom på resan till Etiopien, också hade druckit Artemesia annua-te som malariaprofylax. Hon förblev frisk under hela tiden.

Figur 1. Artemisia annua pulverte.
Bortsett från en tydlig gulsot var han i gott allmäntillstånd och hade oansenliga vitala tecken (afebril med normalt blodtryck, hjärtfrekvens och andningsfrekvens).
Laboratorietester visade: alaninaminotransferas (ALAT) 91 U/L (normalt, 9-59); aspartataminotransferas (ASAT) 42 U/L (normalt, 9-34); alkaliskt fosfatas (ALP) 151 U/L (normalt, 40-130); gamma-glutamyltransferas (GGT) 416 U/L (normalt, 12-68); totalt bilirubin 186.6 μmol/L (normal, 0-24) (konjugerat bilirubin 168,5 μmol/L) och internationell normaliserad kvot (INR) 0,9 (normal, 0,9-1,3). Gallsyranivån var förhöjd till al nivå 460,5 μmol/L (normal, 0-8,0). Differentialblodstatus och c-reaktivt protein var normala. Mild hyponatremi och hypokloremi förelåg, vilket överensstämde med patientens ökade vattenintag under de föregående dagarna. Serologiska tester för akut hepatit A, B, C och E, Epstein-Barr-virus och cytomegalovirusinfektion var negativa. Coeruloplasmin var normalt. Leverspecifika autoantikroppar (anti-nukleära antikroppar, anti-neutrofila antikroppar, anti-smooth muscle antikroppar, anti-mitokondriella antikroppar, anti-proteinas 3-antikroppar och anti-myeloperoxidas-antikroppar) var negativa och IgA, IgM och IgG låg inom normalområdet. Ultraljud i buken visade ett normalt leverparenkym, normala kärl och normala gallgångar. Leverelastografin var förhöjd (FibroScan, 12,7 kPa, normalintervall <5 kPa).
Patienten utvärderades också vid Swiss Tropical and Public Health Institute för olika potentiella underliggande infektionstillstånd. Antikroppar mot rickettsia spotted fever var positiva, men detta ansågs inte ha något samband med den kliniska presentationen och ingen antibiotikabehandling inleddes.
Den initiala leverbiopsin visade en portal hepatit med lymfocytär infiltration av gallgångarna och diffus intrakanalikulär och intracytoplasmatisk bilirubinostasis. Varken fibros eller parasitmaterial sågs (figurerna 2A, B). En nästa generations sekvenseringsanalys på DNA från perifera blodleukocyter för genetiska varianter i de gener som kodar för de 3 viktigaste hepatiska transportörerna för gallsyrahomeostas, nämligen BSEP, MDR3 och FIC1, hittade inga varianter som typiskt förknippas med ärftliga kolestatiska leversjukdomar.
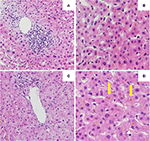
Figur 2. Histologi av den första (A,B) och andra (C,D) leverbiopsin. (A) Lågstyrkekamera av leverbiopsi som visar ett portal lymfocytärt infiltrat . (B) Leverparenkym med intracellulär bilirubinostas (HE, 20x). (C) Låg effektbild av leverbiopsi utan signifikant portalinflammation (HE, 10x). (D) Leverparenkym med betydande intracellulär och extracellulär (pil) bilirubinostas (HE, 20x).
Den toxikologiska analysen av Artemisia-teet med hjälp av vätskekromatografi-masspektrometri och gaskromatografi-masspektrometri avslöjade följande beståndsdelar: arteannuin b, deoxyartemisin, kamfer och scopoletin.
Behandling med prednison 20 mg två gånger dagligen och ursodeoxycholsyra 500 mg två gånger dagligen inleddes. På grund av ihållande gulsot samt ökande bilirubin under 4 veckor trots behandling utfördes en andra leverbiopsi. Den andra biopsin visade en allvarlig intracytoplasmatisk såväl som intracanalikulär bilirubinostasis, med endast minimal inflammation jämfört med den första biopsin (figurerna 2C, D). Kortikosteroidbehandlingen avbröts, ursodeoxikolsyra fortsatte tills upplösning av gulsot och normalisering av bilirubin (15,3 μmol/l) (figur 3) och relevant minskning av gallsyror (19,5 μmol/l) som inträffade tre månader efter sjukdomsdebuten.
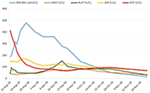
Figur 3. Förlopp för bilirubin och leverenzymer över tid.
Fallet rapporterades till läkemedelsövervakningsenheten vid den schweiziska nationella myndigheten för terapeutiska produkter (Swissmedic). Skriftligt informerat samtycke erhölls från deltagaren för publicering av denna fallrapport.
Diskussion
Artemisininderivat är en hörnsten för behandling men inte kemoprevention av malaria (2). Trots deras omfattande användning har leverskador orsakade av artemisininderivat sällan beskrivits (8, 10). Såvitt vi vet är detta den första fallrapporten om en akut kolestatisk hepatit till följd av intag av Artemisia annua-te.
Herbal and dietary supplements -induced liver injury is a topic of growing interest since HDS are used increasingly worldwide (7). Intaget av HDS betraktas ofta som ofarligt, men ett ökande antal biverkningar som uppträder i samband med användningen har rapporterats (16). Eftersom koncentrationen och sammansättningen av HDS ofta inte anges på produktetiketterna är kvaliteten och kvantiteten av produktens beståndsdelar dessutom okända. I vårt fall baserades diagnosen HDS-inducerad leverskada till följd av intag av Artemisia annua-te på det starka tidsmässiga sambandet mellan exponering och utveckling av biverkningen och avsaknaden av andra möjliga etiologier. Vi beräknade kausalitetsbedömningen enligt RUCAM (Roussel Uclaf Causality Assessment Method) (17) och fick en poäng på 6 som motsvarade en ”sannolik” kausalitet för det anklagade läkemedlet. De olika punkterna poängsattes enligt följande: tid till insjuknande (+2), förlopp (+1), riskfaktorer (+1), samtidiga läkemedel (-1), uteslutande av andra orsaker till leverskada (+2), tidigare information om läkemedlets hepatotoxicitet (+1), svar på återadministrering (0). Det fanns inga andra identifierbara etiologier till leversjukdom.
Det fall som tidigare beskrivits av Kumar uppvisade ett hepatocellulärt mönster av leverskada, följt av en långvarig kolestatisk fas (10). Vår patient presenterade ett övervägande kolestatiskt mönster av leverskada 5 veckor efter det första intaget av Artemisia annua-te. Vi antar att den naturliga historiken liknade Kumars fall, men att vår patient presenterade sig i ett senare skede under utvecklingen av leverskadan. I den toxikologiska analysen av det intagna örtteet identifierade vi dessutom scopoletin och kamfer, som naturligt förekommer i Artemisia annua (18, 19) och som kan ha bidragit till uppkomsten av den kolestatiska leverskadan.
Mekanismen för artemisininderivatinducerad leverskada är fortfarande oklar. De kemiska komponenterna i Artemisiae spp omfattar flyktiga oljor, flavonoider, tanniner, triterpener och polysackarider. Flyktiga oljor från Artemisiae spp har stark farmakologisk aktivitet och toxicitet, och en nyligen genomförd bioinformatisk metod identifierade olika vägar som kan vara involverade i utvecklingen av leverskador (20). Predisposition för läkemedelsinducerad kolestatisk leverskada har förknippats med polymorfismer för gallsaltsexportpumpar (21, 22). Vi sökte därför efter varianter i gallsyretransportörer genom nästa generations sekvensering. Vi upptäckte ingen deletion, duplikation eller patologisk variant i gensekvenserna ABCB11, ATP8B1 och ABCB4 (kodande och flankerande regioner) som kodar för BSEP, FIC1 respektive MDR3 (figur 4). Ett antal gemensamma sekvensvarianter identifierades dock. Vår patient hade homozygot en variant av ABCB11-genen . Det har diskuterats om denna polymorfism är förknippad med godartad återkommande och/eller progressiv familjär intrahepatisk kolestas och intrahepatisk kolestas i samband med graviditet (23, 24). Dessutom upptäcktes en annan vanlig variant i ABCB11-genen i heterozygot tillstånd . Denna variant har förknippats med minskat proteinuttryck (25) och med primär gallcirrhos (26, 27). Båda genvarianterna är dock alldeles för vanliga i den allmänna befolkningen för att vara kausala för kolestatiska leversjukdomar (28). Systematisk sekvensering av transkriptomet i sådana fall kan identifiera varianter i andra regioner av gensekvenserna eller i andra gener som kodar för andra hepatiska transportörer eller proteiner som är involverade i gallbildningen, till exempel ABCC2, ABCC3, ABCC4 respektive tight junction protein 2 (TJP2) (21).
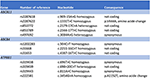
Figur 4. Molekylärgenetisk analys av generna ABCB11, ABCB4 och ATP8B1.
Slutsatsen är att vi beskriver ett fall av en allvarlig HDS-inducerad kolestatisk leverskada som var förenlig med intag av Artemisia annua-te. Ansträngningar bör göras för att motverka användningen av artemisininderivat för att förebygga malaria, vilket är ineffektivt enligt WHO:s rekommendationer och dessutom kan orsaka skada. Dessutom visar fallet vår ännu otillräckliga förståelse av patofysiologin och känsligheten för HDS-inducerad leverskada.
Data Availability Statement
Alla dataset för denna studie ingår i manuskriptet/tilläggsfilerna.
Ethics Statement
Ett etiskt omdöme och godkännande krävdes inte för rapporteringen av ett enskilt kliniskt fall här i enlighet med den lokala lagstiftningen och institutionella krav. Patienten/deltagaren gav sitt skriftliga informerade samtycke till att delta.
Författarbidrag
FR-R skrev det första utkastet till manuskriptet. SH, CB, AL-T, MZ och AJ skrev delar av manuskriptet. FR-R, SH, SR, MZ, KR, JB, AJ, MH, AL-T, LT och CB bidrog till den kliniska hanteringen av patienten, revidering av manuskriptet, läste och godkände den inlämnade versionen.
Intressekonflikter
Författarna förklarar att forskningen utfördes i avsaknad av kommersiella eller ekonomiska relationer som skulle kunna uppfattas som en potentiell intressekonflikt.
1. Klayman DL. Qinghaosu (artemisinin): ett antimalarialäkemedel från Kina. Science. (1985) 228:1049-55. doi: 10.1126/science.3887571
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Världshälsoorganisationen. WHO:s riktlinjer för behandling av malaria, 2nd ed. (2010). Tillgänglig online på: http://www.who.int/malaria/publications/atoz/9789241547925/en/index.html (tillgänglig den 23 november 2018).
Google Scholar
3. SafeTravel.ch. Reismedizinische Beratung. Malariavorbeugung (Chemoprophylaxe) (2016). Tillgänglig online på: http://www.safetravel.ch/safetravel2/servlet/ch.ofac.wv.wv204j.pages.Wv204ConseilsSanteListeCtrl?action=afficheDetail&elementCourant=1 (tillgänglig den 23 november 2018).
Google Scholar
4. Centers for Disease Control and Prevention. Att välja ett läkemedel för att förebygga malaria (2018). Tillgänglig online på: https://www.cdc.gov/malaria/travelers/drugs.html
Google Scholar
5. Shahinas D, Lau R, Khairnar K, Hancock D, Pillai DR. Missbruk av artesunat och plasmodium falciparum-malaria hos resenärer som återvänder från Afrika. Emerg Infect Dis. (2010) 16:1608-10. doi: 10.3201/eid1610.100427
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Världshälsoorganisationen. WHO, ställningstagande. Effectiveness of Non-Pharmaceutical Forms of Artemisia annua L. Against Malaria. Genève: Världshälsoorganisationen (2012).
Google Scholar
7. Navarro VJ, Khan I, Björnsson E, Seeff LB, Serrano J, Hoofnagle JH. Leverskador från ört- och kosttillskott. Hepatologi. (2017) 65:363-73. doi: 10.1002/hep.28813
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Guevart E, Aguemon A. Två fall av fulminant hepatit under en kurativ behandling med en artesunat-amodiaquinkombination. Med Mal Infect. (2009) 39:57-60. doi: 10.1016/j.medmal.2008.09.024
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Centers for Disease Control and Prevention (CDC). Hepatit i samband med ett växtbaserade kosttillskott som innehåller artemisinin – Washington, 2008. Morb Mortal Wkly Rep. (2009) 58:854-6.
Google Scholar
10. Kumar S. Kolestatisk leverskada sekundär till artemisinin. Hepatologi. (2015) 62:973-4. doi: 10.1002/hep.27900
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Stebbings S, Beattie E, McNamara D, Hunt S. En randomiserad, placebokontrollerad klinisk pilotstudie för att undersöka effekten och säkerheten hos ett extrakt av Artemisia annua administrerat under 12 veckor, för att hantera smärta, stelhet och funktionell begränsning i samband med artros i höft och knä. Clin Rheumatol. (2016) 35:1829-36. doi: 10.1007/s10067-015-3110-z
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Medsafe. Arthrem – Potentiell risk för leverskador – Uttalande enligt avsnitt 98 i läkemedelslagen från 1981 (2018). Tillgänglig online på: http://www.medsafe.govt.nz/safety/EWS/2018/Arthrem.asp
Google Scholar
13. National Institutes of Health, LiverTox, Clinical and Research Information on Drug-Induced Liver Injury. Artemisininderivat. (2019). Tillgänglig online på: https://livertox.nih.gov/ArtemisininDerivatives.htm
Google Scholar
14. Savage RL, Tatley MV, Barnes J. Hepatotoxicitet med ett naturligt kosttillskott, Artemisia annua L. Extract in Grapeseed Oil. New Zealand Pharmacovigilance Centre Reports. Drug Safety (2018). I: 18th ISoP Annual Meeting ”Pharmacovigilance without borders”. Geneva (accessed November 11-14, 2018).
Google Scholar
15. Wang JB, Zhu Y, Bai ZF, Wang FS, Li XH, Xiao XH, et al. Guidelines for the Diagnosis and Management of Herb-Induced Liver Injury. Chin J Integr Med. (2018) 24:696-706. doi: 10.1007/s11655-018-3000-8
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Clarke TC, Black LI, Stussman BJ, Barnes PM, Nahin RL. Trender i användningen av komplementära hälsovårdsmetoder bland vuxna: USA, 2002-2012. Natl Health Stat Rep. (2015) 79:1-16.
Google Scholar
17. Danan G, Teschke R. RUCAM in drug and herb induced liver injury: the update. Int J Mol Sci. (2015) 17:E14. doi: 10.3390/ijms17010014
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Zhang X, Zhao Y, Guo L, Qiu Z, Huang L, Qu X. Skillnader i kemiska beståndsdelar i Artemisia annua L från olika geografiska områden i Kina. PLoS ONE. (2017) 12:e0183047. doi: 10.1371/journal.pone.0183047
PubMed Abstract | CrossRef Full Text | Google Scholar
19. Ogwang Engeu P, Omujal F, Agwaya M, Kyakulaga H, Obua C. Variationer i antimalariakomponenter i Artemisia annua Linn från tre regioner i Uganda. Afr Health Sci. (2015) 15:828-34. doi: 10.4314/ahs.v15i3.17
CrossRef Full Text | Google Scholar
20. Liu H, Zhan S, Zhang Y, Ma Y, Chen L, Chen L, et al. Molekylär nätverksbaserad analys av mekanismen för leverskada orsakad av flyktiga oljor från Artemisiae argyi folium. BMC Complement Altern Med. (2017) 17:491. doi: 10.1186/s12906-017-1997-4
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Morgan RE, Trauner M, van Staden CJ, Lee PH, Ramachandran B, Eschenberg M, et al. Interferens med gallsaltsexportpumpens funktion är en känslighetsfaktor för leverskador hos människor vid läkemedelsutveckling. Toxicol Sci. (2010) 118:485-500. doi: 10.1093/toxsci/kfq269
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Kubitz R, Dröge C, Stindt J, Weissenberger K, Häussinger D. The bile sal export pump (BSEP) in health and disease. Clin Res Hepatol Gastroenterol. (2012) 36:536-53. doi: 10.1016/j.clinre.2012.06.006
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Alissa FT, Jaffe R, Shneider BL. Uppdatering om progressiv familjär intrahepatisk kolestas. J Pediatr Gastroenterol Nutr. (2008) 46:241-52.21. doi: 10.1097/MPG.0b013e3181596060
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Dixon PH, Williamson C. The molecular genetics of intrahepatic cholestasis of pregnancy. Obstet Med. (2008) 1:65-71. doi: 10.1258/om.2008.080010
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Stieger B. Natrium-taurocholat-kotransportpolypeptidens (NTCP) och gallsaltsexportpumpens (BSEP) roll i fysiologin och patofysiologin vid gallbildning. Handb Exp Pharmacol. (2011) 201:205-59. doi: 10.1007/978-3-642-14541-4_5
CrossRef Full Text | Google Scholar
26. Pauli-Magnus C, Kerb R, Fattinger K, Lang T, Anwald B, Kullak-Ublick GA, et al. BSEP och MDR3 haplotypsstruktur hos friska kaukasier, primär biliär cirros och primär skleroserande kolangit. Hepatology. (2004) 39:779-91. doi: 10.1002/hep.20159
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Pan S, Li X, Jiang P, Jiang Y, Shuai L, He Y, et al. Variationer i generna ABCB4 och ABCB11 är associerade med primära intrahepatiska stenar. Mol Med Rep. (2015) 11:434-46. doi: 10.3892/mmr.2014.2645
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Dröge C, Bonus M, Baumann U, Klindt C, Lainka E, Kathemann S, et al. Sekvensering av FIC1, BSEP och MDR3 i en stor kohort av patienter med kolestas visade ett stort antal olika genetiska varianter. J Hepatol. (2017) 67:1253-64. doi: 10.1016/j.jhep.2017.07.004
PubMed Abstract | CrossRef Full Text | Google Scholar