INDLEDNING
Få lægemiddelgrupper er blevet undersøgt i så stor udstrækning som betablokkere (BB’er) hos patienter med forskellige kardiovaskulære tilstande i årenes løb. I de sidste 3 årtier har de revolutioneret det kardiologiske område, og omfattende dokumentation bekræfter deres effektivitet i de 4 mest almindelige grupper af kardiovaskulære sygdomme: hjertesvigt (HF), hypertension, arytmier og iskæmisk hjertesygdom. Samtidig finder man stadig nye virkningsmekanismer for BB’er, som bidrager til bedre at forklare årsagerne til deres klare fordele.1 Disse nye opdagelser udvider yderligere de potentielle, men endnu uidentificerede anvendelser af BB’er i kliniske sammenhænge.
Her præsenterer vi den eksisterende dokumentation for fordelene ved BB’er i forskellige kliniske sammenhænge, de virkningsmekanismer, der ligger til grund for disse fordele, og de nuværende anbefalinger.
BETA-BLOCKERE VED HJERTESVAGT
På grund af deres negative inotrope egenskaber blev BB’er længe betragtet som absolut kontraindiceret hos patienter med HF. Feltet gennemgik en begrebsmæssig revolution, da det blev overvejet, at BB’er i modsætning til den fremherskende visdom paradoksalt nok kunne være gavnlige. I det første årti af det 21. århundrede blev det påvist, at disse lægemidler havde meget positive virkninger hos patienter med HF. Siden da er de blevet en hjørnesten i behandlingen af HF hos patienter med systolisk dysfunktion (nedsat venstre ventrikulær ejektionsfraktion , ≤ 40 %; også kendt som reduceret ejektionsfraktion ). HF skal imidlertid forstås i hele sit spektrum, fra asymptomatiske patienter, der ikke desto mindre er i risiko for HF – stadium A i American College of Cardiology/American Heart Association (ACC/AHA)2 – til symptomatiske patienter med forskellige LVEF-intervaller og endda hospitalsindlagte patienter eller patienter med alvorlige HF-symptomer.
Hjertesvigt med reduceret ejektionsfraktion
Evidensen viser entydigt, at BB’er reducerer risikoen for død hos patienter med HFrEF. Deres anvendelse er bredt anerkendt i de seneste kliniske retningslinjer for klinisk praksis fra European Society of Cardiology (ESC).3Tabel 1 viser data fra de vigtigste randomiserede forsøg4-10 , der støtter anvendelsen af BB’er, samt deres evne til at reducere de vigtigste endepunkter. Selv om metoprolol, bisoprolol og carvedilol er forbundet med betydelige gavnlige virkninger, er sammenhængen ikke så konsistent for bucindolol og nebivololol. I SENIORS-forsøget (alder > 70 år, 64 % med rEF) var nebivolol forbundet med en lavere risiko for det sammensatte endepunkt død og kardiovaskulær hospitalsindlæggelse, men ikke for død alene eller de andre endepunkter.4 Bucindololol formåede ikke at reducere dødeligheden i BEST-undersøgelsen, selv om det reducerede hospitalsindlæggelser for HF.5 De 3 BB’er med den stærkeste evidens i denne population (metoprolol, bisoprolol og carvedilol) er forbundet med reduceret sygdomsprogression, som det fremgår af de lavere rater af direkte relateret død (pludselig og HF) og HF-indlæggelser i de forskellige forsøg.6-8
Design og resultater af de vigtigste kliniske forsøg med betablokkere ved hjertesvigt
| Studie (y, patienter) | Medicin, gennemsnit (mg/d) | NYHA | LVEF | Iskæmisk | Middel opfølgning, mo | NYHA klasse III/IV | >NNT1 liv1 y | Reduktion i risiko for død | Reduktion i risiko for hospitalsindlæggelse | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Total | CV | På grund af HF | Total | Total | Total | Til grund af HF | ||||||||||||
| CIBIS-II6 (1999, n=2647) | Bisoprolol 7.5 mg/d | III-IV | ≤35% | 50% | 15 | 100% | 23 | 34% | 29% | 44% | 26% | 20% | 36% | |||||
| MERIT-HF7 (1999, n=3991) | Metoprolol 159 mg/d | II-IV | ≤40% | 65% | 12 | 59% | 27 | 34% | 38% | 38% | 41% | 49% | 18% | 35% | ||||
| US carvedilol10 (1996, n=1094) | Carvedilol 45 mg/d | II-IV | ≤35% | 48% | 6 | 60% | 15 | 65% | 65% | 65% | 55% | 79% | 27% | – | ||||
| COPERNICUS8 (2002, n=2289) | Carvedilol 37 mg/d | III-IV | 25% | 67% | 10 | 100% | 15 | 35% | 35% | – | – | – | 20% | 33% | ||||
| COMET9 (2003, n=3029) | Carvedilol 42 mg/d vs metoprolol 85 mg/d | II-IV | 35% | 51% | 58 | 51% | – | 17% | 20% | 3%, NS | ||||||||
| BEST5 (2001, n=2708) | Bucindolol 152 mg/d | III-IV | ≤35% | 59% | 24 | 100% | – | 10%, NS | 14%, NS | 12%, NS | 15%, NS | 8%, NS | 22% | |||||
| SENIORS4 (2005, n=2128) | Nebivololol 7.7 mg/d | II-IV | * | 68% | 21 | 40% | – | – | 12%, NS | 16%, NS | – | – | 4%, NS | – | ||||
CV, kardiovaskulær; HF, hjertesvigt; LVEF, venstre ventrikulær ejektionsfraktion; NNT, antal der er nødvendigt at behandle; NS, ikke signifikant; NYHA, New York Heart Association.
Alle undersøgelser analyserede betablokkere vs. placebo, undtagen COMET (carvedilol vs. metoprololtartrat). Alle risikoreduktioner er signifikante, medmindre andet er angivet.
LVEF var ikke et inklusionskriterium, men 36 % af patienterne havde en LVEF> 35 %; de inkluderede patienter var ældre end 70 år.
Den COMET-undersøgelse, som er den eneste undersøgelse, der direkte sammenligner 2 BB’er – carvedilol vs. metoprololtartrat – fandt lavere dødelighed med carvedilol; brugen af korttidsvirkende metoprolol, i modsætning til den formulering, der blev anvendt i MERIT-HF-undersøgelsen7 , kan dog i nogen grad forklare disse forskelle9 . I en stor metaanalyse baseret primært på BB’er med dokumenteret overlevelsesfordel blev der ikke fundet nogen forskelle mellem de forskellige BB’er, som tilsammen reducerede 12-måneders mortaliteten med 31 % uden interaktioner mellem behandling og undergruppe.11Figur 1 viser den relative risikoreduktion og det antal patienter, der skal behandles efter 1 år for at reducere de forskellige hændelser, baseret på metaanalysens resultater.11
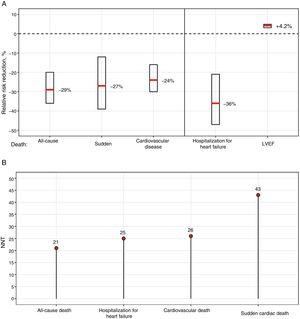
Nytte af betablokkere hos patienter med hjertesvigt og nedsat LVEF. A: Relativ risikoreduktion og 95 % konfidensinterval. B: NNT efter 1 år. LVEF, venstre ventrikulær ejektionsfraktion; NNT, number needed to treat.
I de seneste år har forskellige metaanalyser behandlet forholdet mellem fordelene ved BB’er og hjertefrekvensen hos patienter med rEF. Sammenhængen mellem en højere hjertefrekvens og en dårligere prognose er veletableret. Ikke desto mindre viste en subanalyse af HF-ACTION-undersøgelsen, at fordelen er større ved tilstedeværelse af høje BB-doser, uanset hjertefrekvens12 . På den anden side har andre nyere metaanalyser vist, at den hjertefrekvensreduktionsrelaterede fordel ved BB’er kun opnås hos patienter med sinusrytme eller i det mindste er lavere hos patienter med atrieflimmer (AF).13 En subanalyse af AF-CHF-undersøgelsen viste imidlertid, at BB’er også forbedrede mortalitetsraten hos patienter med AF og rEF.14
Et særligt problem er patienter med asymptomatisk rEF. Hos disse patienter forhindrer BB’er teoretisk set de negative ventrikulære remodelleringsprocesser, der fremmer udviklingen til symptomatisk HF. REVERT-undersøgelsen, den eneste undersøgelse, der randomiserede asymptomatiske patienter i New York Heart Association (NYHA) stadium I og med rEF (stadium B i ACC/AHA),1 viste, at metoprololsuccinat var forbundet med reducerede volumener og øget LVEF efter 1 år.15 CAPRICORN-undersøgelsen (postinfarkt-LVEF
40 %) identificerede mindre progression til symptomatiske stadier og forbedret remodellering og ventrikelfunktion.16 I en observationsundersøgelse reducerede brugen af BB episoder af symptomatisk HF med 60 %.17Hjertesvigt med midterste eller bevaret systolisk funktion
Prospektive kliniske forsøg er sjældne og har typisk indirekte endepunkter som ekkokardiografiske parametre eller små stikprøvestørrelser, der blot tillader en vurdering af effekten på kliniske endepunkter. En observationsundersøgelse, baseret på propensity score-justering med en stor population af indlagte patienter, og flere metaanalyser viser, at BB’er kan reducere dødeligheden hos patienter med en LVEF > 40 %.18 For nylig viste en delundersøgelse af TOPCAT-forsøget (LVEF> 45 %), at BB’er, især hos patienter uden tidligere infarkt, var forbundet med øgede negative kardiovaskulære hændelser.19 Efter anbefalingen i de seneste europæiske retningslinjer om at betragte patienter med LVEF i mellemområdet (40 %-49 %) som en særskilt undergruppe viste en individuel metaanalyse, der omfattede LVEF for hver enkelt patient i de centrale kliniske forsøg, imidlertid, at patienter i sinusrytme rent faktisk kunne drage fordel af BB-behandling med hensyn til dødelighed20 .
Svær akut eller dekompenseret hjertesvigt
For patienter, der indlægges med rEF, reducerer fortsættelse af BB’er under indlæggelsen risikoen for død med 40 %, mens iværksættelse af BB-behandling hos BB-naive patienter reducerer risikoen med næsten 60 %.21 I modsætning hertil fordobler tilbagetrækning af BB’er under indlæggelsen dødeligheden.22 COPERNICUS-undersøgelsen evaluerede patienter med svær HF (NYHA-klasse III-IV og LVEF
25 %), herunder indlagte eller dekompenserede patienter, der indtog intravenøse diuretika. Brugen af carvedilol reducerede den samlede risiko for død med 35 %.7 Desuden lettede iværksættelse af BB under indlæggelse på hospitalet adhærens til BB-behandling under opfølgningen.23 I en anden subanalyse af MERIT-HF-forsøget, der omfattede patienter med værre klinisk forværring (NYHA-klasse III-IV og LVEF 25 %), var fordelen ved metoprolol klar og endnu større.24BETA-BLOKKERER VED HYPERTENSION
Sammenlignet med placebo har BB’er ikke vist sig at reducere den samlede dødelighed eller den kardiovaskulære dødelighed hos patienter med ukompliceret essentiel hypertension.25-27 De kan dog reducere kardiovaskulære hændelser, primært slagtilfælde. Sammenlignet med diuretika reducerer BB’er ikke kardiovaskulære hændelser og kan endda være forbundet med en højere forekomst af slagtilfælde.28 Denne høje slagtilfælde synes at være forbundet med alder, hvilket øger risikoen for BB’er hos personer over 60 år.29 Sammenlignet med calciumantagonister eller angiotensin-konverterende enzymhæmmere/angiotensinreceptorblokkere er BB’er forbundet med en øget risiko for slagtilfælde.26,27 Resultaterne af brugen af BB’er som førstevalgsmedicin til behandling af hypertension i forhold til andre lægemiddelgrupper er vist i figur 2.
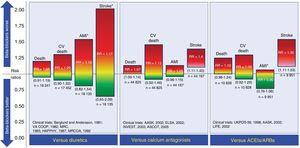
Sammenligning af betablokkere med andre lægemidler, der anvendes som førstelinjestrategier til behandling af essentiel hypertension. Risikokvotienterne er plottet sammen med deres 95 % konfidensintervaller (i parentes). ACEI’er, angiotensin-konverterende enzymhæmmere; AMI, akut myokardieinfarkt; ARB’er, angiotensin II-receptorblokkere; CV, kardiovaskulær; RR, risikokvotient. *Hændelser, hvis risikokvotient og tilsvarende konfidensinterval har en lav grad af sikkerhed i henhold til GRADE-arbejdsgruppens klassifikationer af evidensniveauet. Oplysningerne er baseret på metaanalysen af Wiysonge et al.27
Da BB’er er en heterogen gruppe af lægemidler, bør konklusioner, der er afledt af metaanalyser, generelt tages med forsigtighed. Tabel 2 viser resultaterne af de vigtigste kliniske forsøg, der har analyseret de forskellige BB’ers rolle i behandlingen af hypertension30 .-45
Væsentligste kliniske undersøgelser, der analyserer betablokkere i behandlingen af essentiel hypertension
| Studie | Population | Beta-blocker | Sammenligning | Resultat | |
|---|---|---|---|---|---|
| Berglund og Andersson30 | 47-54 y | Propranolol | Thiazid | Ingen forskel i dødelighed | |
| VA COOP31 | 21-65 y | Propranolol | Thiazid | Ingen forskel i dødelighed, AMI eller slagtilfælde | |
| MRC32 | 35-64 år | Propranolol | ThiazidPlacebo | Lejere risiko for slagtilfælde vs. placebo; ingen forskel i AMI eller dødelighedHøjere risiko for slagtilfælde vs thiazid | |
| Coope og Warrender33 | 60-79 år | Atenolol±thiazid | Placebo | Lækkerere risiko for slagtilfælde vs placebo; ingen forskel i AMI eller dødelighed | |
| HAPPHY34 | 40-65 år (kun mænd) | MetoprololAtenolol | Thiazid | Tendens til mindre slagtilfælde vs. diuretikaIngen forskel i mortalitet eller AMI | |
| MAPHY35 | 40-64 y (kun hvide mænd) | Metoprolol | Thiazid | Reduktion i samlet dødelighed, AMI og slagtilfælde | |
| STOP-Hypertension36 | 70-84 år | PindolololMetoprololAtenololol | Placebo | Reduktion i kardiovaskulær dødelighed, AMI, og slagtilfælde | |
| MRCOA37 | 65-74 y | AtenolololDiuretika | Placebo | Ingen forskel i kardiovaskulær død, slagtilfælde, eller AMI vs placebo (diuretikum vs placebo reducerede sådanne hændelser) | |
| UKPDS38 | Diabetiske patienter | Atenolol | Atenolol | Captopril | Ingen forskel i samlet dødelighed, AMI eller slagtilfælde |
| STOP-239 | 70-84 år | PindolololMetoprololAtenolol | Enalapril Lisinopril Felodipin Isradipin | Ingen forskel i dødelighed, AMI, eller slagtilfælde | |
| CAPPP40 | 20-66 år | MetoprololAtenololol | Captopril | Tendens til højere kardiovaskulær mortalitetIngen forskel i AMILejere risiko for slagtilfælde | |
| ELSA41 | Aterosklerose i halspulsåren | Atenolol | Lacidipin | Øget progression af aterosklerotisk plaque | |
| LIFE42 | 55-80 y | Atenolol | Losartan | Samme kardiovaskulær mortalitetSamme risiko for AMIMere slagtilfældeMere DM | |
| INVEST43 | ≥50 årIskæmisk hjertesygdom | Atenolol±thiazid | Verapamil±trandolapril | Ingen forskel i dødelighed, AMI eller slagtilfælde | |
| CONVINCE44 | ≥ 55 år med 1 CVRF | Atenolol | Verapamil | Ingen forskel i dødelighed, AMI, eller slagtilfælde | |
| ASCOT-BPLA45 | 40-79 årHøj kardiovaskulær risiko | Atenolol±thiazid | Amlodipin±perindopril | Tendens til højere risiko for AMIHøjere risiko for slagtilfældeHøjere kardiovaskulær mortalitetHøjere risiko for DM |
AMI, akut myokardieinfarkt; CVRF, kardiovaskulære risikofaktorer; DM, diabetes mellitus.
De nye europæiske retningslinjer for hypertension46 udelukker BB’er som førstevalg af lægemiddelbehandling til ukompliceret hypertension.
BETA-BLOCKERE OG KARDIÆR ARRHYTHMIAS
β1-receptorer udgør 80 % af de adrenerge receptorer i hjertet. Ved at blokere disse receptorer modvirker BB’er den proarytmiske virkning af sympatikusaktivitet på myokardiet.47 Den antiarytmiske virkning af BB’er er på den ene side resultatet af deres direkte hjerteelektrofysiologiske virkning, som formidles på forskellige måder: ved at reducere hjertefrekvensen, mindske den spontane aktivering af ektopiske pacemakere, bremse ledningen af elektriske impulser eller øge den refraktære periode i den atrioventrikulære knude. På den anden side påvirkes deres antiarytmiske egenskaber af andre mekanismer, der, selv om de ikke har direkte elektrofysiologisk hjerteaktivitet, bidrager til at forebygge hjertearytmier, via hæmning af sympatikusaktivitet, reduktion af myokardisk iskæmi, en virkning på baroreflexfunktionen og nedsat mekanisk stress. Disse virkninger adskiller BB’er fra andre antiarytmika, som udøver deres virkning via direkte modulering af kardiomyocytære ionkanaler. BB’er har begrænsede proarytmiske virkninger og har derfor en fremragende effekt- og sikkerhedsprofil.
Atrieflimren
BB’er er førstevalgsmedicin til kontrol af hjertefrekvensen i forbindelse med AF hos patienter uden kontraindikationer.48 Selv om behandling med hastighedskontrol spiller en grundlæggende rolle i behandlingen af AF, er sympatikusaktivitet forbundet med både initiering og vedligeholdelse af AF.49 Ikke desto mindre er BB’ernes rolle i rytmekontrol sekundær, selv om det er rigtigt, at metoprolol i en randomiseret undersøgelse i forhold til placebo reducerede AF-recidiv med 11 %.50 Desuden kan BB’er hos patienter med HF eller akut myokardieinfarkt (AMI) reducere forekomsten af AF.51
Ventrikulære arytmier
BB’er er særligt nyttige til kontrol af ventrikulære arytmier relateret til sympatisk aktivitet, såsom perioperative arytmier og dem, der er forbundet med stress, AMI og HF.52 De forebygger pludselig hjertedød ved at reducere maligne ventrikulære arytmier i forskellige sammenhænge, primært under akut iskæmiske, systoliske dysfunktioner og kanalopatitilstande. I forbindelse med AMI øger BB’er tærsklen for ventrikelfibrillering under akut iskæmi.53,54 I en mere stabil fase er de især nyttige til forebyggelse af arrelaterede ventrikulære arytmier efter en bekræftet AMI, som generelt viser sig som vedvarende monomorfe ventrikulære takykardi. Hos patienter med rEF er der påvist en absolut reduktion af pludselig hjertedød på ca. 2 % til 3 % (∼40 % relativ reduktion i forhold til placebo).55 Hos patienter med kanalopatier, især patienter med langt QT-syndrom og katekolaminerg ventrikulær takykardi, er BB’er det foretrukne lægemiddel. I denne sammenhæng viste en retrospektiv undersøgelse af 233 patienter med langt QT-syndrom og synkope i fortiden en markant reduktion i dødeligheden med BB’er i forhold til placebo.56 For patienter med katekolaminerg polymorfisk ventrikulær takykardi er BB’er det foretrukne lægemiddel, især nadolol.57 De kliniske situationer med dokumenteret fordel af BB’er til forebyggelse af pludselig hjertedød som følge af ventrikulære arytmier er vist i figur 3.
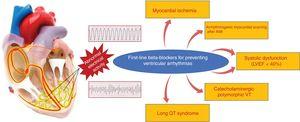
Kliniske situationer med dokumenterede fordele ved betablokkere til forebyggelse af pludselig død som følge af ventrikulære arytmier. AMI, akut myokardieinfarkt; LVEF, venstre ventrikulær ejektionsfraktion; VT, ventrikulær takykardi.
BETA-BLOKKERER VED ISKEMISK HJERTESYGDOM
BB’er har i flere årtier været anvendt til behandling af iskæmisk hjertesygdom i sammenhænge såsom under AMI (intravenøs administration), ved kronisk administration efter AMI eller hos patienter med koronarsygdom uden tidligere AMI. Flere undersøgelser i præperfusionstiden undersøgte den gavnlige virkning af BB’er i forbindelse med AMI og viste en klar reduktion af langtidsmortaliteten.58
Intravenøse betablokkere i den akutte fase af infarkt
Under forløbet af AMI opstår katekolaminmedieret sympatikusaktivitet som reaktion på smerte, angst og nedsat hjertemængde. Denne stigning i den sympatiske tone har negative konsekvenser, såsom et forhøjet myokardisk iltbehov, der fremskynder myokardisk nekrose, og en nedsat tærskel for ventrikelflimmer, der øger risikoen for pludselig hjertedød. Den øgede sympatiske aktivitet aktiverer også forskellige typer cirkulerende celler, f.eks. trombocytter og neutrofile celler. Sidstnævnte bidrager i væsentlig grad til det fænomen, der er kendt som reperfusionsskade.59
De fleste forsøg, der blev gennemført i præperfusionstiden, sammenlignede brugen af intravenøse BB’er umiddelbart efter AMI-diagnosen efterfulgt af orale BB’er vs. placebo.58 Den tidlige iværksættelse af intravenøse BB’er blev undersøgt som en intervention, der kunne begrænse nekrosens omfang, men resultaterne var ikke overbevisende. I mangel af reperfusion er det vanskeligt at finde en fordel ved at begrænse nekrosenes omfang. I den farmakologiske reperfusion (fibrinolyse) æra var intravenøs atenolol ineffektiv til at reducere infarktstørrelsen i et randomiseret forsøg.60 En anden ikke-randomiseret undersøgelse viste imidlertid, at intravenøs metoprolol var forbundet med en mindre infarktstørrelse.61 Den første kliniske undersøgelse af dette spørgsmål hos patienter, der reperfunderes ved primær angioplastik, var METOCARD-CNIC-forsøget, der blev udført i Spanien.62 I dette forsøg var indgivelse af metoprolol forbundet med mindre infarktstørrelse53 og højere LVEF på lang sigt.63 Et andet efterfølgende forsøg, EARLY-BAMI-undersøgelsen, kunne ikke bekræfte de kardiobeskyttende virkninger af tidlig indgivelse af metoprolol hos patienter med AMI, der gennemgik primær angioplastik.64 Diskrepansen mellem de 2 forsøg synes at skyldes tidspunktet for indgivelse af metoprolol (meget tidligere i METOCARD-CNIC), fordi jo længere tid der går mellem den intravenøse indgift af metoprolol og reperfusionen, jo større er den kardioprotektive effekt.65 Den mekanisme, der ligger til grund for metoprolols evne til at reducere infarktstørrelsen, når det administreres intravenøst tidligt før reperfusion, synes at involvere en direkte effekt på cirkulerende neutrofiler og deres aggregering med trombocytter, hvilket resulterer i reduceret reperfusionsskade og reduceret mikrovaskulær obstruktion.66
Den tidlige anvendelse af intravenøse BB’er ved AMI er blevet sat i tvivl på grund af dens potentielle evne til at øge forekomsten af kardiogent chok. Denne bekymring er baseret på resultaterne af COMMIT-undersøgelsen.54 I dette forsøg var den tidlige administration af metoprolol til patienter med AMI forbundet med en betydelig reduktion af ventrikelflimmer, men en stigning i chok. COMMIT-populationen omfattede imidlertid patienter med fremskreden sygdom. Desuden gennemgik halvdelen ikke reperfusion. Desuden havde de patienter, der udviklede kardiogent shock, klare tegn på akut HF sammen med takykardi og hypotension. I modsætning hertil viste en metaanalyse, der omfattede alle forsøg med tidlig indgift af intravenøse BB’er, som beløb sig til mere end 73 000 patienter, at denne strategi er sikker, hvis den anvendes til patienter uden tegn på HF, og at den også reducerer hyppigheden af ventrikelflimmer betydeligt67 .
Baseret på de nye forsøg udført på patienter, der gennemgår primær angioplastik, anbefaler ESC-retningslinjerne for behandling af patienter med ST-segmentelevation AMI tidlig anvendelse af intravenøse BB’er (klasse IIa A) i fravær af HF-tegn eller systolisk hypotension (
mmHg).68 Vedligeholdelse af betablokkere efter infarkt
Anvendelsen af BB’er efter AMI blev undersøgt udtømmende i præperfusionsæraen.58 Bortset fra COMMIT-forsøget,54 med en opfølgning på kun 1 måned, er det eneste kliniske forsøg, der har undersøgt den rolle, som orale vedligeholdelses-BB’er efter AMI spiller, CAPRICORN-undersøgelsen.16 I dette forsøg blev 1950 post-AMI-patienter med LVEF ≤ 40 % randomiseret til carvedilol eller placebo. Brug af BB var forbundet med en reduktion i den samlede dødelighed.16 Da mange af de forsøg, der fokuserer på HFrEF (tabel 1), omfattede post-AMI-patienter, anses det for etableret, at alle patienter, der har haft en AMI med en LVEF ≤ 40 %, har en indikation for BB’er. Der mangler imidlertid evidens for fordelene ved BB’er for post-AMI-patienter med en LVEF> 40 %. Talrige observationsstudier har forsøgt at kaste lys over dette spørgsmål, men alle har store begrænsninger og giver derfor ikke endelig information (et aspekt, der er gennemgået af Ibáñez et al.1).
Givet alt ovenstående anbefaler ESC’s kliniske retningslinjer for klinisk praksis for patienter med AMI kraftigt (klasse IA) brug af BB, når LVEF er ≤ 40 %, uanset om patienterne har ST-segmenthævning eller ikke-ST-segmenthævning ved AMI. Anbefalingen for patienter, der har haft en AMI med en LVEF> 40%, er dog svagere.1
Figur 4 viser de kliniske situationer med dokumenteret fordel af BB’er i forbindelse med AMI.
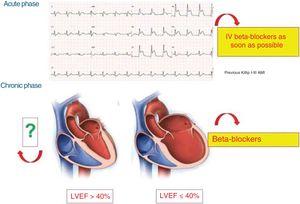
Aktuel status for betablokkere i de forskellige faser af akut koronarsyndrom. AMI, akut myokardieinfarkt; IV, intravenøs; LVEF, venstre ventrikulær ejektionsfraktion.
På grund af denne mangel på evidens om et så vigtigt aspekt af den daglige kliniske behandling er 3 store pragmatiske kliniske forsøg i gang i Europa for at undersøge BB’s rolle hos patienter uden nedsat LVEF, der har haft en AMI. Det kliniske REBOOT-forsøg (NCT03596385), der ledes af det nationale center for kardiovaskulær forskning (CNIC) i Spanien, omfatter deltagelse af mere end 70 spanske og italienske centre. Omkring 8500 post-AMI-patienter med en LVEF> 40% vil blive inkluderet i denne store spanske undersøgelse. Desuden gennemføres REDUCE-SWEDEHEART- (NCT03278509) og BETAMI- (NCT03646357) forsøgene i henholdsvis Sverige og Norge; deres design svarer til REBOOT-forsøget. Disse store kliniske forsøg vil få en klar indvirkning på den kliniske praksis i denne sammenhæng.
Tabel 3 opsummerer resultaterne af de forskellige kliniske forsøg16,53,54,60,64,69-72 , som har analyseret BB’ernes rolle, enten i den akutte fase af AMI eller i vedligeholdelsesperioden efter den akutte hændelse.
Hovedforsøg om anvendelse af betablokkere ved akut koronarsyndrom
| Studie (y) | Reperfusion | Medicin | Nr. | Kriterier | Resultater | ||
|---|---|---|---|---|---|---|---|
| Intravenøs administration i akut fase | |||||||
| ISIS-I69 (1986)* | Ingen | Atenolol | 16 027 | Mistanke om AMI på ethvert sted | 15% reduktion i dødelighed | ||
| MIAMI70 (1985)* | Ingen | Metoprolol | 5778 | Mistanke om AMI på et hvilket som helst sted | 29% reduktion i mortalitet | ||
| MILIS71 (1986) | Nej | Propranolol | 269 | Suspekt AMI på ethvert sted | Ingen reduktion i mortalitet eller AMI-størrelse | ||
| Van de Werf et al.60 (1993) | Ja (fibrinolyse) | Atenolol | 292 | Mistanke om AMI uanset sted | Ingen reduktion i dødelighed eller AMI-størrelse | ||
| METOCARD-CNIC53 (2013)* | Ja (angioplastik) | Metoprolol | 270 | Mistanke om tidligere AMI | Reduktion i AMI-størrelse og efterfølgende stigning i LVEF | ||
| FREMTID-BAMI64 (2016) | Ja (angioplastik) | Metoprolol | 683 | Mistanke om AMI på ethvert sted | Ingen reduktion af infarktstørrelse | Ingen reduktion af infarktstørrelse | |
| Kronisk administration efter infarkt | |||||||
| BHAT72 (1982)* | Ingen | Propranolol | 3837 | Infarkt uanset sted | 26% reduktion i dødelighed | ||
| CAPRICORN16 (2001)* | Ja (fibrinolyse) | Carvedilol | 1959 | Infarkt uanset sted og LVEF ≤ 40 % | 23 % reduktion i dødelighed | ||
| COMMIT54 (2005) | Fibrinolyse: 54% af prøven; 46% ikke reperfunderet | Metoprolol | 45 852 | Infarkt på ethvert sted uden LVEF-begrænsning | Ingen reduktion i mortalitet.Reduktion af reinfarkt og VF | ||
AMI, akut myokardieinfarkt; LVEF, venstre ventrikulær ejektionsfraktion; VF, ventrikelflimmer.
Studier med positive (gunstige) resultater for betablokkere.
Stabil iskæmisk hjertesygdom
De antianginale virkninger af BB’er er veletablerede og indgår i de kliniske retningslinjer for klinisk praksis.73 Sammenlignet med calciumkanalblokkere reducerer BB’er anginale episoder og tiden til iskæmiens indtræden ved anstrengelsestestest.74 Ingen kliniske forsøg har imidlertid undersøgt på randomiseret vis og med tilstrækkelig statistisk styrke, om BB’er forbedrer overlevelsen hos patienter med stabil koronarsygdom, men uden AMI eller rEF. I en systematisk gennemgang og metaanalyse viste brugen af dem ikke at reducere dødeligheden.75 REACH-registret, som omfattede mere end 40 000 svenske patienter, fandt ingen fordele hos patienter med stabil koronarsygdom, men uden tidligere AMI, efter propensity score-justering. Flere undersøgelser støtter den konklusion, at brugen af BB’er ved stabil koronarsygdom og uden tidligere AMI ikke har gavnlige virkninger på dødelighed og negative kardiovaskulære hændelser.76
KONKLUSIONER
BB’er er en gruppe af lægemidler, der er en del af det terapeutiske standardarmeringsprogram til behandling af flere kardiovaskulære sygdomme. Deres fordele hos patienter med HF og ventrikeldysfunktion er klart fastslået, og det samme gælder deres antiarytmiske virkninger. I forbindelse med AMI reducerer tidlig indgift af intravenøse BB’er forekomsten af ventrikelflimmer og kan mindske infarktstørrelsen, selv om det stadig er nødvendigt at vise, om dette giver sig udslag i en forbedring af morbiditet og mortalitet på lang sigt. Fordelen ved kroniske BB’er hos patienter uden ventrikeldysfunktion, som har haft en AMI, er ikke fastslået. Selv om de tidligere var almindeligt anvendt, har BB’ernes rolle hos patienter med hypertension uden andre komorbiditeter mistet sin betydning. På trods af mere end 4 årtiers brug af BB’er er der stadig kliniske og eksperimentelle spørgsmål, der skal løses, hvilket gør denne gruppe af lægemidler til en af de mest fascinerende, vi har til rådighed.
FUNDING
B. Ibáñez leder projekter i forbindelse med emnet for denne anmeldelse for det spanske kardiologiselskab (2017 Translational Research Project) og MICINN (det spanske ministerium for videnskab, innovation og universiteter) gennem Instituto de Salud Carlos III Health Research Fund (PI16/02110) og Den Europæiske Fond for Regionaludvikling (EFRU: SAF2013-49663-EXP). CNIC (Nationalt center for kardiovaskulær forskning) er finansieret af MICINN, ISCiii og ProCNIC Foundation og er et Severo Ochoa Center of Excellence (SEV-2015-0505).
Interessekonflikter
Ingen anmeldt.