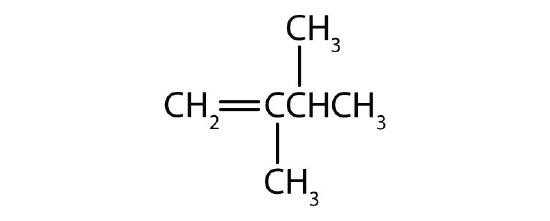
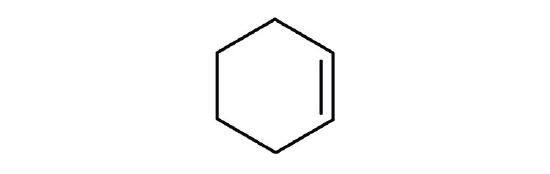
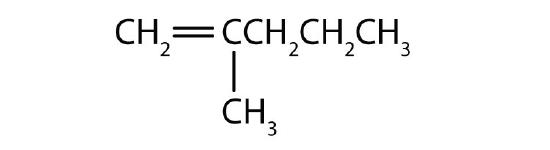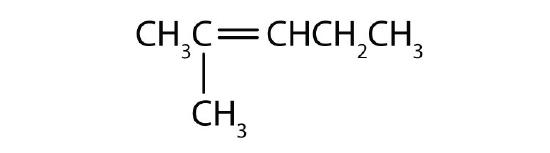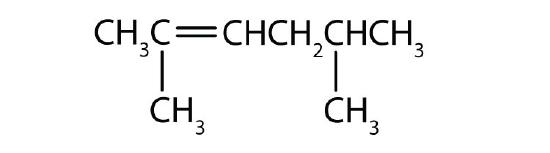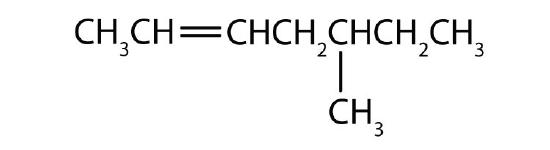Læringsmål
- At navngive alkener med givne formler og skrive formler for alkener med givne navne.
Som tidligere nævnt er alkener kulbrinter med kulstof-kulstof-dobbeltbindinger (R2C=CR2) og alkyner er kulbrinter med kulstof-kulstof-tripelbindinger (R-C≡C-R). Tilsammen kaldes de umættede kulbrinter, fordi de har færre hydrogenatomer end en alkan med det samme antal kulstofatomer, hvilket fremgår af følgende generelle formler:
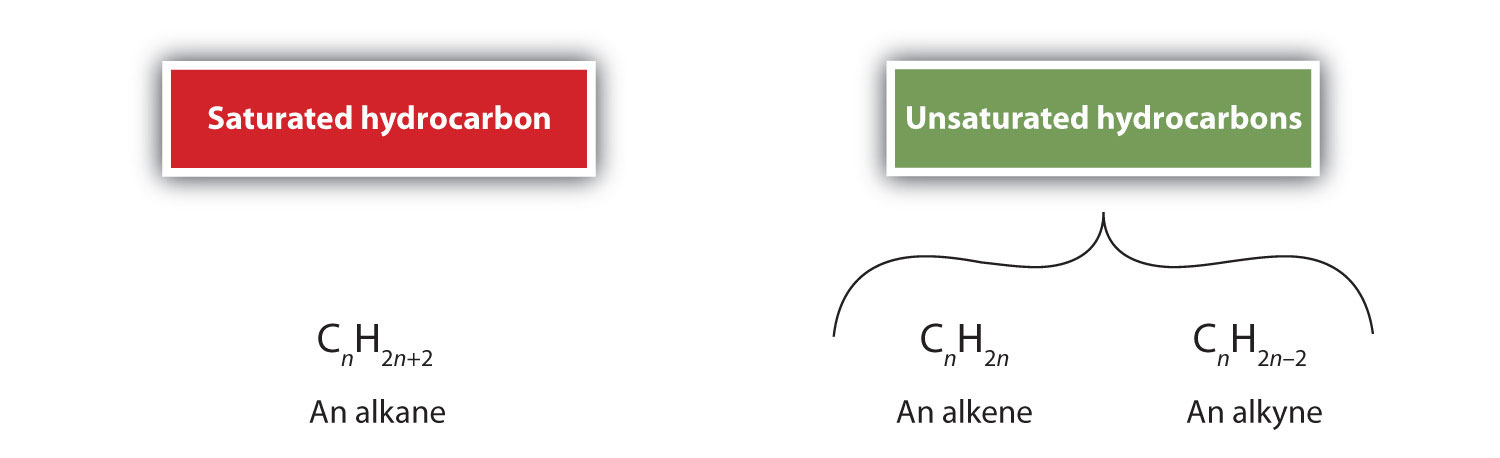
Nogle repræsentative alkener – deres navne, strukturer og fysiske egenskaber – er angivet i tabel \(\PageIndex{1}\).
| IUPAC-navn | Molekylformel | Kondenseret strukturformel | Smeltepunkt (°C) | Kogningspunkt (°C) | |
|---|---|---|---|---|---|
| ethen | C2H4 | CH2=CH2 | -169 | -104 | |
| propen | C3H6 | CH2=CHCH3 | -185 | -47 | |
| 1-buten | C4H8 | CH2=CHCHCH2CH3 | -185 | -6 | |
| 1-penten | C5H10 | CH2=CH(CH2)2CH3 | -138 | 30 | |
| 1-hexen | C6H12 | CH2=CH(CH2)3CH3 | -140 | 63 | |
| 1-hepten | C7H14 | CH2=CH(CH2)4CH3 | -119 | 94 | |
| 1-octen | C8H16 | CH2=CH(CH2)5CH3 | -102 | 121 |
Vi har kun anvendt kondenserede strukturformler i tabel \(\PageIndex{1}\). CH2=CH2 står således for
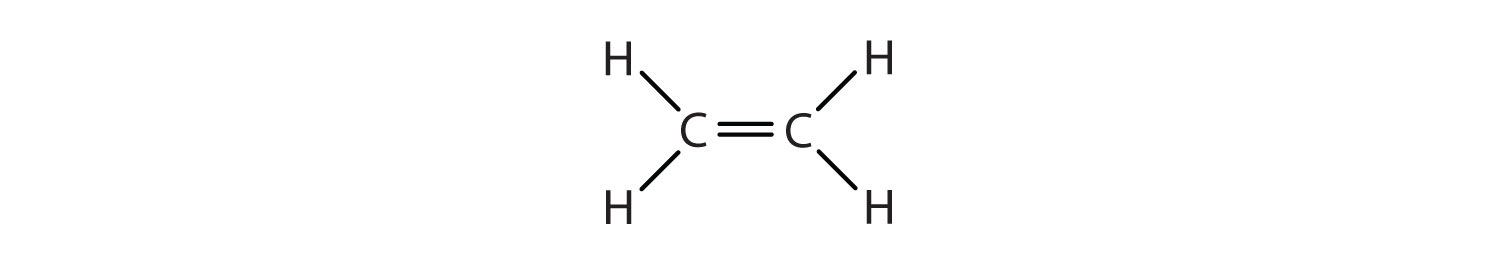
Dobbeltbindingen deles af de to kulstofatomer og involverer ikke hydrogenatomerne, selv om den kondenserede formel ikke gør dette tydeligt. Bemærk, at molekylformlen for ethen er C2H4, mens molekylformlen for ethan er C2H6.
De to første alkener i tabel \(\PageIndex{1}\), ethen og propylen, kaldes oftest ved deres almindelige navne – henholdsvis ethen og propylen (figur \(\PageIndex{1}\)). Ethylen er et vigtigt kommercielt kemikalie. Den kemiske industri i USA producerer ca. 25 mia. kg ethylen årligt, hvilket er mere end noget andet syntetisk organisk kemikalie. Mere end halvdelen af dette ethylen går til fremstilling af polyethylen, et af de mest kendte plastmaterialer. Propylen er også et vigtigt industrikemikalie. Det omdannes til plast, isopropylalkohol og en række andre produkter.

Selv om der kun findes ét alken med formlen C2H4 (ethen) og kun ét med formlen C3H6 (propen), findes der flere alkener med formlen C4H8.
Her er nogle grundlæggende regler for navngivning af alkener fra International Union of Pure and Applied Chemistry (IUPAC):
- Den længste kæde af kulstofatomer, der indeholder dobbeltbindingen, betragtes som moderkæden. Den navngives ved hjælp af samme stamme som den alkan, der har det samme antal kulstofatomer, men ender på -en for at identificere den som en alken. Således er forbindelsen CH2=CHCHCH3 propen.
- Hvis der er fire eller flere kulstofatomer i en kæde, skal vi angive dobbeltbindingens position. Kulstofatomerne nummereres således, at det første af de to, der er dobbeltbundet, får det laveste af de to mulige numre. forbindelsen CH3CH=CHCHCHCH2CH3 har f.eks. dobbeltbindingen mellem det andet og tredje kulstofatom. Dens navn er 2-penten (ikke 3-penten).
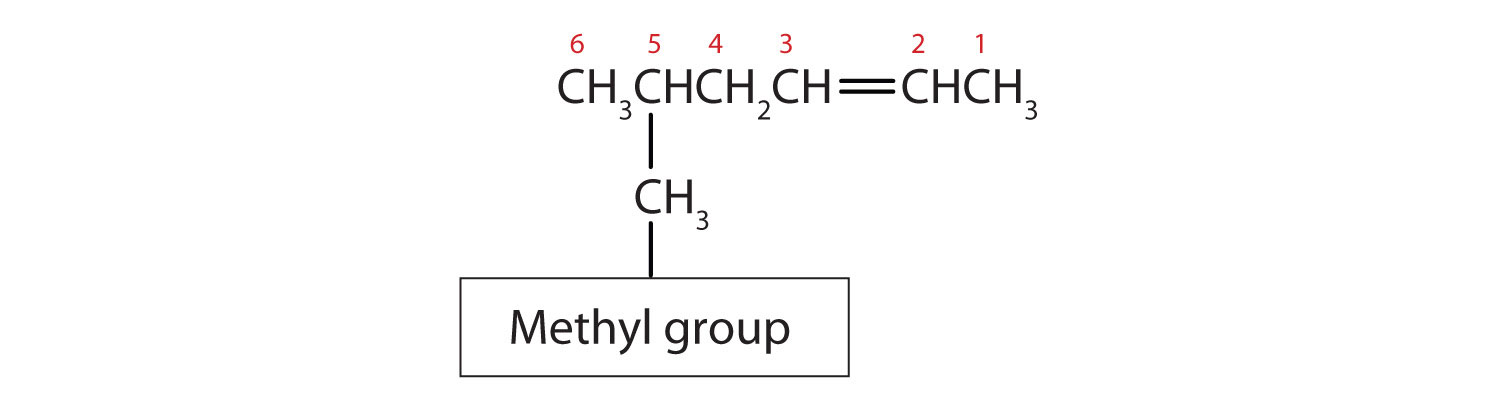
- Substituerende grupper navngives som ved alkaner, og deres position angives med et tal. Nedenstående struktur er således 5-methyl-2-hexen. Bemærk, at nummereringen af moderkæden altid sker på en sådan måde, at dobbeltbindingen får det laveste nummer, også selv om det medfører, at en substituent får et højere nummer. Dobbeltbindingen har altid prioritet ved nummereringen.
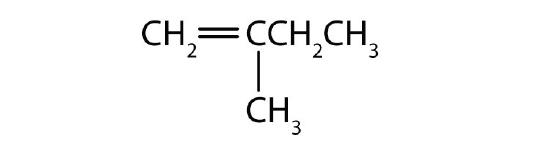
Eksempel \(\PageIndex{1}\)
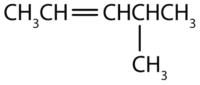
Nævn hver forbindelse.
Løsning
- Den længste kæde, der indeholder dobbeltbindingen, har fem kulstofatomer, så forbindelsen er en penten (regel 1). For at give det første kulstofatom i dobbeltbindingen det laveste nummer (regel 2), nummererer vi fra venstre, så forbindelsen er en 2-penten. Der er en methylgruppe på det fjerde kulstofatom (regel 3), så forbindelsens navn er 4-methyl-2-penten.
- Den længste kæde, der indeholder dobbeltbindingen, har fem kulstofatomer, så grundforbindelsen er en penten (regel 1). For at give det første kulstofatom i dobbeltbindingen det laveste nummer (regel 2), nummererer vi fra venstre, så forbindelsen er en 2-penten. Der er en methylgruppe på det tredje kulstofatom (regel 3), så forbindelsens navn er 3-methyl-2-penten.
Ovelse \(\PageIndex{1}\)
Nævn hver forbindelse.
-
CH3CH2CH2CH2CH2CH2CH=CHCHCH3
-
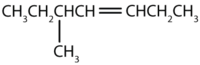
Som der er cycloalkaner, er der også cycloalkener. Disse forbindelser benævnes som alkener, men med præfikset cyclo- knyttet til begyndelsen af navnet på det overordnede alken.
Eksempel \(\PageIndex{2}\)
Tegn strukturen for hver forbindelse.
- 3-methyl-2-penten
- cyclohexen
Løsning
- Skriv først moderkæden med fem kulstofatomer: C-C-C-C-C-C-C-C. Tilføj derefter dobbeltbindingen mellem det andet og tredje kulstofatom:
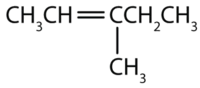
Sæt nu methylgruppen på det tredje kulstofatom og tilføj nok hydrogenatomer til at give hvert kulstofatom i alt fire bindinger.
- Først skal du overveje, hvad hver af de tre dele af navnet betyder. Cyclo betyder en ringforbindelse, hex betyder 6 kulstofatomer, og -en betyder en dobbeltbinding.

Ovelse \(\PageIndex{2}\)
Tegn strukturen for hver forbindelse.
- 2-ethyl-1-hexen
- cyclopenten
Begrebsgennemgang Øvelser
-
Nævn kort de vigtige forskelle mellem et mættet kulbrinte og et umættet kulbrinte.
-
Oplys kort de vigtige forskelle mellem en alken og en alkan.
-
Klassificer hver forbindelse som mættet eller umættet. Identificer hver af dem som en alkan, et alken eller et alkyn.
-
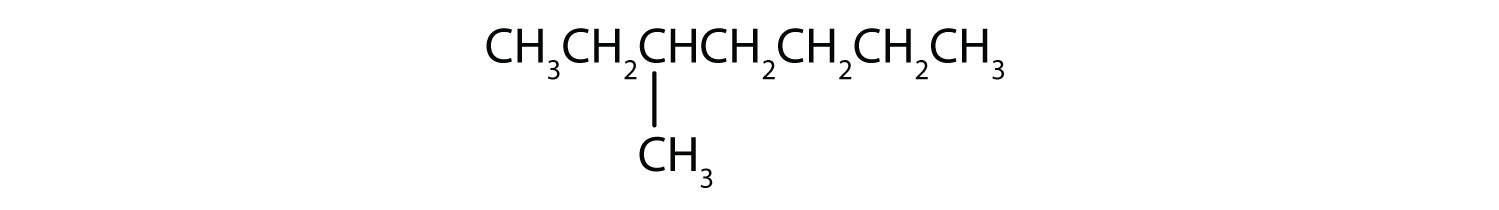
- CH3CH2C≡CCH3
-
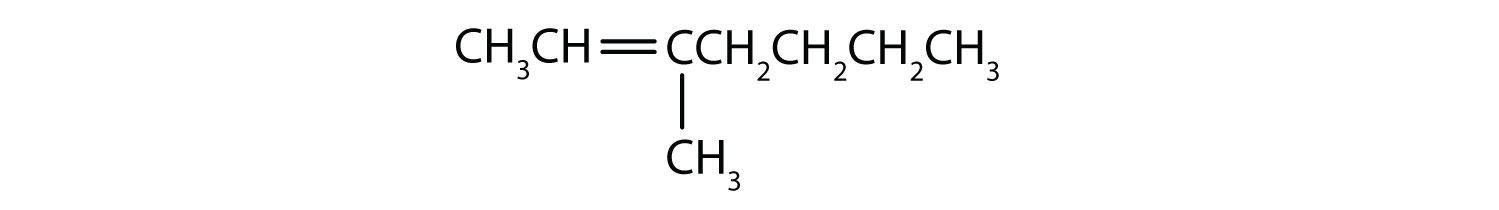
-
Svar
-
Umættede carbonhydrider har dobbelt- eller trippelbindinger og er ret reaktive; mættede carbonhydrider har kun enkeltbindinger og er ret ureaktive.
-
En alken har en dobbeltbinding; en alkan har kun enkeltbindinger.
-
- mættet; alkan
- umættet; alkyn
- umættet; alken
Key Takeaway
- Alkener er carbonhydrider med en kulstof-kulstof-dobbeltbinding.
Opgaver
-
Tegn strukturen for hver forbindelse.
- 2-methyl-2-penten
- 2,3-dimethyl-1-buten
- cyclohexen
-
Tegn strukturen for hver forbindelse.
- 5-methyl-1-hexen
- 3-ethyl-2-penten
- 4-methyl-2-hexen
-
Nævn hver forbindelse i henhold til IUPAC-systemet.
-
-
Nævn hver forbindelse i henhold til IUPAC-systemet.
-
Svar
-
- 2-methyl-1-pentene
- 2-methyl-2-pentene
- 2,5-dimethyl-2-hexen