Kemiallinen alkuaine rauta luokitellaan siirtymämetalliin. Se on tunnettu jo antiikin ajoista lähtien. Sen löytäjä ja löytöajankohta ovat tuntemattomia.

Tietovyöhyke
| Luokitus: | Rauta on siirtymämetalli |
| Väri: | hopeanharmaa |
| Atomipaino: | 55.847 |
| Tila: | kiinteä |
| Lämpötila: | kiinteä |
| Sulamispiste: | 1535.1 oC, 1808.2 K |
| Kiehumispiste: | 2750 oC, 3023 K |
| Elektronit: | 26 |
| Protonit: | 26 |
| Runsaimmin esiintyvässä isotoopissa on neutroneita: | 30 |
| Elektronikuoret: | 2,8,14,2 |
| Elektronikonfiguraatio: | 3d6 4s2 |
| Tiheys @ 20oC: | 7.87 g/cm3 |
Näytä lisää, mm: Lämmöt, energiat, hapettuminen,
reaktiot, yhdisteet, säteet, johtavuudet
| Atomitilavuus: | 7.1 cm3/mol |
| Rakenne: | bcc: body-centered cubic |
| Kovuus: | 4.0 mohs |
| Ominaislämpökapasiteetti | 0.44 J g-1 K-1 |
| Fuusiolämpö | 13.80 kJ mol-1 |
| Atomisointilämpö | 415 kJ mol-1 |
| Höyrystymislämpö | 349.60 kJ mol-1 |
| 1. ionisaatioenergia | 759.3 kJ mol-1 |
| 2. ionisaatioenergia | 1561.1 kJ mol-1 |
| 3. ionisaatioenergia | 2957.3 kJ mol-1 |
| Elektronien affiniteetti | 15.7 kJ mol-1 |
| Minimi hapetusluku | -2 |
| Min. yhteinen hapetusluku | 0 |
| Suurin hapetusluku | 6 |
| Max. yhteinen hapetusluku. | 3 |
| Elektronegatiivisuus (Paulingin asteikko) | 1.9 |
| Polarisoituvuusmäärä | 8.4 Å3 |
| Reaktio ilman kanssa | lievä, ⇒ Fe3O4 |
| Reaktio 15 M HNO3:n kanssa | passivoitu |
| Reaktio 6 M:n HCl:n kanssa | voimakas, ⇒ H2, FeCl2 |
| Reaktio 6 M NaOH:n kanssa | – |
| Oksidi(t) | FeO, Fe2O3 (hematiitti), Fe3O4 (magnetiitti) |
| Hydridi(t) | ei ole |
| Kloridi(t) | FeCl2, FeCl3 |
| Atomisäde | 140 pm |
| Ionisäde (1+-ioni) | – |
| Ionisäde (2+-ioni) | 77 pm |
| Ionisäde (3+-ioni) | 63 pm |
| Ionisäde (1- Ioni) | – |
| Ionisäde (2-ioni) | – |
| Ionisäde (3-ioni) | – |
| Lämmönjohtavuus | 80.4 W m-1 K-1 |
| Sähkönjohtavuus | 11.2 x 106 S m-1 |
| Jäätymis-/sulamispiste: | 1535.1 oC, 1808,2 K |
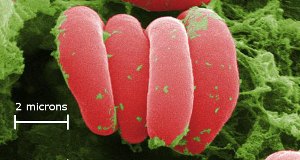
Punaiset verisolut – väri tulee hemoglobiinin raudasta. Solut on suurennettu x10 000. Jos kasvattaisit x10 000, voisit asettaa jalkasi Seattleen ja koskettaa käsilläsi Perthiä, Australiaa. Hemoglobiinin sisältämä rauta kuljettaa happea kehossamme. Kuva Ref. (10)

Lähikuva rautameteoriitista: Tällaiset meteoriitit olivat todennäköisesti esi-isiemme ensimmäinen raudanlähde. Tämä on Sikhote-Alinin meteoriitin fragmentti – noin 93 % rautaa, 6 % nikkeliä ja 1 % muita alkuaineita. Meteoriitin pinta on sulanut peukalonjäljen muotoiseksi lentäessään planeettamme ilmakehän läpi. Kuva: Carl Allen, NASA JSC Photo S94-43472.

Rauta- ja teräsromua kierrätykseen. Kuinka ajat ovatkaan muuttuneet; rauta oli aikoinaan kahdeksan kertaa arvokkaampaa kuin kulta.
Raudan löytäminen
Rauta on tunnettu jo muinaisista ajoista lähtien.
Ensimmäinen ihmisen käyttämä rauta on todennäköisesti peräisin meteoriiteista.
Useimmat avaruudesta maahan putoavat esineet ovat kivisiä, mutta pieni osa, kuten kuvassa oleva, on ”rautameteoriitteja”, joiden rautapitoisuus on yli 90 prosenttia.
Rauta syöpyy helposti, joten muinaisilta ajoilta peräisin olevat rautaesineet ovat paljon harvinaisempia kuin hopeasta tai kullasta tehdyt esineet. Tämän vuoksi raudan historiaa on vaikeampi jäljittää kuin vähemmän reagoivien metallien.
Meteoriittiraudasta tehtyjä esineitä on löydetty noin 5000 eaa. ajalta (ja ne ovat siis noin 7000 vuotta vanhoja) – esimerkiksi rautahelmiä Egyptin haudoista. (1)
Mesopotamiassa (Irakissa) on todisteita siitä, että ihmiset sulattivat rautaa noin 5000 eKr.
Egyptistä ja Mesopotamiasta on löydetty sulatetusta raudasta tehtyjä esineitä noin 3000 eaa. ajalta. (1), (2), (3)
Tuolloin rauta oli seremoniallinen metalli; se oli liian kallista käytettäväksi jokapäiväisessä elämässä. Assyrialaiset kirjoitukset kertovat, että rauta oli kahdeksan kertaa arvokkaampaa kuin kulta. (1)
Rautakausi alkoi noin 1300-1200 eaa., kun raudasta tuli tarpeeksi halpaa korvatakseen pronssin.
Hiilen lisääminen rautaan teräksen valmistamiseksi oli aluksi luultavasti satunnaista – sulan raudan ja sulatuspalosta peräisin olevan puuhiilen yhteen tulemista. Tämä tapahtui todennäköisesti noin 1000 eaa. (4)
Ennen kuin tämä tapahtui, oli vain vähän teknologisia syitä sille, että pronssikausi väistyi rautakauden tieltä; tarvittiin tekniikoita, joilla rautaa parannettiin lisäämällä hiiltä (teräksen valmistamiseksi) ja kylmätyöstämällä, ennen kuin rautaa voitiin täysin suosia pronssin sijaan. (5)
Rooman aikana rautaa käytettiin yleisesti. Ensimmäisellä vuosisadalla Plinius vanhempi sanoi: ”Raudan avulla rakennamme taloja, hakkaamme kallioita ja suoritamme niin monia muita hyödyllisiä elämäntehtäviä.” (6)
Kemiallinen symboli Fe on peräisin latinankielisestä sanasta ”ferrum”, joka tarkoittaa rautaa. Itse sana rauta tulee anglosaksisesta sanasta ’iren’.
Interenkiintoisia faktoja raudasta
- Kolmanneksen maapallon massasta uskotaan olevan rautaa, josta suurin osa on syvällä planeetan sisällä, sen ytimessä.
- Maassa on tarpeeksi rautaa kolmen uuden planeetan luomiseen, joista jokainen olisi yhtä massiivinen kuin Mars.
- Syvällä Maan sisällä olevan nestemäisen raudan kierron uskotaan synnyttävän sähkövirrat, jotka luovat planeettamme magneettikentän.
- Rauta on välttämätöntä ihmisen aivojen kehitykselle. Lasten raudanpuute johtaa muun muassa heikentyneeseen oppimiskykyyn. (7)
- Vanhoina aikoina ihmiset eivät tienneet, miten hyvin runsaasti rautaa oli maapallolla. Heidän ainoa metallisen raudan lähteensä oli meteoriitit. Assyrialaisista kirjoituksista saamme tietää, että rauta oli kahdeksan kertaa arvokkaampaa kuin kulta. Harvinaisuutensa lisäksi rauta saattoi olla hyvin haluttua myös siksi, että sitä pidettiin taivaasta tulevana jumalien lahjana: muinaiset egyptiläiset kutsuivat sitä nimellä ”ba-ne-pe”, joka tarkoittaa ”taivaan metallia”. Yhteyttä taivaaseen vahvistavat pyramiditekstit, jotka käännetään esimerkiksi seuraavasti: ”luuni ovat rautaa ja raajani ovat katoamattomia tähtiä”. (8) (9)
- Rauta oli ensimmäinen löydetty magneettinen metalli. Antiikin merenkulkijat käyttivät jalokiviä, koska niitä voitiin käyttää kompasseina, jotka osoittivat magneettiseen pohjoisnapaan; tämän kuvasi antiikin kreikkalainen filosofi Thales Miletolainen vuonna 600 eaa. Jalokivet valmistettiin magnetiitista, joka on luonnossa esiintyvä rautaoksidi. Magnetiitin kaava on FeO.Fe2O3.
- Joillain eläimillä on kuudes aisti – magneettinen aisti. Magnetiittia on löydetty monista eläimistä, kuten hunajamehiläisistä, kirjekyyhkyistä ja delfiineistä. Nämä eläimet ovat herkkiä maan magneettikentälle, mikä auttaa niiden navigointikykyä.
- Namibiassa sijaitseva Hoba-meteoriitti on maailman suurin luonnossa esiintyvä rautakappale, joka painaa yli 60 tonnia. Se koostuu 82-83-prosenttisesti raudasta, 16-17-prosenttisesti nikkelistä, noin 1 prosentista kobolttia ja hyvin pienistä jäljistä muita alkuaineita. Hoban meteoriitti on suurin koskaan löydetty yksittäinen meteoriitti.
- Rauta on ferromagneettinen. Ferromagnetismi on vahvin magnetismin tyyppi. Muita yleisiä ferromagneettisia metalleja ovat nikkeli ja koboltti.
- Erittäin voimakkaita magneetteja voidaan valmistaa käyttämällä rautaa, nikkeliä tai kobolttia yhdessä harvinaisten maametallien kanssa. NIB-magneetit (neodyymi – rauta – boori) keksittiin 1980-luvun alussa. Ne ovat seos suhteessa Nd2Fe14B. Niitä käytetään tietokoneissa, matkapuhelimissa, lääketieteellisissä laitteissa, leluissa, moottoreissa, tuulivoimaloissa ja audiojärjestelmissä.



Esiintyminen ja ominaisuudet
Haitalliset vaikutukset:
Rautaa ei pidetä myrkyllisenä.
Ominaisuudet:
Rauta on sitkeää, harmaata, suhteellisen pehmeää metallia ja se johtaa kohtalaisen hyvin lämpöä ja sähköä.
Se vetää puoleensa magneetteja ja se voidaan helposti magnetoida.
Puhdas metalli on kemiallisesti hyvin reaktiivinen ja ruostuu helposti kosteassa ilmassa muodostaen punaruskeita oksideja.
Raudalla on kolme allotrooppista muotoa, jotka tunnetaan nimillä alfa, gamma ja delta.
Alfa-rauta, joka tunnetaan myös ferriittinä, on raudan vakaa muoto normaalilämpötiloissa.
Raudan käyttötarkoitukset
Rauta on halvin ja tärkein kaikista metalleista – tärkeä siinä mielessä, että rauta on ylivoimaisesti yleisimmin käytetty metalli, sillä sen osuus maailman metallituotannosta on 95 prosenttia.
Rautaa käytetään teräksen ja muiden rakentamisessa ja teollisuudessa tärkeiden seosten valmistukseen.
Rauta on myös elintärkeää elävien organismien toiminnassa, sillä se kuljettaa happea veressä hemoglobiinimolekyylin kautta.
Runsaus ja isotoopit
Runsaus maankuori: 5,6 % painosta, 2,1 % mooleista
Runsaus aurinkokunta: 1000 miljoonasosaa painosta, 30 miljoonasosaa mooleista
Kustannus, puhdas: 7,2 dollaria 100g:ssa
Kustannus, irtotavarana: 0,02 dollaria 100g:ssa
Lähde: Rautaa ei esiinny luonnossa vapaana, vaan sitä on rautamalmissa, kuten hematiitissa (Fe2O3), magnetiitissa (Fe3O4) ja takoniitissa. Kaupallisesti rautaa valmistetaan uunissa noin 2000 oC:n lämpötilassa pelkistämällä hematiittia tai magnetiittia hiilen kanssa.
Isotoopit: Raudalla on 24 isotooppia, joiden puoliintumisajat tunnetaan ja joiden massanumerot ovat 46-69. Luonnossa esiintyvä rauta on neljän isotoopin seos, ja niitä esiintyy esitetyissä prosenttiosuuksissa: 54Fe (5,8 %), 56Fe (91,8 %), 57Fe (2,1 %) ja 58Fe (0,3 %).

- Henry Maryon, Early Near Eastern Steel Swords., 65, 1961, American Journal of Archaeology s. 1.
- Michael D. Fenton, Mineral Commodity Profiles – Iron and Steel., 2005, U.S. Geological Survey.
- R. J. Forbes, Studies in Ancient Technology., IX, 1965, s247.
- Michael Woods, Mary B. Woods, Ancient Machines: From Wedges to Waterwheels., 2000, s30, Runestone Press.
- Vincent C. Pigott, The Archaeometallurgy of the Asian Old World. 1999, s28, UPenn Museum of Archaeology.
- Mary Elvira Weeks, Discovery of the Elements. 2003, s5, Kessinger Publishing.
- http://www.ncbi.nlm.nih.gov/pubmed/17101454.
- John G. Burke, Cosmic Debris: Meteorites in History., 1986, s229, University of California Press.
- Robert G. Bauval, Tutkimus benbenin kiven alkuperästä. 14, 1989, Discussions in Egyptology.
- Kuva: CDC
Lainaa tätä sivua
Verkkolinkitystä varten kopioi ja liitä jompikumpi seuraavista:
<a href="https://www.chemicool.com/elements/iron.html">Iron</a>
tai
<a href="https://www.chemicool.com/elements/iron.html">Iron Element Facts</a>
Jos haluat siteerata tätä sivua akateemisessa asiakirjassa, käytä seuraavaa MLA-standardin mukaista viittaustapaa:
"Iron." Chemicool Periodic Table. Chemicool.com. 06 Oct. 2012. Web. <https://www.chemicool.com/elements/iron.html>.