Introduction
Maailman terveysjärjestön mukaan masennuksesta kärsii arviolta 350 miljoonaa ihmistä maailmanlaajuisesti (Organization, 2017). Masennuspotilaat osoittavat ahdistuneisuushäiriöiden oireita ja niihin liittyy kyvyttömyys kokea mielihyvää ja kiinnostusta, keskittymiskyvyn heikkeneminen, itseepäily, sosiaalinen ahdistuneisuus, uni- ja ruokahaluttomuus (Namola ym., 2015). Tärkeimmät masennusta aiheuttavat tekijät ovat aivojen kemikaalien tai hormonien epätasapaino. Tärkein masennukseen liittyvä hormoni on serotoniini. Muita hormoneja ovat noradrenaliini ja dopamiini (Yi ym., 2008). Näitä hormoneja tarvitaan aivojen normaaliin toimintaan ja tunteiden hallintaan. Näiden hormonien tuhoutuminen voi aiheuttaa aivoissa kemiallista epätasapainoa, joka johtaa masennukseen.
Depressiota voidaan hoitaa sen vakavuudesta riippuen psykoterapialla tai lääkityksellä. Masennuslääkkeet ovat tärkeimmät masennuksen hoitoon käytettävät lääkkeet. Saatavilla on monenlaisia masennuslääkkeitä, ja ne eroavat toisistaan vain tavassa, jolla ne vaikuttavat aivoihin, kustannuksissa ja haittavaikutusprofiilissa. Ensilinjan hoidossa useimmille potilaille määrätään joko trisyklinen masennuslääke (TCA) tai selektiivinen serotoniinin takaisinoton estäjä (SSRI; McCarthy ym., 2016). Ahdistuneisuuden hoidossa yleisesti käytettyjä lääkkeitä ovat bentsodiatsepiinit. Vaikka markkinoilla on monia masennuslääkkeitä, joita käytetään masennuksen hoitoon, näiden lääkkeiden käytön jälkivaikutukset aiheuttavat suurta huolta (Binfaré ym., 2009). Vaihtoehtoinen masennuksen hoito on kasviperäisten lääkkeiden käyttö (Fajemiroye et al., 2016). Kasviuutteiden käyttö on saamassa yhä laajempaa hyväksyntää lääketieteen ammattilaisten ja potilaiden keskuudessa. Suurin osa masennuksen hoidossa hyödynnetyistä kasvirohdosvalmisteista on raakoja tai puolipuhdistettuja uutteita (Calixto ym., 2000; Carlini, 2003; Guan ja Liu, 2016).
Tutkimusraportteja, joissa on mukana aktiivinen periaate, joka kykenee aikaansaamaan toimintaa keskushermostossa (CNS), on niukasti. Carlinin (2003) katsaus sisältää tietoa ainoastaan psykoanaleptisista, psykoleptisistä ja psykodysleptisistä vaikutuksista. Guanin ja Liun (2016) tuoreessa katsauksessa käsiteltiin luonnollisista ja synteettisistä lähteistä eristettyjen flavonoidien masennuslääkkeiden antidepressiivisten vaikutusten rakenne-aktiivisuussuhdetta. Synteettisiä indolialkaloideja, niiden aktiivisuutta ja mahdollista käyttöä lääketieteessä on jo tarkasteltu useissa artikkeleissa (de Sa et al., 2009). Yhtään katsausartikkelia ei kuitenkaan ole julkaistu, jossa eristetyt kasvi-indolialkaloidit korreloituisivat masennuslääkkeiden vaikutukseen. Tässä katsauksessa annetaan tietoa luonnon indolialkaloidien potentiaalista neurologisten häiriöiden hoidossa, rakenne-aktiivisuussuhdetutkimuksista ja näiden laajuudesta muihin bioaktiivisiin metaboliitteihin mahdollisina masennuslääkkeiden johtolankoina kemiallisen rakenteen näkökulmasta. Se on koottu tieteellisten lehtien bibliografisella tutkimuksella ja Web of Science -elektronisten tietokantojen kautta tunnistetun asiaankuuluvan kirjallisuuden avulla.
Antidepressiiviset kasvit
Tämä katsausartikkeli käsittelee kasveja, joilla on toimintaa keskushermostoon. Vaikka monet kasvityypit kuuluvat tähän luokkaan, tuomme esiin vain kasveja, joilla on masennuslääkkeitä. Kaksi indolialkaloideja sisältävää kasvia ovat Passiflora incarnata L. (passion kukka) ja Mitragyna speciosa (Korth.) Havil (kratom), kun taas kaksi muuta kasvia, jotka eivät osoittaneet indolialkaloidien esiintymistä, ovat Piper methysticum G. Forst (kava) ja Valeriana officinalis L., ansaitsevat erityistä huomiota. Näistä kasveista eristettyjen yhdisteiden kemiallista rakennetta voidaan käyttää uusien lääkkeiden kehittämisen perustana.
Passiflora incarnata ja muut lajit, kuten P. alata Curtis, P. coerulea L. ja P. edulis Sims, ovat laajalti käytössä rauhoittavina lääkkeinä perinteisessä lääketieteessä useimmissa Euroopan maissa ja Amerikassa (Houghton ja Seth, 2003). Bentsodiatsepiinilääkkeiden rakenne koostuu bentseenirenkaasta, joka on fuusioitunut diatsepiinijärjestelmään, joka koostuu seitsenjäsenisestä heterosyklisestä osasta, jossa on kaksi typpiatomia renkaan paikoissa 1 ja 2. P. incarnatasta eristetyt indolialkaloidit eli harman, harmoli, harmiini, harmaloli ja harmaliini koostuvat bentseenirenkaasta, joka on fuusioitunut viisijäseniseen heterosykliin, joka sisältää yhden typpiatomin.
Monet tutkimukset ovat osoittaneet, että P. incarnatalla on samanlainen farmakologinen profiili kuin bentsodiatsepiineillä ja että se toimii gamma-aminovoihappo (GABA) -reseptoreiden välityksellä (Jawna-Zboiñska et al., 2016). M. speciosan lehtiä on käytetty perinteisenä lääkkeenä ripulin ja diabeteksen hoitoon sekä verenkierron parantamiseen (Vicknasingam et al., 2010). Mitragyniini on tärkein M. speciosassa esiintyvä indolialkaloidi ja sen analogit, speciogyniini, paynantheiini ja speciociliatiini (León et al., 2009). Kaksi tutkimusta, jotka tehtiin M. speciosan vesiuutteella ja alkaloidiuutteella, aiheuttivat masennuslääkkeen kaltaisen vaikutuksen käyttäytymisen epätoivon hiirimalleissa (Kumarnsit et al., 2007). Idayun ym. (2011) mitragyniinillä tekemä tutkimus osoittaa masennuslääkkeen vaikutuksen masennuksen käyttäytymismallissa eläimillä vuorovaikutuksen kautta hypotalamus-aivolisäke-lisämunuais-lisämunuais-akselin (HPA-akselin) kanssa neuroendokriinisessä järjestelmässä (Idayu ym., 2011).
Piper methysticum G. Forstia kulutetaan kava-nimisenä juomana, joka aiheuttaa miellyttävän henkisen olotilan kohti pirteyttä vähentäen väsymystä ja ahdistuneisuutta (Bilia ym., 2002). Tutkimus osoittaa, että suurin osa farmakologisista vaikutuksista säilyy lipidiliukoisessa uutteessa verrattuna vesiuutteeseen. Rasvaliukoinen uute sisältää ainakin seitsemän pyronia, jotka tunnetaan nimellä kavalaktoni. Kavalaktonit ovat yleensä vuorovaikutuksessa dopaminergisten, serotoniini-, gamma-aminovoihappo- (GABA) ja glutamatergisten neurotransmissioiden kanssa, estävät monoamiinioksidaasi B:tä (MOB) ja tarjoavat myös erilaisia vaikutuksia ionikanaviin (Grunze et al., 2001). Dihydrometystisiini on yksi kava-kasvin kuudesta tärkeimmästä kavalaktonista. Dihydrometystisiinin rakenne käsittää aryleeni-α-pyronin, joka on sitoutunut indolin kaltaiseen osaan, jossa on kaksi happigeeniä nitrogeenien sijasta. Se edistää anksiolyyttistä aktiivisuutta ja toimii masennuslääkkeinä. Kaksoissokkoutetut plasebokontrolloidut tutkimukset osoittivat, että kavalaktonit vaikuttavat anksiolyyttisesti ilman, että ne masentavat psyykkisiä ja motorisia toimintoja, ja parantavat unen laatua. Kavalaktonit ovat vaihtoehto korvaamaan bentsodiatsepiinien käyttöä masennuksen hoidossa (Malsch ja Kieser, 2001).
Valeriana officinalis L., joka tunnetaan myös nimellä valerian, on laajalti käytössä monissa maissa rauhoittavana, kouristuslääkkeenä, hypnoottisten vaikutusten ja anksiolyyttisen aktiivisuuden vuoksi (Ghaderi ja Jafari, 2014). Valeriinihappoa ja valepotriaatteja on raportoitu vaikuttavina aineina farmaseuttisissa valmisteissa, ja valerianin kaupallisilla raakauutteilla on kirjattu käyttöä monissa maissa (Bos et al., 2002). Valepotriaatteja, jotka koostuvat polyhydroksisyklopenta-(c)-pyraanien triestereistä karboksyylihappojen kanssa: etikkahappo, valeriinihappo, isovaleriinihappo, α-isovaleriinihappo, β-isovaleriinihappo, β-metyylivaleriinihappo, β-asetoksi-isovaleriinihappo, β-hydroksi-isovaleriinihappo ja β-asetoksiβ-metyylivaleriinihappo, käytetään rauhoittavina. Valepotriaatit ovat epästabiileja, lämpökestäviä ja hajoavat nopeasti happamissa tai emäksisissä olosuhteissa vedessä sekä alkoholiliuoksissa (Bos et al., 2002). Valepotriaatit ovat käyttökelpoisia eläinten ja ihmisten olojen parantamisessa bentsodiatsepiinien vieroitusoireiden aikana (Poyares et al., 2002).
Vaikkakin erilaisia kemiallisia ainesosia on useita, vaikutusmekanismiksi on raportoitu valerianin vuorovaikutus aivojen GABA-järjestelmän kanssa estämällä GABA-transaminaasia, vuorovaikutus GABA-reseptorin/bentsodiatsepiinin kanssa ja häiriö GABA:n imeytymisessä ja sisäänoton rekrytoinnissa synaptosomeihin (Sichardt ym., 2007). Kasvien masennuslääkkeellisten vaikutusten tutkimisessa on hyödynnetty erilaisia malleja. Farmakodynaamisia malleja ovat in vitro, in vivo ja kliiniset mallit, joita hyödynnettiin vaikutusten arvioimiseksi (taulukko 1). Suurin osa tarkastelluista valituista kasvilajeista tutkittiin in vivo -tasolla, muutama tutkimus in vitro, ja vain kava oli käynyt läpi kliinisiä tutkimuksia. Kaikissa tapauksissa on tehtävä lisätutkimuksia, jotta voidaan selvittää aktiiviset yhdisteet, tehokkain annos ja määrittää, vaihteleeko tämä eri masennustyyppien välillä.

TAULUKKO 1. JOHDANTO. Tiedot tarkasteltujen kasvien farmakologisista tutkimuksista.
Indolialkaloidit
Indolialkaloideilla on bisyklinen rakenne, joka koostuu kuusirenkaisesta bentseenirenkaasta, joka on fuusioitunut viisirenkaiseen typpeä sisältävään pyrrolirenkaaseen. Tämä typpiatomilla varustettu pyrrolirengas synnyttää indolialkaloidien perusominaisuudet, jotka tekevät niistä erityisen farmakologisesti aktiivisia (El-Sayed ja Verpoorte, 2007). Indolialkaloideja esiintyy laajalti Apocynaceae-, Loganiaceae-, Rubiaceae- ja Nyssaceae-sukuihin kuuluvissa kasveissa. Tärkeitä kasveista eristettyjä indolialkaloideja ovat muun muassa Rauvolfia serpentina -kasvista saatu verenpainelääke reserpiini (Sagi et al., 2016) ja Catharanthus roseus -kasvista saadut voimakkaat kasvainlääkkeet vinblastiini ja vinkristiini (El-Sayed ja Verpoorte, 2007). Tutkimukset indolialkaloidien tehokkuudesta masennuksen hoidossa eivät ole uusia, ja niitä on tehty vuodesta 1952 lähtien, mutta tällä hetkellä tiedeyhteisö on kiinnittänyt hyvin vähän huomiota masennuslääkkeellisillä ominaisuuksilla varustettujen kasvien terapeuttisen käyttökelpoisuuden hyötyihin.
Indolialkaloidit liitetään usein G-proteiinireseptoreiden toimintaan, erityisesti neuronaaliseen signaalinsiirtoon serotoniinireseptoreiden (5-HT/hydroksitryptamiini) kautta. Vapaan N-H:n kautta tapahtuvan vedynluovuttajan lisäksi π-elektronitiheys vaikuttaa osaltaan planaarisen indolirungon korkeimmin miehitetyn molekyyliorbitaalin (HOMO) energiaan. Tämä mahdollistaa vuorovaikutuksen nukleobaasien, erityisesti protonoidun atomin sekä kohdeproteiinien kanssa (de Sa et al., 2009). Neurotransmitterin serotoniinin kemiallinen rakenne perustuu elektronirikkaaseen aromaattiseen indolirenkaaseen. Typpiatomin läsnäolo indolirenkaassa ylläpitää aromaattista järjestelmää ja tekee sitovasta N-H:sta happaman pikemminkin kuin typen emäksisen. Indolirengas pystyy muodostamaan vetysidoksia N-H-osan kautta ja π-π- pinoutumista tai kationi-π-vuorovaikutuksia aromaattisen osan kautta (Shimazaki et al., 2009). Indolirenkaiden hydrofobisuus on lähes sama kuin fenyylialayksikön ja vähemmän hydrofobinen kuin klassisen isosterisen bentsotiofeeni- ja bentsofuraanirenkaan. N-H-indoliryhmällä on ratkaiseva rooli vuorovaikutuksessa kohteen bioreseptorin kanssa, kun taas syntetisoidut bentsotiofeni- ja bentsofuraanijohdannaiset osoittavat kohtalaista tai rajallista affiniteettia kohteen bioreseptoria kohtaan (de Sa et al., 2009). Reserpiini on yksi esimerkki viimeisten 60 vuoden aikana eristetyistä indolialkaloideista, joilla on rauhoittava vaikutus keskushermostoon. Muuten kaksi aivoissa esiintyvää kemikaalia, nimittäin tryptamiini ja serotoniini, ovat myös indolialkaloidijohdannaisia.
Nykyisin on vielä epäselvää, mitkä kasviuutteiden aktiiviset ainesosat ovat vastuussa masennuslääkkeen vaikutuksesta. Näin ollen pyrimme tunnistamaan muutamia tärkeitä kemiallisia rakenteita, jotka on eristetty kasviuutteista, joilla on masennuslääkkeellistä vaikutusta, ja selvittämään luurankomallin samankaltaisuuden, joka saattaa vaikuttaa masennuslääkkeelliseen aktiivisuuteen. Serotoniinin ja indolialkaloidien välisiä rakenteellisia yhtäläisyyksiä on yritetty jo varhain tunnistaa. Selvin samankaltaisuus koostuu kuusijäsenisistä heterosyklisistä renkaista, jotka ovat fuusioituneet viisijäsenisiin renkaisiin. Erona on typpiatomin läsnäolo tai π-elektronien jakautuminen (kuva 1). Rakenne-aktiivisuussuhdetutkimuksen avulla Nichols (2012) raportoi, että erityyppisten molekyylien aktiivisuuden vaihtelu viittaa siihen, että reseptori on hyvin herkkä tryptamiinin luonteelle. Muut masennuslääkekasveista menestyksekkäästi eristetyt kemialliset yhdisteet mainitaan tässä katsauksessa, koska ne ovat ehkä spesifisiä agonisteja, joilla on erityisiä substituutiomalleja, jotka pystyvät valikoivasti aktivoimaan osajoukon efektoreista. Tätä ilmiötä kutsutaan nykyään toiminnalliseksi selektiivisyydeksi.
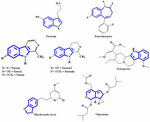
KUVIO 1. Toiminnallinen selektiivisyys. Serotoniinin, bentsodiatsepiinin ja masennuslääkekasveista eristettyjen yhdisteiden kemialliset rakenteet. Samankaltaisuus luurankomallissa, joka koostuu kuusijäsenisistä heterosyklisistä renkaista, joihin on kiinnittynyt viisijäsenisiä renkaita.
Serotoniinia, käytetään laajalti aivojen toiminnassa ja kognitiossa endogeenisena reseptoriagonistina (Fink ja Göthert, 2007). Serotoniini harjoittaa toimintojaan seitsemän reseptoriperheen (5-HT1-5-HT7) kautta, jotka ovat G-proteiinikytkentäisten reseptorien perheen jäseniä. Useiden indoliosaa sisältävien yhdisteiden on kuvattu omaavan affiniteetin eri serotoniinireseptoreihin (Kochanowska-Karamyan ja Hamann, 2010). Indolialkaloidien (eksogeenisten agonistien) rakenteellinen samankaltaisuus endogeenisten välittäjäaineiden, kuten serotoniinin, kanssa on saanut tutkijat ennustamaan näiden molekyylien mahdollista neurologista aktiivisuutta. Kaavio eksogeenisten agonistien neurotransmissioon liittyvistä prosesseista on kuvattu kuvassa 2.
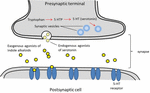
KUVA 2. Eksogeenisten agonistien neurotransmissioon liittyvät prosessit. Kaavio neurotransmissioon liittyvistä prosesseista. Eksogeeniset agonistit kasveista peräisin olevat indolialkaloidit, joilla on rakenteellisia yhtäläisyyksiä serotoniinin kanssa, minkä ansiosta ne voivat sitoutua serotoniinireseptoreihin (5-HT-reseptoreihin).
Indolirengas tunnetaan myös nimellä bioisostereenit, ja sillä on samankaltaisia kemiallisia ja fysikaalisia ominaisuuksia kuin biologisilla molekyyleillä. Tätä samankaltaisuutta käytetään prototyyppilääkkeen kehittämisessä, jolla pyritään parantamaan farmakologista aktiivisuutta ja optimoimaan farmakokineettinen profiili. Toisessa tutkimuksessa bentsofuraanien ja tienopyrrolin farmakologinen arviointi johti bioisosterisiin molekyyleihin, joilla on dimetyylitryptamiinin kaltainen aktiivisuus. Varhainen työ bentsotiofeenien ja 3-indenalkyyliamiinien kanssa osoitti, että yhdisteiden, joista puuttuu rengassubstituentteja, kyky toimia agonisteina rotan funduksessa oli suunnilleen sama kuin tryptamiinien. Tulokset osoittivat, että indoli-NH ei ollut välttämätön 5-HT2-reseptorin aktivoimiseksi rotan funduksessa (Nichols, 2012). Sarja 2-aryyli-indoli NK1-reseptoriantagonisteja ja niiden johdannaisia ovat hyviä ligandeja, mutta niiden oraalinen biologinen hyötyosuus rotilla on alhainen. Liukoisuuden ja imeytymisen lisäämiseksi lisättiin emäksinen typpi, mikä johti analogiseen atsaindoliin ja siihen liittyviin yhdisteisiin, joilla on sama NK1-sitoutumisaffiniteetti kuin 2-aryyli-indoli NK1-reseptoriantagonistien sarjalla (Cooper et al., 2001). Kahden fenyyli-indoli-johdannaisen ligandien molekulaarinen telakointi serotoniinin 5-HT6- ja melanokortiini-4-reseptoreiden kanssa osoittaa, että etuoikeutettu teline voi mukautua riippuen luonteeltaan konservoituneesta alataskusta ja ei-konservoituneesta sitoutumistaskusta. Sitoutumistaskun ei-konservoituneiden osien vuorovaikutukset ovat vastuussa tärkeistä eroista molekyylitunnistuksessa vastaavan kohdereseptorin toimesta (Bondensgaard et al., 2004).
De Sa et al. (2009) mukaan yleisiä luonnollisista lähteistä löytyviä indolialkaloideja ovat ihmisen ravitsemuksessa esiintyvät tryptofaaniaminohapot ja sellaisten kasvihormonien löytäminen, joilla on terapeuttisia vaikutuksia, kuten tulehduskipulääkkeitä, fosfodiesteraasin estäjä, 5-HT-reseptoriagonistit ja -antagonistit, kannabinoidireseptoriagonistit ja HMG-CoA-reduktaasin estäjät. Indolirakenteella on sitoutumistaskuja, ja sillä on yhteinen komplementaarinen sitoutumisalue kohdereseptorin kanssa, joka kuuluu GPCR-luokkaan (G-proteiinien tärkeät kalvoreseptorit kytkettyinä). Useimmat markkinoilla olevat lääkkeet sisältävät indolialarakennetta. Näihin kuuluvat indometasiini, ergotamiini, frovatriptaani, ondansetroni ja tadalafiili.
Johtopäätös
Tässä katsauksessa todettiin, että suurin osa psykiatristen vaivojen hoitoon ilmoitetuista kasviperäisistä lääkkeistä oli raakoja tai puolipuhtaita. In vivo- ja in vitro -tulokset vaihtelevat, eivätkä ne olleet toistettavissa, koska eri biogeografisilla alueilla kasvien sekundaaristen metaboliittien pitoisuus korreloi ravinteiden saatavuuden, ilmaston ja ekologisten olosuhteiden kanssa. Lisäksi kasvien bioaktiivisuus voi johtua yksittäisestä yhdisteestä tai yhdisteiden seoksesta. Kirjoittajat ehdottavat, että ponnisteluja aktiivisten periaatteiden saamiseksi, fytokemikaalien tunnistamiseksi ja metabolomiikan tutkimiseksi olisi suoritettava tarkastuksia in vitro ja in vivo kasvipohjaisten lääkkeiden paremman luonnehdinnan varmistamiseksi. Useimmissa tapauksissa indolialkaloidien synteesiä innoittivat luonnossa esiintyvät molekyylit ja niiden samankaltaisuus serotoniinin kanssa.
Kasvilähteistä peräisin olevat indolialkaloidit ovat melko monimutkaisia verrattuna synteettisiin. Synteettisten indolialkaloidien merkitys on jo todettu, koska rakenne on saatavilla erilaisissa ligandireseptoreissa, entsyymi-inhibiittoreissa ja modulaattoreissa bioreseptoreissa. Joitakin luonnossa esiintyviä indolialkaloideja ei voida syntetisoida nykyisin tunnetuilla menetelmillä. Lisäksi suurin osa indolialkaloidien tehokkuutta koskevista tiedoista on raportoitu synteettisistä indolialkaloideista. Tämän seurauksena monien luonnossa esiintyvien indolialkaloidien potentiaalia uusina lääkeaineina erilaisiin psykiatrisiin häiriöihin ei ole vielä hyödynnetty. Historiallisesti kasviperäiset yhdisteet ovat olleet lähteenä useille menestyksekkäimmille lääkejohdoille tai lääkkeille, joita on käytetty lääketieteessä. Tämä on osoitus siitä, että lisää voisi olla löydettävänä.
Johtopäätöksenä voidaan todeta, että useita indolialkaloideja on käytetty masennuslääkkeinä tai ne tarjoavat johtorakenteita sen kehittämiseen. Havaintojemme perusteella kasvit sisältävät indolialkaloidien varannon, jotka ovat arvokkaita lähtökohtia tulevien masennuslääkkeiden kehittämiseksi.
Author Contributions
HH: Käsikirjoituksen valmistelu. MY: Englannin kielen muokkaaminen ja ehdottaa joitakin tärkeitä tietoja käsikirjoituksen parantamiseksi. AR: Contribute for understanding the schematic of processes associated with neurotransmission.
Funding
Tukea tähän työhön antoi Universiti Malaysia Pahang tutkimusapurahan UMP RDU170302 kautta HH:lle.
Conflict of Interest Statement
Tekijät ilmoittavat, että tutkimus tehtiin ilman kaupallisia tai taloudellisia suhteita, jotka voitaisiin tulkita mahdolliseksi eturistiriidaksi.
Bilia, A. R., Gallori, S. ja Vincieri, F. F. (2002). Kava-kava ja ahdistus: kasvava tieto tehosta ja turvallisuudesta. Life Sci. 70, 2581-2597. doi: 10.1016/S0024-3205(02)01555-2
PubMed Abstract | CrossRef Full Text | Google Scholar
Binfaré, R. W., Rosa, A. O., Lobato, K. R., Santos, A. R. ja Rodrigues, A. L. S. (2009). Askorbiinihapon antaminen tuottaa masennuslääkkeen kaltaisen vaikutuksen: näyttöä monoaminergisen neurotransmission osallistumisesta. Prog. Neuropsychopharmacol. Biol. Psychiatry 33, 530-540. doi: 10.1016/j.pnpbp.2009.02.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Bondensgaard, K., Ankersen, M., Thøgersen, H., Hansen, B. S., Wulff, B. S. ja Bywater, R. P. (2004). G-proteiinikytkentäisten reseptorien etuoikeutettujen rakenteiden tunnistaminen. J. Med. Chem. 47, 888-899. doi: 10.1021/jm0309452
PubMed Abstract | CrossRef Full Text | Google Scholar
Bos, R., Woerdenbag, H. J. ja Pras, N. (2002). Valepotriaattien määrittäminen. J. Chromatogr. A 967, 131-146. doi: 10.1016/S0021-9673(02)00036-5
CrossRef Full Text | Google Scholar
Calixto, J. B., Beirith, A., Ferreira, J., Santos, A. R. ja Yunes, R. A. (2000). Luonnossa esiintyvät antinociceptiiviset aineet kasveista. Phytother. Res. 14, 401-418. doi: 10.1002/1099-1573(200009)14:6<401::AID-PTR762>3.0.CO;2-H
PubMed Abstract | CrossRef Full Text | Google Scholar
Carlini, E. (2003). Kasvit ja keskushermosto. Pharmacol. Biochem. Behav. 75, 501-512. doi: 10.1016/S0091-3057(03)00112-6
CrossRef Full Text | Google Scholar
Cooper, L. C., Chicchi, G. G., Dinnell, K., Elliott, J. M., Hollingworth, G. J., Kurtz, M. M., et al. (2001). 2-Aryl-indoli NK 1 -reseptoriantagonistit: indolisubstituution optimointi. Bioorg. Med. Chem. Lett. 11, 1233-1236. doi: 10.1016/S0960-894X(01)00182-2
CrossRef Full Text | Google Scholar
de Sa, A., Fernando, R., Barreiro, E. J., Fraga, M. ja Alberto, C. (2009). Luonnosta lääkekeksintöihin: indolirunko ”etuoikeutettuna rakenteena”. Mini Rev. Med. Chem. 9, 782-793. doi: 10.2174/138955709788452649
CrossRef Full Text | Google Scholar
El-Sayed, M., ja Verpoorte, R. (2007). Catharanthus terpenoidi indolialkaloidit: biosynteesi ja säätely. Phytochem. Rev. 6, 277-305. doi: 10.1007/s11101-006-9047-8
CrossRef Full Text | Google Scholar
Fajemiroye, J. O., Silva, D. M., Oliveira, D. R., and Costa, E. A. (2016). Ahdistuksen ja masennuksen hoito: lääkekasvit takautuvasti. Fundam. Clin. Pharmacol. 30, 198-215. doi: 10.1111/fcp.12186
PubMed Abstract | CrossRef Full Text | Google Scholar
Fiebich, B. L., Knörle, R., Appel, K., Kammler, T. ja Weiss, G. (2011). Farmakologiset tutkimukset mäkikuisman (Hypericum perforatum) ja passionkukan (Passiflora incarnata) kasviperäisellä lääkeyhdistelmällä: in vitro- ja in vivo -näyttö Hypericumin ja Passifloran synergiasta masennuslääkkeiden farmakologisissa malleissa. Fitoterapia 82, 474-480. doi: 10.1016/j.fitote.2010.12.006
PubMed Abstract | CrossRef Full Text | Google Scholar
Fink, K. B., ja Göthert, M. (2007). Neurotransmitterien vapautumisen 5-HT-reseptorin säätely. Pharmacol. Rev. 59, 360-417. doi: 10.1124/pr.59.07103
CrossRef Full Text | Google Scholar
Ghaderi, N., and Jafari, M. (2014). Tehokas kasvien uudistaminen, geneettinen uskollisuus ja kahden farmaseuttisen yhdisteen korkeatasoinen kertyminen Valeriana officinalis L. S. Afrin uudistetuissa kasveissa. J. Bot. 92, 19-27. doi: 10.1016/j.sajb.2014.01.010
CrossRef Full Text | Google Scholar
Grunze, H., Langosch, J., Schirrmacher, K., Bingmann, D., Von Wegerer, J. ja Walden, J. (2001). Kava-pyronit vaikuttavat hermosolujen siirtoon ja transmembraanisiin kationivirtoihin samalla tavalla kuin vakiintuneet mielialan stabilisaattorit – katsaus. Prog. Neuropsychopharmacol. Biol. Psychiatry 25, 1555-1570.
Google Scholar
Guan, L.-P., and Liu, B.-Y. (2016). Flavonoidien ja niihin liittyvien analogien masennuslääkkeiden kaltaiset vaikutukset ja mekanismit. Eur. J. Med. Chem. 121, 47-57. doi: 10.1016/j.ejmech.2016.05.026
PubMed Abstract | CrossRef Full Text | Google Scholar
Hattesohl, M., Feistel, B., Sievers, H., Lehnfeld, R., Hegger, M. ja Winterhoff, H. (2008). Valeriana officinalis L. sl -uutteilla on anksiolyyttisiä ja masennuslääkkeellisiä vaikutuksia, mutta ei rauhoittavia eikä myorelaksanttisia ominaisuuksia. Phytomedicine 15, 2-15. doi: 10.1016/j.phymed.2007.11.027
PubMed Abstract | CrossRef Full Text | Google Scholar
Houghton, P. J., ja Seth, P. (2003). Kasvit ja keskushermosto. Pharmacol. Biochem. Behav. 75, 497-499. doi: 10.1016/S0091-3057(03)00161-8
CrossRef Full Text | Google Scholar
Idayu, N. F., Hidayat, M. T., Moklas, M., Sharida, F., Raudzah, A. N., Shamima, A., et al. (2011). Mitragyna speciosa Korthista eristetyn mitragyniinin masennuslääkkeen kaltainen vaikutus hiirten masennusmallissa. Phytomedicine 18, 402-407. doi: 10.1016/j.phymed.2010.08.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Jawna-Zboiñska, K., Blecharz-Klin, K., Joniec-Maciejak, I., Wawer, A., Pyrzanowska, J., Piechal, A., et al. (2016). Passiflora incarnata L. parantaa avaruudellista muistia, vähentää stressiä ja vaikuttaa neurotransmissioon rotilla. Phytother. Res. 30, 781-789. doi: 10.1002/ptr.5578
PubMed Abstract | CrossRef Full Text | Google Scholar
Kochanowska-Karamyan, A. J., ja Hamann, M. T. (2010). Merelliset indolialkaloidit: potentiaaliset uudet lääkejohdot masennuksen ja ahdistuksen hallintaan. Chem. Rev. 110, 4489-4497. doi: 10.1021/cr900211p
PubMed Abstract | CrossRef Full Text | Google Scholar
Kumarnsit, E., Vongvatcharanon, U., Keawpradub, N. ja Intasaro, P. (2007). Mitragyna speciosan alkaloidiuutteen indusoima Fos:n kaltainen immunoreaktiivisuus rotan dorsaalisissa raphe-ytimissä. Neurosci. Lett. 416, 128-132. doi: 10.1016/j.neulet.2007.01.061
PubMed Abstract | CrossRef Full Text | Google Scholar
León, F., Habib, E., Adkins, J. E., Furr, E. B., McCurdy, C. R. ja Cutler, S. J. (2009). Yhdysvalloissa kasvatetun Mitragyna speciosan lehtien fytokemiallinen karakterisointi. Nat. Prod. Commun. 4, 907-910.
PubMed Abstract | Google Scholar
Malsch, U., and Kieser, M. (2001). Kava-kavan teho ei-psykoottisen ahdistuksen hoidossa bentsodiatsepiinien esikäsittelyn jälkeen. Psychopharmacology 157, 277-283. doi: 10.1007/s002130100792
PubMed Abstract | CrossRef Full Text
McCarthy, A., Wafford, K., Shanks, E., Ligocki, M., Edgar, D. M. ja Dijk, D.-J. (2016). REM-unen homeostaasi REM-unen puuttuessa: Masennuslääkkeiden vaikutukset. Neuropharmacology 108, 415-425. doi: 10.1016/j.neuropharm.2016.04.047
PubMed Abstract | CrossRef Full Text | Google Scholar
Namola, V., Ratan, P., and Kothiyal, P. (2015). Meren biomateriaalien masennus ja rooli: katsaus. Eur. J. Biomed. Pharm. Sci. 2, 137-148.
Nichols, D. E. (2012). Serotoniinin 5-HT 2A -agonistien rakenne-aktiivisuussuhteet. WIREs Membr. Transp. Signaling 1, 559-579. doi: 10.1002/wmts.42
CrossRef Full Text | Google Scholar
Organisaatio, W. H. (2017). Depression Fact Sheet 2016. Saatavilla osoitteessa: http://www.who.int/mediacentre/factsheets/fs369/en/
Google Scholar
Poyares, D. R., Guilleminault, C., Ohayon, M. M., and Tufik, S. (2002). Voiko valerian parantaa unettomien unta bentsodiatsepiinien vieroituksen jälkeen? Prog. Neuropsychopharmacol. Biol. Psychiatry 26, 539-545.
PubMed Abstract | Google Scholar
Sagi, S., Avula, B., Wang, Y.-H., and Khan, I. A. (2016). Rauwolfia serpentinan juurista peräisin olevien alkaloidien kvantifiointi ja karakterisointi ultra-high performance liquid chromatography-photo diode array-mass spectrometry -menetelmällä. Anal. Bioanal. Chem. 408, 177-190. doi: 10.1007/s00216-015-9093-4
PubMed Abstract | CrossRef Full Text | Google Scholar
Sarris, J., Kavanagh, D., Byrne, G., Bone, K., Adams, J. ja Deed, G. (2009). The Kava Anxiety Depression Spectrum Study (KADSS): satunnaistettu, plasebokontrolloitu ristikkäistutkimus, jossa käytettiin Piper methysticumin vesipohjaista uutetta. Psychopharmacology 205, 399-407. doi: 10.1007/s00213-009-1549-9
PubMed Abstract | CrossRef Full Text | Google Scholar
Shimazaki, Y., Yajima, T., Takani, M., ja Yamauchi, O. (2009). Indolirenkaita sisältävät metallikompleksit: rakenteet ja metalli-indoli-vuorovaikutusten vaikutukset. Coord. Chem. Rev. 253, 479-492. doi: 10.1016/j.ccr.2008.04.012
CrossRef Full Text | Google Scholar
Sichardt, K., Vissiennon, Z., Koetter, U., Brattström, A. ja Nieber, K. (2007). Rotan kortikaalisten neuronien postsynaptisten potentiaalien modulointi eri alkoholeilla maseroitujen valeriaaniuutteiden avulla: adenosiini A1- ja GABAA-reseptorien osallistuminen. Phytother. Res. 21, 932-937. doi: 10.1002/ptr.2197
PubMed Abstract | CrossRef Full Text | Google Scholar
Vicknasingam, B., Narayanan, S., Beng, G. T. ja Mansor, S. M. (2010). Ketumin (Mitragyna speciosa) epävirallinen käyttö opioidivieroitukseen Malesian niemimaan pohjoisissa osavaltioissa ja vaikutukset huumeiden korvaushoitoon. Int. J. Drug Policy 21, 283-288. doi: 10.1016/j.drugpo.2009.12.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Vijeepallam, K., Pandy, V., Kunasegaran, T., Murugan, D. D. ja Naidu, M. (2016). Mitragyna speciosa -lehtiuutteella on antipsykoottinen vaikutus, jolla on potentiaalia lievittää psykoosin positiivisia ja negatiivisia oireita hiirillä. Front. Pharmacol. 7:464. doi: 10.3389/fphar.2016.00464
PubMed Abstract | CrossRef Full Text | Google Scholar
Yi, L.-T., Li, J.-M., Li, Y.-C., Li, Y.-C., Pan, Y., Xu, Q. ja Kong, L.-D. (2008). Sitrushedelmiin liittyvän kemikaalin apigeniinin masennuslääkkeen kaltaiset käyttäytymis- ja neurokemialliset vaikutukset. Life Sci. 82, 741-751. doi: 10.1016/j.lfs.2008.01.007
PubMed Abstract | CrossRef Full Text | Google Scholar