Background
Artemisia annua on kiinalainen lääkekasvi (tunnetaan myös nimellä ”qing hao” tai ”makea koiruoho”), jolla on todistetusti malariaa ehkäisevä vaikutus (1). Maailman terveysjärjestö (WHO) suosittelee artemisiiniinijohdannaisiin perustuvia yhdistelmähoitoja (ACT) komplisoitumattoman malarian hoitoon yhdessä tehokkaiden malarialääkkeiden kanssa (2). Matkailijoiden kemoprofylaksia riippuu malarian endeemisestä matkakohteesta, ja siihen kuuluu atovaakonin/proguaniilin, klorokiinin, doksisykliinin, meflokiinin tai primakiinin yhdistelmä (3, 4). On kuvattu tapauksia, joissa malariainfektio on saanut alkunsa artemisiiniinijohdannaisten kemoprofylaksiasta (5), eikä WHO suosittele A. annua -kasvimateriaalin käyttöä missään muodossa, tee mukaan luettuna, malarian hoitoon tai ennaltaehkäisyyn (6).
Yrtti- ja ravintolisiä (HDS) käytetään yhä enemmän kaikkialla maailmassa, ja HDS:ien aiheuttamat maksavauriot ovat kasvava huolenaihe (7). Huolimatta ACT-lääkkeiden laajamittaisesta käytöstä malariaa endeemisillä alueilla artemisiniinijohdannaisten aiheuttamat maksavauriot ovat harvinaisia (8, 9). Kumar raportoi tapauksesta, jossa potilaalle kehittyi kolestaattinen maksavaurio kuusi viikkoa sen jälkeen, kun hän oli ottanut suun kautta artemisiiniiniä sisältävää kasviperäistä lisäravinetta yleisen terveyden ylläpitämiseksi (10). Artemisia annua -valmisteen aiheuttamaan maksavaurioon liittyy muutamia muita julkaisuja (9, 11-14). Kiinalainen kiinalaisen lääketieteen yhdistys on hiljattain ehdottanut kliinistä ohjeistusta, jonka avulla voidaan arvioida syy-yhteyttä ja tehdä diagnoosi yrttien aiheuttamasta maksavauriosta (15). Esittelemme tapauksen akuutista kolestaattisesta maksatulehduksesta, joka johtui Artemisia-teen nauttimisesta sytostaattiprofylaksiana Etiopiasta palaavalla potilaalla.
Tapauskuvaus
Sveitsiläisen Baselin yliopistollisen sairaalan päivystyspoliklinikalle esiteltiin 51-vuotias mies, jolla oli ollut huonovointisuutta, vatsavaivoja, kelluvaa keltaista jakkaraa, keltarauhasen keltaisuutta, keltatautia ja sappinokkosihappomyrkytystä, joiden kesto oli kestänyt 4 päivää, ja joka oli menettänyt 6-8 kiloa painostaan viimeisten kuuden viikon aikana. Hän oli palannut 4 viikon matkalta Etiopiasta 3 viikkoa ennen hoitoon hakeutumista. Etiopiassa ollessaan hän nautti päivittäin 1,25 g Artemisia annua -jauheteetä malarian sytostaattiprofylaksiana. Noin 90 prosentissa tapauksista hän laimensi jauheen kiehuvaan veteen, lopuissa 10 prosentissa jauhe nautittiin ruokaan sekoitettuna. Lisäravinne oli ostettu Internetin kautta. Potilas antoi meille pakkauksen, jossa oli alun perin ollut 50 g tummanvihreää jauhetta (kuva 1). Esittelyhetkellä säiliössä oli 2 g, mikä osoittaa, että hän oli nauttinut yhteensä 48 g. Etiopiassa oleskelunsa aikana hän oli nauttinut myös muita teen kaltaisia valmisteita. Tietojemme mukaan näihin aineisiin liittyvää maksatoksisuutta ei ole kuvattu. Hän kielsi käyttävänsä muita reseptilääkkeitä, reseptivapaita lääkkeitä tai kasviperäisiä lääkkeitä. Hänellä ei ollut aiemmin tai suvussa maksasairauksia, alkoholin tai huumeiden väärinkäyttöä tai virushepatiitin riskitekijöitä. Hän kertoi, että hänen vaimonsa, joka oli hänen mukanaan Etiopian-matkalla, oli myös käyttänyt Artemesia annua -teetä malariaprofylaksia varten. Hän pysyi koko ajan terveenä.

Kuva 1. Artemisia annua -jauhemainen tee.
Hän oli merkittävää keltaisuutta lukuun ottamatta hyvässä yleiskunnossa, ja hänen elintoimintonsa olivat merkitsemättömät (kuumeeton, verenpaine, syke ja hengitystaajuus normaalit).
Laboratoriokokeet osoittivat: alaniiniaminotransferaasi (ALAT) 91 U/L (normaali, 9-59); aspartaattiaminotransferaasi (ASAT) 42 U/L (normaali, 9-34); emäksinen fosfataasi (ALP) 151 U/L (normaali, 40-130); gammaglutamyylitransferaasi (GGT) 416 U/L (normaali, 12-68); bilirubiini yhteensä 186.6 μmol/l (normaali, 0-24) (konjugoitu bilirubiini 168,5 μmol/l); ja kansainvälinen normalisoitu suhde (INR) 0,9 (normaali, 0,9-1,3). Sappihappotaso oli kohonnut al-tasolle 460,5 μmol/l (normaali, 0-8,0). Verenkuva ja c-reaktiivinen proteiini olivat normaalit. Lievää hyponatremiaa ja hypokloremiaa esiintyi, mikä vastaa potilaan lisääntynyttä veden saantia edellisinä päivinä. Serologiset testit akuutin A-, B-, C- ja E-hepatiitin, Epstein-Barr-viruksen ja sytomegalovirusinfektion varalta olivat negatiiviset. Koeruloplasmiini oli normaali. Maksaspesifiset autovasta-aineet (ydinvasta-aine, neutrofiilivasta-aine, sileän lihaksen vasta-aine, antimitokondriovasta-aine, proteinaasi 3 -vasta-aine ja myeloperoksidaasivasta-aine) olivat negatiivisia, ja IgA-, IgM- ja IgG-arvot olivat normaalialueella. Vatsan ultraäänitutkimus osoitti normaalia maksan parenkyymiä, verisuonia ja sappitiehyitä. Maksan elastografia oli koholla (FibroScan, 12,7 kPa, normaali alue <5 kPa).
Potilas arvioitiin myös Sveitsin trooppisen ja kansanterveyslaitoksessa erilaisten mahdollisten infektioperäisten perussairauksien varalta. Rickettsia-täpläkuumeen vasta-aineet olivat positiivisia, mutta tämän ei katsottu liittyvän kliiniseen taudinkuvaan, eikä antibioottihoitoa aloitettu.
Alustava maksabiopsia osoitti portaalista hepatiittia, johon liittyi sappiteiden lymfosyyttinen infiltraatio ja diffuusi intra-kanalikulaarinen ja sytoplasman sisäinen bilirubinostaasi. Fibroosia tai loismateriaalia ei havaittu (kuvat 2A,B). Perifeerisen veren leukosyyttien DNA:sta tehdyssä seuraavan sukupolven sekvensointianalyysissä perifeerisen veren leukosyyttien DNA:n geneettisten varianttien löytämiseksi geeneistä, jotka koodaavat kolmea tärkeintä sappihappojen homeostaasiin vaikuttavaa maksansiirtäjää, nimittäin BSEP:tä, MDR3:a ja FIC1:tä, ei löytynyt mitään tyypillisesti perinnöllisiin kolestaattisiin maksasairauksiin liitettyjä variantteja.
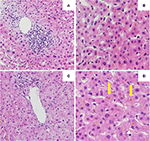
KUVA2. Ensimmäisen (A,B) ja toisen (C,D) maksabiopsian histologia. (A) Matalan tehon näkymä maksabiopsiasta, jossa näkyy portaalinen lymfosyyttinen infiltraatti . (B) Maksaparenchyma, jossa on solunsisäinen bilirubinostaasi (HE, 20x). (C) Matalan tehon näkymä maksabiopsiasta ilman merkittävää portaalitulehdusta (HE, 10x). (D) Maksan parenkyma, jossa on merkittävä solunsisäinen ja solunulkoinen (nuoli) bilirubinostaasi (HE, 20x).
Artemisia-teen toksikologinen analyysi nestekromatografia-massaspektrometrialla ja kaasukromatografia-massaspektrometrialla paljasti seuraavat ainesosat: arteannuin b, deoksiartemisiini, kamferi ja skopoletiini.
Hoito prednisonilla 20 mg kahdesti päivässä ja ursodeoksikolihapolla 500 mg kahdesti päivässä aloitettiin. Jatkuvan keltaisuuden sekä bilirubiinin nousun vuoksi 4 viikon aikana hoidosta huolimatta tehtiin toinen maksabiopsia. Toisessa biopsiassa todettiin vakava intrasytoplasmaattinen sekä intrakanalikulaarinen bilirubinostaasi, ja tulehdus oli vain minimaalinen verrattuna ensimmäiseen biopsiaan (kuvat 2C, D). Kortikosteroidihoito lopetettiin, ursodeoksikolihappoa jatkettiin keltaisuuden häviämiseen ja bilirubiinin (15,3 μmol/l) normalisoitumiseen (kuva 3) sekä sappihappojen merkitykselliseen vähenemiseen (19,5 μmol/l) asti, mikä tapahtui kolme kuukautta taudin puhkeamisen jälkeen.
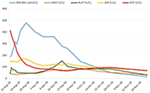
Kuva 3. Sappihappojen väheneminen. Bilirubiinin ja maksaentsyymien kulku ajan kuluessa.
Tapauksesta ilmoitettiin Sveitsin kansallisen lääkevalmisteviranomaisen (Swissmedic) lääkevalvontayksikölle. Osallistujalta saatiin kirjallinen tietoinen suostumus tämän tapausselostuksen julkaisemiseen.
Keskustelu
Artemisiinijohdannaiset ovat malarian hoidon mutta ei kemoterapian kulmakivi (2). Huolimatta niiden laajasta käytöstä artemisiini-derivaattojen maksavaurioita on kuvattu harvoin (8, 10). Tietojemme mukaan tämä on ensimmäinen tapausselostus akuutista kolestaattisesta hepatiitista, joka johtui Artemisia annua -teen nauttimisesta.
Kasvi- ja ravintolisien aiheuttama maksavaurio on kasvavan mielenkiinnon kohteena, koska HDS-valmisteita käytetään yhä enemmän maailmanlaajuisesti (7). HDS:ien nauttimista pidetään usein vaarattomana, mutta niiden käytön yhteydessä on kuitenkin raportoitu yhä useammin haittavaikutuksia (16). Koska HDS:ien pitoisuutta ja koostumusta ei useinkaan ilmoiteta tuoteselosteissa, tuotteen ainesosien laatu ja määrä jäävät tuntemattomiksi. Tapauksessamme diagnoosi Artemisia annua -teen käytöstä johtuvasta HDS:n aiheuttamasta maksavauriosta perustui siihen, että altistumisen ja haittavaikutuksen kehittymisen välillä oli vahva ajallinen yhteys ja että muita mahdollisia syitä ei ollut. Laskimme kausaalisuuden arviointipisteet RUCAM-menetelmän (Roussel Uclaf Causality Assessment Method) (17) mukaisesti ja saimme pistemääräksi 6, joka vastaa ”todennäköistä” syy-yhteyttä epäiltyyn lääkkeeseen. Eri kohdat pisteytettiin seuraavasti: alkamisaika (+2), kulku (+1), riskitekijät (+1), samanaikaiset lääkkeet (-1), muiden maksavaurion syiden poissulkeminen (+2), aiemmat tiedot lääkkeen hepatotoksisuudesta (+1), vaste uudelleenkäytölle (0). Muita tunnistettavia maksasairauden etiologioita ei ollut.
Kumarin aiemmin kuvaamassa tapauksessa esiintyi maksavaurion hepatosellulaarinen malli, jota seurasi pitkittynyt kolestaattinen vaihe (10). Potilaallamme ilmeni pääasiassa kolestaattinen maksavaurio 5 viikkoa Artemisia annua -teen ensimmäisen nauttimisen jälkeen. Oletamme, että luonnollinen kulku oli samanlainen kuin Kumarin tapauksessa, mutta että potilaamme sairastui maksavaurion kehittymisen myöhemmässä vaiheessa. Nautitun yrttiteen toksikologisessa analyysissä tunnistimme lisäksi skopoletiinia ja kamferia, joita esiintyy luonnostaan Artemisia annua -teessä (18, 19) ja jotka ovat saattaneet vaikuttaa kolestaattisen maksavaurion puhkeamiseen.
Artemisiinin johdannaisten aiheuttaman maksavaurion mekanismi on edelleen epäselvä. Artemisiae spp:n kemiallisia komponentteja ovat haihtuvat öljyt, flavonoidit, tanniinit, triterpeenit ja polysakkaridit. Artemisiae spp:stä peräisin olevilla haihtuvilla öljyillä on voimakkaita farmakologisia vaikutuksia ja myrkyllisyyttä, ja äskettäisessä bioinformatiikan lähestymistavassa tunnistettiin erilaisia reittejä, jotka voivat olla mukana maksavaurion kehittymisessä (20). Alttius lääkkeiden aiheuttamalle kolestaattiselle maksavauriolle on yhdistetty sappisuolan vientipumpun polymorfismiin (21, 22). Sen vuoksi etsimme sappihaponkuljettajien variantteja seuraavan sukupolven sekvensoinnilla. Emme havainneet deletioita, duplikaatioita tai patologisia variantteja ABCB11-, ATP8B1- ja ABCB4-geenisekvensseissä (koodaavilla ja rinnakkaisilla alueilla), jotka koodaavat BSEP:tä, FIC1:tä ja MDR3:a (kuva 4). Useita yhteisiä sekvenssivariantteja kuitenkin tunnistettiin. Potilaallamme oli homotsygoottisesti ABCB11-geenin variantti . On keskusteltu siitä, liittyykö tämä polymorfismi hyvänlaatuiseen toistuvaan ja/tai etenevään tuttuun maksansisäiseen kolestaasiin ja raskauden aikaiseen maksansisäiseen kolestaasiin (23, 24). Lisäksi toinen ABCB11-geenin yleinen variantti havaittiin heterotsygoottisena . Tämä variantti on yhdistetty vähentyneeseen proteiinin ilmentymiseen (25) ja primaariseen sappikirroosiin (26, 27). Molemmat geenivariantit ovat kuitenkin aivan liian yleisiä väestössä ollakseen syyllisiä kolestaattisiin maksasairauksiin (28). Transkriptomin systemaattinen sekvensointi voi tällaisissa tapauksissa tunnistaa variantteja geenisekvenssien muilla alueilla tai muissa geeneissä, jotka koodaavat muita maksan transportaattoreita tai sapen muodostukseen osallistuvia proteiineja, kuten ABCC2:ta, ABCC3:a, ABCC4:ää ja tiukka liitosproteiini 2:ta (tight junction protein 2, TJP2) (21) (21).
KUVIO 4. Sappinesteen ja sappinesteen muodostukseen osallistuvien proteiinien koodaus. Geenien ABCB11, ABCB4 ja ATP8B1 molekyyligeneettinen analyysi.
Johtopäätöksenä kuvaamme tapauksen, jossa vakava HDS:n aiheuttama kolestaattinen maksavaurio oli yhteensopiva Artemisia annua -teen nauttimisen kanssa. Olisi pyrittävä vähentämään artemisiiniinijohdannaisten käyttöä malarian ehkäisyyn, sillä se on WHO:n suositusten mukaan tehotonta ja voi lisäksi aiheuttaa haittoja. Lisäksi tapaus osoittaa, että ymmärryksemme HDS:n aiheuttaman maksavaurion patofysiologiasta ja alttiudesta on vielä riittämätön.
Tietojen saatavuusilmoitus
Kaikki tämän tutkimuksen tietokokonaisuudet sisältyvät käsikirjoitukseen/täydentäviin tiedostoihin.
Eettiset näkökohdat
Eettistä tarkastusta ja hyväksyntää ei vaadittu tässä raportoitavaan yksittäiseen kliiniseen tapauskertomukseen paikallisen lainsäädännön ja laitosvaatimusten mukaisesti. Potilas/osallistuja antoi kirjallisen tietoon perustuvan suostumuksensa osallistumiseen.
Author Contributions
FR-R kirjoitti käsikirjoituksen ensimmäisen luonnoksen. SH, CB, AL-T, MZ ja AJ kirjoittivat käsikirjoituksen osia. FR-R, SH, SR, MZ, KR, JB, AJ, MH, AL-T, LT ja CB osallistuivat potilaan kliiniseen hoitoon, käsikirjoituksen tarkistamiseen, lukivat ja hyväksyivät toimitetun version.
Interintäristiriita
Tekijät ilmoittavat, että tutkimus suoritettiin ilman kaupallisia tai taloudellisia suhteita, jotka voitaisiin tulkita mahdolliseksi eturistiriidaksi.
1. Klayman DL. Qinghaosu (artemisiniini): malarialääke Kiinasta. Science. (1985) 228:1049-55. doi: 10.1126/science.3887571
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Maailman terveysjärjestö. WHO Guidelines for the Treatment of Malaria, 2. painos. (2010). Saatavilla verkossa osoitteessa: http://www.who.int/malaria/publications/atoz/9789241547925/en/index.html (accessed November 23, 2018).
Google Scholar
3. SafeTravel.ch. Reismedizinische Beratung. Malariavorbeugung (Chemoprophylaxe) (2016). Saatavilla verkossa osoitteessa: http://www.safetravel.ch/safetravel2/servlet/ch.ofac.wv.wv204j.pages.Wv204ConseilsSanteListeCtrl?action=afficheDetail&elementCourant=1 (accessed November 23, 2018).
Google Scholar
4. Google Scholar
. Centers for Disease Control and Prevention. Lääkkeen valinta malarian ehkäisemiseksi (2018). Saatavilla verkossa osoitteessa: https://www.cdc.gov/malaria/travelers/drugs.html
Google Scholar
5. Verkkopalvelussa. Shahinas D, Lau R, Khairnar K, Hancock D, Pillai DR. Artesunaatin väärinkäyttö ja Plasmodium falciparum -malaria Afrikasta palaavilla matkustajilla. Emerg Infect Dis. (2010) 16:1608-10. doi: 10.3201/eid1610.100427
PubMed Tiivistelmä | CrossRef Full Text | Google Scholar
6. Maailman terveysjärjestö. WHO, kannanotto. Effectiveness of Non-Pharmaceutical Forms of Artemisia annua L. Against Malaria. Geneve: World Health Organization (2012).
Google Scholar
7. Navarro VJ, Khan I, Björnsson E, Seeff LB, Serrano J, Hoofnagle JH. Yrtti- ja ravintolisien aiheuttamat maksavauriot. Hepatology. (2017) 65:363-73. doi: 10.1002/hep.28813
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Hepatologinen tutkimus. Guevart E, Aguemon A. Kaksi fulminantin hepatiitin tapausta kuratiivisen artesunaatti-amodiaquin-yhdistelmähoidon aikana. Med Mal Infect. (2009) 39:57-60. doi: 10.1016/j.medmal.2008.09.024
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Centers for Disease Control and Prevention (CDC). Artemisiniinia sisältävään kasviperäiseen lisäravinteeseen ajallisesti liittyvä hepatiitti – Washington, 2008. Morb Mortal Wkly Rep. (2009) 58:854-6.
Google Scholar
10. Kumar S. Kolestaattinen maksavaurio sekundaarisesti artemisiiniinille. Hepatology. (2015) 62:973-4. doi: 10.1002/hep.27900
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Stebbings S, Beattie E, McNamara D, Hunt S. Satunnaistettu, plasebokontrolloitu kliininen pilottitutkimus, jossa tutkitaan 12 viikon ajan annettavan Artemisia annua -uutteen tehoa ja turvallisuutta lonkan ja polven nivelrikkoon liittyvän kivun, jäykkyyden ja toimintarajoitteiden hallinnassa. Clin Rheumatol. (2016) 35:1829-36. doi: 10.1007/s10067-015-3110-z
PubMed Abstract | CrossRef Full Text | Google Scholar
12. JOHTOPÄÄTÖKSET. Medsafe. Arthrem – Mahdollinen maksavaurion vaara -Lausunto vuoden 1981 lääkelain 98 §:n nojalla (2018). Saatavilla verkossa osoitteessa: http://www.medsafe.govt.nz/safety/EWS/2018/Arthrem.asp
Google Scholar
13. Google Scholar
. National Institutes of Health, LiverTox, Clinical and Research Information on Drug-Induced Liver Injury. Artemisiinin johdannaiset. (2019). Saatavilla verkossa osoitteessa: https://livertox.nih.gov/ArtemisininDerivatives.htm
Google Scholar
14. Verkkosivusto. Savage RL, Tatley MV, Barnes J. Hepatotoksisuus luonnollisella ravintolisällä, Artemisia annua L. Extract in Grapeseed Oil. Uuden-Seelannin lääkevalvontakeskuksen raportteja. Drug Safety (2018). In: 18th ISoP Annual Meeting ”Pharmacovigilance without borders”. Geneva (accessed November 11-14, 2018).
Google Scholar
15. Wang JB, Zhu Y, Bai ZF, Wang FS, Li XH, Xiao XH, et al. Guidelines for the Diagnosis and Management of Herb-Induced Liver Injury. Chin J Integr Med. (2018) 24:696-706. doi: 10.1007/s11655-018-3000-8
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Maksa- ja verisuonitautien hoito. Clarke TC, Black LI, Stussman BJ, Barnes PM, Nahin RL. Täydentävien terveyslähestymistapojen käytön suuntaukset aikuisten keskuudessa: Yhdysvallat, 2002-2012. Natl Health Stat Rep. (2015) 79:1-16.
Google Scholar
17. Danan G, Teschke R. RUCAM lääkkeiden ja yrttien aiheuttamissa maksavaurioissa: päivitys. Int J Mol Sci. (2015) 17:E14. doi: 10.3390/ijms17010014
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Zhang X, Zhao Y, Guo L, Qiu Z, Huang L, Qu X. Kiinan eri maantieteellisiltä alueilta peräisin olevan Artemisia annua L:n kemiallisten ainesosien erot. PLoS ONE. (2017) 12:e0183047. doi: 10.1371/journal.pone.0183047
PubMed Abstract | Ristiintaulukoitu kokoteksti | Google Scholar
19. Ristiintaulukoinnin tulokset. Ogwang Engeu P, Omujal F, Agwaya M, Kyakulaga H, Obua C. Variations in antimalarial components of Artemisia annua Linn from three regions of Uganda. Afr Health Sci. (2015) 15:828-34. doi: 10.4314/ahs.v15i3.17
CrossRef Full Text | Google Scholar
20. Afr Health Science. Liu H, Zhan S, Zhang Y, Ma Y, Chen L, Chen L, et al. Molecular network-based analysis of the mechanism of liver injury induced by volatile oils from Artemisiae argyi folium. BMC Complement Altern Med. (2017) 17:491. doi: 10.1186/s12906-017-1997-4
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Ks. esim. Morgan RE, Trauner M, van Staden CJ, Lee PH, Ramachandran B, Eschenberg M, et al. Interferenssi sappisuolan vientipumpun toimintaan on altistava tekijä ihmisen maksavaurioille lääkekehityksessä. Toxicol Sci. (2010) 118:485-500. doi: 10.1093/toxsci/kfq269
PubMed Abstract | CrossRef Full Text | Google Scholar
22. Maksa- ja lääketiede. Kubitz R, Dröge C, Stindt J, Weissenberger K, Häussinger D. The bile sal export pump (BSEP) in health and disease. Clin Res Hepatol Gastroenterol. (2012) 36:536-53. doi: 10.1016/j.clinre.2012.06.006
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Ks. esim. Alissa FT, Jaffe R, Shneider BL. Päivitys progressiivisesta familiaalisesta intrahepaattisesta kolestaasista. J Pediatr Gastroenterol Nutr. (2008) 46:241-52.21. doi: 10.1097/MPG.0b013e3181596060
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Dixon PH, Williamson C. The molecular genetics of intrahepatic cholestasis of pregnancy. Obstet Med. (2008) 1:65-71. doi: 10.1258/om.2008.080010
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Stieger B. Natrium-taurokolaatti-kotransportoivan polypeptidin (NTCP) ja sappisuolan vientipumpun (BSEP) rooli sapen muodostuksen fysiologiassa ja patofysiologiassa. Handb Exp Pharmacol. (2011) 201:205-59. doi: 10.1007/978-3-642-14541-4_5
CrossRef Full Text | Google Scholar
26. Sappitietokanta. Pauli-Magnus C, Kerb R, Fattinger K, Lang T, Anwald B, Kullak-Ublick GA, et al. BSEP- ja MDR3-haplotyyppirakenne terveillä valkoihoisilla, primaarisessa sappikirroosissa ja primaarisessa sklerosoivassa kolangiitissa. Hepatology. (2004) 39:779-91. doi: 10.1002/hep.20159
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Hepatologinen tutkimus. Pan S, Li X, Jiang P, Jiang Y, Shuai L, He Y, et al. ABCB4- ja ABCB11-geenien variaatiot liittyvät primaarisiin maksansisäisiin kiviin. Mol Med Rep. (2015) 11:434-46. doi: 10.3892/mmr.2014.2645
PubMed Abstract | CrossRef Full Text | Google Scholar
28. Dröge C, Bonus M, Baumann U, Klindt C, Lainka E, Kathemann S, et al. FIC1:n, BSEP:n ja MDR3:n sekvensointi suuressa kohortissa potilaita, joilla on kolestaasi, paljasti suuren määrän erilaisia geneettisiä variantteja. J Hepatol. (2017) 67:1253-64. doi: 10.1016/j.jhep.2017.07.004
PubMed Abstract | CrossRef Full Text | Google Scholar