
Molekulaariset dimeerit muodostuvat usein kahden identtisen yhdisteen reaktiossa esim: 2A → A-A. Tässä esimerkissä monomeerin ”A” sanotaan dimeroituvan muodostaen dimeerin ”A-A”. Esimerkki on diaminokarbeeni, joka dimeroituu antaen tetraaminoeteenin:
2 C(NR2)2 → (R2N)2C=C(NR2)2
Karbeenit ovat erittäin reaktiivisia ja muodostavat helposti sidoksia.
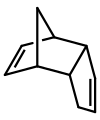
Disyklopentadieeni on epäsymmetrinen dimeeri kahdesta syklopentadieenimolekyylistä, jotka ovat reagoineet Diels-Alderin reaktiossa antaen tuotteen. Kuumennettaessa se ”halkeaa” (käy läpi retro-Diels-Alder-reaktion) antaen identtisiä monomeerejä:
C10H12 → 2 C5H6
Monetalliset alkuaineet esiintyvät dimeereinä: vety, typpi, happi, halogeenit eli fluori, kloori, bromi ja jodi. Jalokaasut voivat muodostaa van der Waalsin sidosten yhdistämiä dimeerejä, esimerkiksi dihelium tai diargon. Elohopea esiintyy elohopea(I)kationina (Hg22+), joka on muodollisesti dimeeri-ioni. Muut metallit voivat muodostaa höyryissään osan dimeereistä. Tunnettuja metallisia dimeerejä ovat Li2, Na2, K2, Rb2 ja Cs2.
Monet pienet orgaaniset molekyylit, erityisesti formaldehydi, muodostavat helposti dimeerejä. Formaldehydin (CH2O) dimeeri on dioksetaani (C2H4O2).