
Los dímeros moleculares se forman a menudo por la reacción de dos compuestos idénticos, por ejemplo: 2A → A-A. En este ejemplo, se dice que el monómero «A» se dimeriza para dar el dímero «A-A». Un ejemplo es un diaminocarbeno, que se dimeriza para dar un tetraaminoetileno:
2 C(NR2)2 → (R2N)2C=C(NR2)2
Los carbenos son muy reactivos y forman fácilmente enlaces.
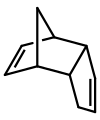
El diciclopentadieno es un dímero asimétrico de dos moléculas de ciclopentadieno que han reaccionado en una reacción de Diels-Alder para dar el producto. Al calentarse, se «agrieta» (experimenta una reacción de Diels-Alder) para dar monómeros idénticos:
C10H12 → 2 C5H6
Muchos elementos no metálicos se presentan como dímeros: hidrógeno, nitrógeno, oxígeno, los halógenos, es decir, flúor, cloro, bromo y yodo. Los gases nobles pueden formar dímeros unidos por enlaces de Van der Waals, por ejemplo el dihelio o el diargón. El mercurio se presenta como un catión de mercurio(I) (Hg22+), formalmente un ion dimérico. Otros metales pueden formar una proporción de dímeros en su vapor. Entre los dímeros metálicos conocidos se encuentran el Li2, el Na2, el K2, el Rb2 y el Cs2.
Muchas moléculas orgánicas pequeñas, sobre todo el formaldehído, forman fácilmente dímeros. El dímero del formaldehído (CH2O) es el dioxetano (C2H4O2).