EINFÜHRUNG
Nur wenige Medikamentengruppen wurden im Laufe der Jahre bei Patienten mit verschiedenen kardiovaskulären Erkrankungen so umfassend untersucht wie die Betablocker (BBs). In den letzten drei Jahrzehnten haben sie das Gebiet der Kardiologie revolutioniert, und es gibt umfangreiche Belege für ihre Wirksamkeit bei den vier häufigsten Gruppen von Herz-Kreislauf-Erkrankungen: Herzinsuffizienz (HF), Bluthochdruck, Herzrhythmusstörungen und ischämische Herzerkrankungen. Gleichzeitig werden immer wieder neue Wirkmechanismen von BBs entdeckt, die dazu beitragen, die Gründe für ihre eindeutigen Vorteile besser zu erklären.1 Diese neuen Entdeckungen erweitern die potenziellen, aber noch nicht identifizierten Anwendungsmöglichkeiten von BBs im klinischen Bereich.
Im Folgenden werden die vorhandenen Belege für den Nutzen von BBs in verschiedenen klinischen Kontexten, die diesen Vorteilen zugrunde liegenden Wirkmechanismen und die aktuellen Empfehlungen vorgestellt.
BETA-BLOCKER BEI HERZSCHWACHSENHEIT
Aufgrund ihrer negativ inotropen Eigenschaften galten BBs bei Patienten mit HF lange Zeit als absolut kontraindiziert. Das Fachgebiet erfuhr eine konzeptionelle Revolution, als man feststellte, dass BBs entgegen der vorherrschenden Weisheit paradoxerweise von Vorteil sein könnten. Im ersten Jahrzehnt des 21. Jahrhunderts wurde nachgewiesen, dass diese Medikamente bei Patienten mit HF äußerst positive Auswirkungen haben. Seitdem sind sie zu einem Eckpfeiler in der Behandlung von HF bei Patienten mit systolischer Dysfunktion (reduzierte linksventrikuläre Auswurffraktion , ≤ 40 %; auch bekannt als reduzierte Auswurffraktion ) geworden. HF muss jedoch in ihrem gesamten Spektrum verstanden werden, von asymptomatischen Patienten, die dennoch ein HF-Risiko haben – Stadium A des American College of Cardiology/American Heart Association (ACC/AHA)2 – bis hin zu symptomatischen Patienten mit unterschiedlichen LVEF-Bereichen und sogar hospitalisierten Patienten oder solchen mit schweren HF-Symptomen.
Herzinsuffizienz mit reduzierter Auswurffraktion
Die Belege zeigen eindeutig, dass BBs das Sterberisiko bei Patienten mit HFrEF verringern. Ihr Einsatz wird in den jüngsten klinischen Praxisleitlinien der Europäischen Gesellschaft für Kardiologie (ESC) weitgehend anerkannt.3 Tabelle 1 zeigt Daten aus den wichtigsten randomisierten Studien4-10, die den Einsatz von BBs unterstützen, sowie ihre Fähigkeit, die wichtigsten Endpunkte zu reduzieren. Obwohl Metoprolol, Bisoprolol und Carvedilol mit signifikanten positiven Effekten assoziiert sind, ist die Assoziation für Bucindolol und Nebivolol nicht so konsistent. In der SENIORS-Studie (Alter > 70 Jahre, 64 % mit rEF) wurde Nebivolol mit einem geringeren Risiko für den zusammengesetzten Endpunkt Tod und kardiovaskuläre Krankenhauseinweisung in Verbindung gebracht, nicht aber für den Tod allein oder die anderen Endpunkte.4 Bucindolol konnte in der BEST-Studie die Sterblichkeit nicht senken, wohl aber die Krankenhauseinweisungen wegen HF.5 Die 3 BBs mit der stärksten Evidenz in dieser Population (Metoprolol, Bisoprolol und Carvedilol) werden mit einer geringeren Krankheitsprogression in Verbindung gebracht, wie die niedrigeren Raten von direkt damit verbundenen Todesfällen (plötzlicher Tod und HF) und HF-Hospitalisierungen in den verschiedenen Studien zeigen.6-8
Design und Ergebnisse der wichtigsten klinischen Studien zu Betablockern bei Herzinsuffizienz
| Studie (j, Patienten) | Medikament, Mittelwert (mg/d) | NYHA | LVEF | Ischämisch | Mittlere Nachbeobachtung, mo | NYHA-Klasse III/IV | NNT1 Leben1 y | Reduzierung des Sterberisikos | Reduzierung des Krankenhausaufenthaltsrisikos | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Gesamt | CV | Plötzlich | Auf Grund von HF | Gesamt | Auf Grund von HF | |||||||||
| CIBIS-II6 (1999, n=2647) | Bisoprolol 7.5 mg/d | III-IV | ≤35% | 50% | 15 | 100% | 23 | 34% | 29% | 44% | 26% | 20% | 36% | |
| MERIT-HF7 (1999, n=3991) | Metoprolol 159 mg/d | II-IV | ≤40% | 65% | 12 | 59% | 27 | 34% | 38% | 41% | 49% | 18% | 35% | |
| US Carvedilol10 (1996, n=1094) | Carvedilol 45 mg/d | II-IV | ≤35% | 48% | 6 | 60% | 15 | 65% | 65% | 55% | 79% | 27% | – | |
| COPERNICUS8 (2002, n=2289) | Carvedilol 37 mg/d | III-IV | 25% | 67% | 10 | 100% | 15 | 35% | – | – | – | 20% | 33% | |
| COMET9 (2003, n=3029) | Carvedilol 42 mg/d vs. Metoprolol 85 mg/d | II-IV | 35% | 51% | 58 | 51% | – | 17% | 20% | > | 3%, NS | |||
| BEST5 (2001, n=2708) | Bucindolol 152 mg/d | III-IV | ≤35% | 59% | 24 | 100% | – | 10%, NS | 14%, NS | 12%, NS | 15%, NS | 8%, NS | 22% | |
| SENIORS4 (2005, n=2128) | Nebivolol 7.7 mg/d | II-IV | * | 68% | 21 | 40% | – | 12%, NS | 16%, NS | – | – | 4%, NS | – | |
CV, Herz-Kreislauf; HF, Herzinsuffizienz; LVEF, linksventrikuläre Auswurffraktion; NNT, number needed to treat; NS, nicht signifikant; NYHA, New York Heart Association.
Alle Studien analysierten Betablocker gegenüber Placebo, außer COMET (Carvedilol gegenüber Metoprolol-Tartrat). Alle Risikoreduktionen sind signifikant, sofern nicht anders angegeben.
Die LVEF war kein Einschlusskriterium, aber 36 % der Patienten hatten eine LVEF> 35 %; die eingeschlossenen Patienten waren älter als 70 Jahre.
Die COMET-Studie, die einzige Studie, in der 2 BBs direkt verglichen wurden – Carvedilol vs. Metoprolol-Tartrat -, ergab eine niedrigere Sterblichkeit mit Carvedilol; allerdings könnte die Verwendung von kurz wirkendem Metoprolol, im Gegensatz zu der in der MERIT-HF-Studie verwendeten Formulierung,7 diese Unterschiede teilweise erklären.9 In einer großen Meta-Analyse, die sich hauptsächlich auf BBs mit nachgewiesenem Überlebensvorteil stützt, wurden keine Unterschiede zwischen den verschiedenen BBs gefunden, die zusammen die 12-Monats-Sterblichkeit um 31 % reduzierten, ohne dass es zu Wechselwirkungen zwischen Behandlung und Untergruppe kam.11Abbildung 1 zeigt die relative Risikoreduktion und die Anzahl der Patienten, die nach 1 Jahr behandelt werden müssen, um die verschiedenen Ereignisse zu reduzieren, basierend auf den Ergebnissen der Meta-Analyse.11
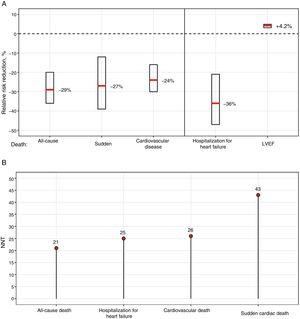
Nutzen von Betablockern bei Patienten mit Herzinsuffizienz und reduzierter LVEF. A: Relative Risikoreduktion und 95%-Konfidenzintervall. B: NNT nach 1 Jahr. LVEF, linksventrikuläre Auswurffraktion; NNT, number needed to treat.
In den letzten Jahren haben sich verschiedene Meta-Analysen mit dem Zusammenhang zwischen dem Nutzen von BBs und der Herzfrequenz bei Patienten mit rEF beschäftigt. Der Zusammenhang zwischen einer höheren Herzfrequenz und einer schlechteren Prognose ist gut belegt. Dennoch zeigte eine Subanalyse der HF-ACTION-Studie, dass der Nutzen bei hohen BB-Dosen größer ist, unabhängig von der Herzfrequenz.12 Andererseits haben andere neuere Metaanalysen darauf hingewiesen, dass der mit der Herzfrequenzsenkung verbundene Nutzen von BBs nur bei Patienten mit Sinusrhythmus erreicht wird oder zumindest bei Patienten mit Vorhofflimmern (AF) geringer ist.13 Eine Subanalyse der AF-CHF-Studie zeigte jedoch, dass BBs auch die Sterblichkeitsrate bei Patienten mit Vorhofflimmern und rEF verbesserten.14
Ein besonderes Problem sind Patienten mit asymptomatischem rEF. Bei diesen Patienten verhindern BBs theoretisch die nachteiligen ventrikulären Umbauprozesse, die das Fortschreiten zu symptomatischer HF fördern. Die REVERT-Studie, die einzige Studie, in der asymptomatische Patienten im Stadium I der New York Heart Association (NYHA) und mit rEF (Stadium B der ACC/AHA) randomisiert wurden,1 zeigte, dass Metoprololsuccinat nach einem Jahr mit einer Verringerung des Volumens und einer Erhöhung der LVEF verbunden war.15 In der CAPRICORN-Studie (LVEF nach Infarkt
40%) wurde eine geringere Progression zu symptomatischen Stadien und eine Verbesserung des Remodeling und der ventrikulären Funktion festgestellt.16 In einer Beobachtungsstudie verringerte der Einsatz von BB die Episoden symptomatischer HF um 60 %.17Herzinsuffizienz mit mittlerer oder erhaltener systolischer Funktion
Prospektive klinische Studien sind rar und haben in der Regel indirekte Endpunkte wie echokardiographische Parameter oder kleine Stichprobengrößen, die lediglich eine Schätzung der Wirkung auf klinische Endpunkte erlauben. Eine Beobachtungsstudie, die auf einer Propensity-Score-Anpassung mit einer großen Population von Krankenhauspatienten beruht, und mehrere Meta-Analysen deuten darauf hin, dass BBs die Sterblichkeit bei Patienten mit einer LVEF > 40 % senken können.18 Kürzlich hat eine Teilstudie der TOPCAT-Studie (LVEF> 45 %) gezeigt, dass BBs, insbesondere bei Patienten ohne vorangegangenen Infarkt, mit einer erhöhten Anzahl unerwünschter kardiovaskulärer Ereignisse verbunden sind.19 Nach der Empfehlung in den neuesten europäischen Leitlinien, Patienten mit mittlerer LVEF (40%-49%) als separate Untergruppe zu betrachten, zeigte eine individuelle Metaanalyse, die die LVEF jedes Patienten in den entscheidenden klinischen Studien einbezog, dass Patienten im Sinusrhythmus in Bezug auf die Sterblichkeit tatsächlich von einer BB-Therapie profitieren könnten.20
Schwerwiegende akute oder dekompensierte Herzinsuffizienz
Bei Patienten, die mit rEF ins Krankenhaus eingeliefert werden, reduziert die Fortsetzung der BB-Therapie während der Aufnahme das Sterberisiko um 40 %, während die Einleitung einer BB-Therapie bei BB-naiven Patienten das Risiko um fast 60 % senkt.21 Im Gegensatz dazu verdoppelt sich die Sterblichkeit bei Absetzen der BB-Therapie während des Krankenhausaufenthalts.22 In der COPERNICUS-Studie wurden Patienten mit schwerer HF (NYHA-Klasse III-IV und LVEF
25 %) untersucht, darunter auch hospitalisierte oder dekompensierte Patienten, die intravenöse Diuretika einnahmen. Der Einsatz von Carvedilol verringerte das Gesamttodesrisiko um 35 %.7 Darüber hinaus erleichterte die Einführung von BB während des Krankenhausaufenthalts die Einhaltung der BB-Therapie während der Nachbeobachtung.23 In einer anderen Subanalyse der MERIT-HF-Studie, die Patienten mit einer stärkeren klinischen Verschlechterung (NYHA-Klasse III-IV und LVEF 25 %) einschloss, war der Nutzen von Metoprolol eindeutig und sogar noch größer.24BETA-BLOCKER BEI HYPERTENSION
Im Vergleich zu Placebo konnten BBs die Gesamtmortalität oder die kardiovaskuläre Mortalität bei Patienten mit unkomplizierter essenzieller Hypertonie nicht senken.25-27 Sie können jedoch kardiovaskuläre Ereignisse, vor allem Schlaganfälle, verringern. Im Vergleich zu Diuretika verringern BBs nicht die Zahl der kardiovaskulären Ereignisse und können sogar mit einer höheren Schlaganfallhäufigkeit in Verbindung gebracht werden.28 Diese hohe Schlaganfallhäufigkeit scheint mit dem Alter zusammenzuhängen, das das Risiko von BBs bei über 60-Jährigen erhöht.29 Im Vergleich zu Kalziumantagonisten oder Angiotensin-Converting-Enzym-Hemmern/Angiotensin-Rezeptor-Blockern sind BBs mit einem erhöhten Schlaganfallrisiko verbunden.26,27 Die Ergebnisse des Einsatzes von BBs als First-Line-Medikamente bei der Behandlung von Bluthochdruck im Vergleich zu anderen Medikamentengruppen sind in Abbildung 2 dargestellt.
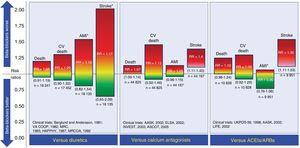
Vergleich von Betablockern mit anderen Medikamenten, die als First-Line-Strategie zur Behandlung der essentiellen Hypertonie eingesetzt werden. Die Risikoverhältnisse sind zusammen mit ihren 95%-Konfidenzintervallen (in Klammern) dargestellt. ACEI, Angiotensin-konvertierende Enzyminhibitoren; AMI, akuter Myokardinfarkt; ARB, Angiotensin-II-Rezeptorblocker; CV, kardiovaskulär; RR, Risikoverhältnis. *Ereignisse, deren Risikoverhältnis und entsprechendes Konfidenzintervall nach den Evidenzgradklassifikationen der GRADE-Arbeitsgruppe ein niedriges Maß an Sicherheit aufweisen. Die Informationen basieren auf der Meta-Analyse von Wiysonge et al.27
Da es sich bei BBs um eine heterogene Gruppe von Medikamenten handelt, sind Schlussfolgerungen aus Meta-Analysen generell mit Vorsicht zu genießen. Tabelle 2 zeigt die Ergebnisse der wichtigsten klinischen Studien, in denen die Rolle der verschiedenen BBs bei der Behandlung von Bluthochdruck untersucht wurde.30-45
Hauptstudien zur Untersuchung von Betablockern bei der Behandlung der essentiellen Hypertonie
| Studie | Population | Beta-Blocker | Vergleich | Ergebnis |
|---|---|---|---|---|
| Berglund und Andersson30 | 47-54 Jahre | Propranolol | Thiazid | Kein Unterschied in der Mortalität |
| VA COOP31 | 21-65 Jahre | Propranolol | Thiazid | Kein Unterschied in der Mortalität, AMI oder Schlaganfall |
| MRC32 | 35-64 Jahre | Propranolol | ThiazidPlacebo | Niedrigeres Schlaganfallrisiko gegenüber Placebo; kein Unterschied bei AMI oder MortalitätErhöhtes Schlaganfallrisiko gegenüber Thiazid |
| Coope und Warrender33 | 60-79 Jahre | Atenolol±Thiazid | Placebo | Geringes Schlaganfallrisiko gegenüber Placebo; kein Unterschied bei AMI oder Mortalität |
| HAPPHY34 | 40-65 Jahre (nur Männer) | MetoprololAtenolol | Thiazid | Tendenz zu weniger Schlaganfällen im Vergleich zu DiuretikaKein Unterschied bei Sterblichkeit oder AMI |
| MAPHY35 | 40-64 Jahre (nur weiße Männer) | Metoprolol | Thiazid | Reduktion der Gesamtmortalität, AMI und Schlaganfall |
| STOP-Hypertension36 | 70-84 y | PindololMetoprololAtenolol | Placebo | Reduzierung der kardiovaskulären Sterblichkeit, AMI, und Schlaganfall |
| MRCOA37 | 65-74 Jahre | AtenololDiuretika | Placebo | Kein Unterschied bei kardiovaskulären Todesfällen, Schlaganfall, oder AMI vs. Placebo (Diuretikum vs. Placebo reduzierte diese Ereignisse) |
| UKPDS38 | Diabetiker | Atenolol | Captopril | Kein Unterschied in der Gesamtmortalität, AMI oder Schlaganfall |
| STOP-239 | 70-84 y | PindololMetoprololAtenolol | Enalapril Lisinopril Felodipin Isradipin | Kein Unterschied in der Sterblichkeit, AMI, oder Schlaganfall |
| CAPPP40 | 20-66 Jahre | MetoprololAtenolol | Captopril | Tendenz zu höherer kardiovaskulärer MortalitätKein Unterschied bei AMI Geringeres Schlaganfallrisiko |
| ELSA41 | Atherosklerose der Karotis | Atenolol | Lacidipin | Erhöhte atherosklerotische Plaque-Progression |
| LIFE42 | 55-80 Jahre | Atenolol | Losartan | Gleiche kardiovaskuläre MortalitätGleiches Risiko für AMMehr SchlaganfallMehr DM |
| INVEST43 | ≥50 JahreSchämische Herzkrankheit | Atenolol±thiazid | Verapamil±trandolapril | Kein Unterschied in der Sterblichkeit, AMI oder Schlaganfall |
| CONVINCE44 | ≥ 55 Jahre mit 1 CVRF | Atenolol | Verapamil | Kein Unterschied in der Sterblichkeit, AMI, oder Schlaganfall |
| ASCOT-BPLA45 | 40-79 JahreHohes kardiovaskuläres Risiko | Atenolol±Thiazid | Amlodipin±Perindopril | Tendenz für höheres AMI-RisikoHöheres SchlaganfallrisikoHöhere kardiovaskuläre MortalitätHöheres DM-Risiko |
AMI, akuter Myokardinfarkt; CVRF, kardiovaskuläre Risikofaktoren; DM, Diabetes mellitus.
Die neuen europäischen Leitlinien zur Hypertonie46 schließen BBs als medikamentöse Therapie der ersten Wahl bei unkompliziertem Bluthochdruck aus.
BETA-BLOCKER UND KARDIALE ARRHYTHMIAS
β1-Rezeptoren machen 80 % der adrenergen Rezeptoren im Herzen aus. Indem sie diese Rezeptoren blockieren, wirken die BBs der proarrhythmischen Wirkung der sympathischen Aktivität auf das Myokard entgegen.47 Die antiarrhythmische Wirkung der BBs ergibt sich einerseits aus ihrer direkten elektrophysiologischen Wirkung auf das Herz, die auf verschiedene Weise vermittelt wird: durch die Senkung der Herzfrequenz, die Verringerung der spontanen Aktivierung von ektopischen Schrittmachern, die Verlangsamung der Leitung elektrischer Impulse oder die Verlängerung der Refraktärzeit des Atrioventrikularknotens. Andererseits werden ihre antiarrhythmischen Eigenschaften durch andere Mechanismen beeinflusst, die zwar keine direkte elektrophysiologische Wirkung auf das Herz haben, aber über die Hemmung der Sympathikusaktivität, die Verringerung der myokardialen Ischämie, die Beeinflussung der Baroreflexfunktion und die Verringerung der mechanischen Belastung zur Verhinderung von Herzrhythmusstörungen beitragen. Diese Wirkungen unterscheiden BBs von anderen Antiarrhythmika, die ihre Wirkung über eine direkte Modulation der Ionenkanäle der Kardiomyozyten entfalten. BBs haben nur begrenzte proarrhythmische Wirkungen und weisen daher ein ausgezeichnetes Wirksamkeits- und Sicherheitsprofil auf.
Vorhofflimmern
BBs sind Medikamente der ersten Wahl für die Kontrolle der Herzfrequenz im Zusammenhang mit Vorhofflimmern bei Patienten ohne Kontraindikationen.48 Obwohl die Therapie zur Kontrolle der Herzfrequenz eine grundlegende Rolle bei der Behandlung von Vorhofflimmern spielt, ist die Aktivität des Sympathikus sowohl mit der Entstehung als auch mit der Aufrechterhaltung von Vorhofflimmern verbunden.49 Nichtsdestotrotz ist die Rolle von BBs bei der Rhythmuskontrolle zweitrangig, auch wenn es stimmt, dass Metoprolol in einer randomisierten Studie im Vergleich zu Placebo das Wiederauftreten von Vorhofflimmern um 11 % reduzierte.50 Darüber hinaus können BBs bei Patienten mit HF oder akutem Myokardinfarkt (AMI) die Inzidenz von Vorhofflimmern reduzieren.51
Kammerrhythmusstörungen
BBs sind besonders nützlich für die Kontrolle ventrikulärer Arrhythmien, die mit der Aktivität des Sympathikus zusammenhängen, wie perioperative Arrhythmien und solche, die mit Stress, AMI und HF in Verbindung stehen.52 Sie verhindern den plötzlichen Herztod, indem sie bösartige ventrikuläre Arrhythmien in verschiedenen Situationen reduzieren, vor allem unter akuten ischämischen Bedingungen, bei systolischer Dysfunktion und bei Kanalopathie. Im Rahmen eines AMI erhöhen BBs die Schwelle für Kammerflimmern während einer akuten Ischämie.53,54 In einer stabileren Phase sind sie besonders nützlich, um narbenbedingte ventrikuläre Arrhythmien nach einem bestätigten AMI zu verhindern, die sich im Allgemeinen als anhaltende monomorphe ventrikuläre Tachykardie zeigen. Bei Patienten mit rEF wurde eine absolute Senkung der Rate des plötzlichen Herztods um etwa 2 % bis 3 % nachgewiesen (∼40 % relative Senkung im Vergleich zu Placebo).55 Bei Patienten mit Kanalopathien, insbesondere bei Patienten mit langem QT-Syndrom und katecholaminerger ventrikulärer Tachykardie, sind BBs das Mittel der Wahl. In diesem Zusammenhang zeigte eine retrospektive Studie mit 233 Patienten mit langem QT-Syndrom und einer Vorgeschichte von Synkopen eine deutliche Verringerung der Sterblichkeit unter BBs im Vergleich zu Placebo.56 Bei Patienten mit katecholaminerger polymorpher ventrikulärer Tachykardie sind BBs das Mittel der Wahl, insbesondere Nadolol.57 Die klinischen Situationen mit nachgewiesenem Nutzen von BBs zur Prävention des plötzlichen Herztods aufgrund ventrikulärer Arrhythmien sind in Abbildung 3 dargestellt.
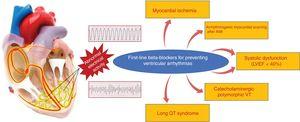
Klinische Situationen mit nachgewiesenem Nutzen von Betablockern zur Vorbeugung des plötzlichen Todes aufgrund ventrikulärer Arrhythmien. AMI, akuter Myokardinfarkt; LVEF, linksventrikuläre Auswurffraktion; VT, ventrikuläre Tachykardie.
BETA-BLOCKER BEI ISCHEMISCHER HERZKRANKHEIT
BBs werden seit mehreren Jahrzehnten zur Behandlung ischämischer Herzkrankheiten eingesetzt, z. B. während eines AMI (intravenöse Verabreichung), bei chronischer Verabreichung nach einem AMI oder bei Patienten mit koronarer Herzkrankheit ohne vorherigen AMI. Mehrere Studien in der Präperfusions-Ära untersuchten die positive Wirkung von Betablockern bei AMI und zeigten eine deutliche Verringerung der Langzeitmortalität.58
Intravenöse Betablocker in der akuten Phase des Infarkts
Im Verlauf des AMI kommt es zu einer katecholaminvermittelten Sympathikusaktivität als Reaktion auf Schmerzen, Angst und eine verminderte Herzleistung. Dieser erhöhte Sympathikustonus hat negative Folgen, wie z. B. einen erhöhten myokardialen Sauerstoffbedarf, der die Myokardnekrose beschleunigt, und eine verringerte Schwelle für Kammerflimmern, die das Risiko eines plötzlichen Herztodes erhöht. Die erhöhte Sympathikusaktivität aktiviert auch verschiedene Arten von zirkulierenden Zellen, wie z. B. Thrombozyten und Neutrophile. Letztere tragen wesentlich zu dem Phänomen bei, das als Reperfusionsschaden bekannt ist.59
Die meisten Studien, die in der Präperfusionsära durchgeführt wurden, verglichen den Einsatz intravenöser BBs unmittelbar nach der AMI-Diagnose, gefolgt von oralen BBs im Vergleich zu Placebo.58 Die frühe Einleitung intravenöser BBs wurde als eine Intervention untersucht, die das Ausmaß der Nekrose begrenzen kann, aber die Ergebnisse waren nicht schlüssig. Ohne Reperfusion ist es schwierig, einen Nutzen bei der Begrenzung des Ausmaßes der Nekrose zu finden. In der Ära der pharmakologischen Reperfusion (Fibrinolyse) erwies sich die intravenöse Gabe von Atenolol in einer randomisierten Studie als unwirksam bei der Verringerung der Infarktgröße.60 Eine andere, nicht randomisierte Studie zeigte jedoch, dass die intravenöse Gabe von Metoprolol mit einer geringeren Infarktgröße verbunden war.61 Die erste klinische Studie zu diesem Thema bei Patienten, die durch primäre Angioplastie reperfundiert wurden, war die METOCARD-CNIC-Studie, die in Spanien durchgeführt wurde.62 In dieser Studie wurde die Verabreichung von Metoprolol mit einer geringeren Infarktgröße53 und einer höheren Langzeit-LVEF in Verbindung gebracht.63 Eine weitere nachfolgende Studie, die EARLY-BAMI-Studie, konnte die kardioprotektiven Effekte einer frühen Metoprolol-Gabe bei Patienten mit AMI, die sich einer primären Angioplastie unterzogen, nicht bestätigen.64 Die Diskrepanz zwischen den beiden Studien scheint auf den Zeitpunkt der Verabreichung von Metoprolol zurückzuführen zu sein (in der METOCARD-CNIC-Studie viel früher), denn je länger die Zeit zwischen der intravenösen Verabreichung von Metoprolol und der Reperfusion ist, desto größer ist seine kardioprotektive Wirkung.65 Der Mechanismus, der der Fähigkeit von Metoprolol zur Verringerung der Infarktgröße zugrunde liegt, wenn es früh vor der Reperfusion intravenös verabreicht wird, scheint eine direkte Wirkung auf zirkulierende Neutrophile und ihre Aggregation mit Thrombozyten zu haben, was zu einer geringeren Reperfusionsschädigung und einer geringeren mikrovaskulären Obstruktion führt.66
Der frühe Einsatz intravenöser BBs beim AMI wurde in Frage gestellt, weil er die Inzidenz des kardiogenen Schocks erhöhen könnte. Diese Bedenken stützen sich auf die Ergebnisse der COMMIT-Studie.54 In dieser Studie war die frühe Verabreichung von Metoprolol an Patienten mit AMI mit einer signifikanten Verringerung des Kammerflimmerns, aber einer Zunahme des Schocks verbunden. Die COMMIT-Population umfasste jedoch Patienten mit fortgeschrittener Erkrankung. Darüber hinaus wurde die Hälfte der Patienten nicht reperfundiert. Außerdem hatten die Patienten, die einen kardiogenen Schock entwickelten, deutliche Anzeichen einer akuten HF sowie Tachykardie und Hypotonie. Im Gegensatz dazu zeigte eine Metaanalyse, die alle Studien mit frühzeitiger Verabreichung von intravenösen BBs einschloss, die mehr als 73 000 Patienten umfasste, dass diese Strategie sicher ist, wenn sie bei Patienten ohne Anzeichen von HF angewendet wird, und auch die Häufigkeit von Kammerflimmern deutlich reduziert.67
Auf der Grundlage der neuen Studien, die bei Patienten durchgeführt wurden, die sich einer primären Angioplastie unterzogen, empfehlen die ESC-Leitlinien für die Behandlung von Patienten mit AMI mit ST-Strecken-Hebung den frühzeitigen Einsatz intravenöser BBs (Klasse IIa A) bei Fehlen von HF-Zeichen oder systolischer Hypotonie (
mmHg).68Erhaltungs-Beta-Blocker nach Infarkt
Der Einsatz von BBs nach AMI wurde in der Präperfusions-Ära eingehend untersucht.58 Abgesehen von der COMMIT-Studie54 mit einer Nachbeobachtungszeit von nur einem Monat ist die CAPRICORN-Studie die einzige klinische Studie, in der die Rolle oraler Erhaltungsbetablocker nach einem Herzinfarkt untersucht wurde.16 In dieser Studie wurden 1950 Patienten mit einer LVEF ≤ 40 % nach einem Herzinfarkt nach dem Zufallsprinzip auf Carvedilol oder Placebo verteilt. Die Einnahme von BB war mit einer Verringerung der Gesamtmortalität verbunden.16 Da viele der Studien, die sich auf HFrEF konzentrieren (Tabelle 1), Patienten nach einem AMI einschlossen, gilt es als erwiesen, dass alle Patienten nach einem AMI mit einer LVEF ≤ 40 % eine Indikation für BBs haben. Allerdings fehlt es an Belegen für den Nutzen von BBs bei Patienten mit einer LVEF > 40 % nach AMI. Zahlreiche Beobachtungsstudien haben versucht, Licht in diese Frage zu bringen, aber alle weisen erhebliche Einschränkungen auf und liefern daher keine endgültigen Informationen (ein Aspekt, der von Ibáñez et al.1 untersucht wurde).
In Anbetracht all dessen empfehlen die klinischen Praxisleitlinien der ESC für Patienten mit AMI nachdrücklich (Klasse IA) den Einsatz von BB, wenn die LVEF ≤ 40 % ist, unabhängig davon, ob die Patienten eine ST-Segment-Hebung oder eine Nicht-ST-Segment-Hebung der AMI haben. Die Empfehlung für Patienten, die einen AMI mit einer LVEF > 40% hatten, ist jedoch schwächer.1
Abbildung 4 zeigt die klinischen Situationen mit nachgewiesenem Nutzen von BBs im Zusammenhang mit AMI.
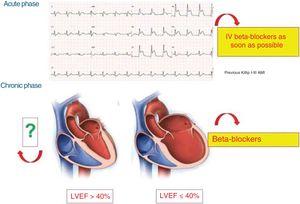
Aktueller Stand der Betablocker in den verschiedenen Phasen des akuten Koronarsyndroms. AMI, akuter Myokardinfarkt; IV, intravenös; LVEF, linksventrikuläre Auswurffraktion.
Aufgrund dieses Mangels an Beweisen für einen so wichtigen Aspekt der täglichen klinischen Versorgung laufen in Europa derzeit drei große pragmatische klinische Studien, um die Rolle von BBs bei Patienten ohne reduzierte LVEF, die einen AMI erlitten haben, zu untersuchen. An der klinischen Studie REBOOT (NCT03596385), die vom Nationalen Zentrum für kardiovaskuläre Forschung (CNIC) in Spanien geleitet wird, sind mehr als 70 spanische und italienische Zentren beteiligt. In diese große spanische Studie werden etwa 8500 Patienten mit einer LVEF> von 40 % nach einem Herzinfarkt einbezogen. Darüber hinaus werden in Schweden und Norwegen die Studien REDUCE-SWEDEHEART (NCT03278509) und BETAMI (NCT03646357) durchgeführt, deren Konzept dem von REBOOT ähnlich ist. Diese großen klinischen Studien werden sich deutlich auf die klinische Praxis in diesem Bereich auswirken.
Tabelle 3 fasst die Ergebnisse der verschiedenen klinischen Studien16,53,54,60,64,69-72 zusammen, die die Rolle von BBs entweder in der akuten Phase des AMI oder in der Erhaltungsphase nach dem akuten Ereignis untersucht haben.
Hauptstudien zum Einsatz von Betablockern beim akuten Koronarsyndrom
| Studie (y) | Reperfusion | Medikament | Anzahl. | Kriterien | Ergebnisse |
|---|---|---|---|---|---|
| Intravenöse Verabreichung in akuter Phase | |||||
| ISIS-I69 (1986)* | Keine | Atenolol | 16 027 | Verdacht auf AMI an beliebiger Stelle | 15% Reduktion der Sterblichkeit |
| MIAMI70 (1985)* | Keine | Metoprolol | 5778 | Verdacht auf AMI an beliebiger | 29% Verringerung der Sterblichkeit |
| MILIS71 (1986) | Nein | Propranolol | 269 | Verdacht auf AMI an beliebiger Stelle | Keine Verringerung der Sterblichkeit oder der AMI-Größe |
| Van de Werf et al.60 (1993) | Ja (Fibrinolyse) | Atenolol | 292 | Verdacht auf AMI an beliebiger Stelle | Keine Verringerung der Mortalität oder der Größe des AMI |
| METOCARD-CNIC53 (2013)* | Ja (Angioplastie) | Metoprolol | 270 | Vorangegangener AMI | Reduktion der AMI-Größe und anschließender Anstieg der LVEF |
| EARLY-BAMI64 (2016) | Ja (Angioplastie) | Metoprolol | 683 | Verdacht auf AMI an beliebiger Stelle | Keine Reduzierung der Infarktgröße |
| Chronische Verabreichung nach Infarkt | |||||
| BHAT72 (1982)* | Keine | Propranolol | 3837 | Infarkt an beliebiger Stelle | 26%ige Verringerung der Sterblichkeit |
| CAPRICORN16 (2001)* | Ja (Fibrinolyse) | Carvedilol | 1959 | Infarkt an beliebiger Stelle und LVEF ≤ 40% | 23% Verringerung der Mortalität |
| COMMIT54 (2005) | Fibrinolyse: 54 % der Stichprobe; 46 % nicht reperfundiert | Metoprolol | 45 852 | Infarkt an beliebiger Stelle ohne LVEF-Einschränkung | Keine Verringerung der Sterblichkeit.Reduktion von Reinfarkt und VF |
AMI, akuter Myokardinfarkt; LVEF, linksventrikuläre Auswurffraktion; VF, Kammerflimmern.
Studien mit positiven (günstigen) Ergebnissen für Betablocker.
Stabile ischämische Herzkrankheit
Die antianginösen Wirkungen von BBs sind gut etabliert und werden in den klinischen Praxisleitlinien berücksichtigt.73 Im Vergleich zu Kalziumkanalblockern reduzieren BBs anginale Episoden und die Zeit bis zum Einsetzen der Ischämie bei Belastungstests.74 Allerdings wurde in keiner klinischen Studie randomisiert und mit ausreichender statistischer Aussagekraft untersucht, ob BBs das Überleben von Patienten mit stabiler koronarer Herzkrankheit, aber ohne AMI oder rEF verbessern. In einer systematischen Übersichtsarbeit und Metaanalyse wurde festgestellt, dass ihre Anwendung die Sterblichkeit nicht verringert.75 Das REACH-Register, das mehr als 40 000 schwedische Patienten umfasste, fand nach einer Propensity-Score-Anpassung keinen Nutzen bei Patienten mit stabiler koronarer Herzkrankheit, aber ohne vorangegangene AMI. Mehrere Studien stützen die Schlussfolgerung, dass die Einnahme von BB bei stabiler koronarer Herzkrankheit und ohne vorangegangenen Herzinfarkt keine positiven Auswirkungen auf die Sterblichkeit und unerwünschte kardiovaskuläre Ereignisse hat.76
ZUSAMMENFASSUNG
BB sind eine Gruppe von Medikamenten, die zur Standardtherapie bei verschiedenen kardiovaskulären Erkrankungen gehören. Ihr Nutzen bei Patienten mit Herzinsuffizienz und ventrikulärer Dysfunktion sowie ihre antiarrhythmischen Wirkungen sind eindeutig belegt. Im Zusammenhang mit einem Herzinfarkt verringert die frühzeitige Verabreichung von intravenösen BBs die Häufigkeit von Kammerflimmern und kann die Infarktgröße verringern, obwohl noch zu zeigen ist, ob sich dies in einer Verbesserung der langfristigen Morbidität und Mortalität niederschlägt. Der Nutzen von chronischen BBs bei Patienten ohne ventrikuläre Dysfunktion, die einen AMI erlitten haben, ist nicht erwiesen. Obwohl sie in der Vergangenheit häufig eingesetzt wurden, hat die Rolle der Blutdrucksenker bei Patienten mit Bluthochdruck ohne andere Komorbiditäten an Bedeutung verloren. Trotz der mehr als vier Jahrzehnte währenden Anwendung von BB gibt es immer noch klinische und experimentelle Fragen zu klären, was diese Gruppe von Medikamenten zu einer der faszinierendsten macht, die uns zur Verfügung stehen.
Förderung
B. Ibáñez leitet Projekte im Zusammenhang mit dem Thema dieser Übersichtsarbeit für die Spanische Gesellschaft für Kardiologie (2017 Translational Research Project) und das MICINN (Spanisches Ministerium für Wissenschaft, Innovation und Universitäten) über den Gesundheitsforschungsfonds Instituto de Salud Carlos III (PI16/02110) und den Europäischen Fonds für regionale Entwicklung (EFRE: SAF2013-49663-EXP). Das CNIC (Nationales Zentrum für kardiovaskuläre Forschung) wird vom MICINN, dem ISCiii und der Stiftung ProCNIC finanziert und ist ein Severo Ochoa Center of Excellence (SEV-2015-0505).
INTERESSENSKONFLIKTE
Es wurden keine erklärt.