O elemento químico ferro é classificado como um metal de transição. Ele é conhecido desde a antiguidade. O seu descobridor e data de descoberta são desconhecidos.

Zona de dados
| Classificação: | O ferro é um metal de transição |
| Cor: | Cinza-prateada |
| Peso atómico: | 55.847 |
| Estado: | Sólido: |
| Ponto de fusão: | 1535.1 oC, 1808.2 K |
| Ponto de fusão: | 2750 oC, 3023 K |
| Electrões: | 26 |
| Protões: | 26 |
| Neutrons no isótopo mais abundante: | 30 |
| Conchas de electrões: | 2,8,14,2 |
| Configuração de electrões: | 3d6 4s2 |
| Densidade @ 20oC: | 7.87 g/cm3 |
Mostrar mais, incluindo: Aquecimento, Energias, Oxidação,
Reacções, Compostos, Raios, Condutividades
| Volume atómico: | 7,1 cm3/mol |
| Estrutura: | bcc: cúbico centrado no corpo |
| Dureza: | 4.0 mohs |
| Capacidade térmica específica | 0.44 J g-1 K-1 |
| Calor de fusão | 13.80 kJ mol-1 |
| Calor de atomização | 415 kJ mol-1 |
| Calor de vaporização | 349.60 kJ mol-1 |
| 1ª energia de ionização | 759,3 kJ mol-1 |
| 2ª energia de ionização | 1561.1 kJ mol-1 |
| 3ª energia de ionização | 2957,3 kJ mol-1 |
| Afinidade electrónica | 15.7 kJ mol-1 |
| Número mínimo de oxidação | -2 |
| Mín. número comum de oxidação | 0 |
| Número máximo de oxidação | 6 |
| Número máximo de oxidação comum. | 3 |
| Electronegatividade (Escala de Paulagem) | 1.9 |
| Volume de polarização | 8.4 Å3 |
| Reacção com ar | suave, ⇒ Fe3O4 |
| Reacção com 15 M HNO3 | passivado |
| Reacção com 6 M HCl | vigoroso, ⇒ H2, FeCl2 |
| Reacção com NaOH 6 M | – |
| Óxido(s) | FeO, Fe2O3 (hematite), Fe3O4 (magnetita) |
| Hidreto(s) | nenhum |
| Cloreto(s) | FeCl2, FeCl3 |
| Raio atómico | 140 pm |
| Raio iónico (1+ião) | – |
| Raio iónico (2+ião) | 77 pm |
| Raio iónico (3+ião) | 63 pm |
| Raio iónico (1- ião) | – |
| Raio iónico (2 iões) | – |
| Raio iónico (3 iões) | – |
| Condutividade térmica | 80.4 W m-1 K-1 |
| Condutividade eléctrica | 11,2 x 106 S m-1 |
| Ponto de congelação/congelação: | 1535.1 oC, 1808.2 K |
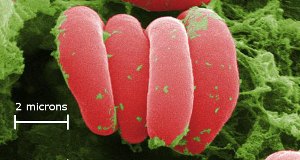
Células de sangue vermelhas – a cor vem do ferro em hemoglobina. As células são ampliadas x10.000. Se você cresceu x10.000, você poderia colocar seus pés em Seattle e tocar Perth, Austrália, com suas mãos. O ferro na hemoglobina transporta oxigênio ao redor do nosso corpo. Ref. imagem (10)

Fechamento de um meteorito de ferro: Meteoritos como este foram provavelmente a primeira fonte de ferro dos nossos antepassados. Este é um fragmento do meteorito Sikhote-Alin – aproximadamente 93% de ferro, 6% de níquel e 1% de outros elementos. A superfície do meteorito foi derretida em formas de impressão digital durante o seu voo através da atmosfera do nosso planeta. Foto de Carl Allen, NASA JSC Foto S94-43472.

Sucata de ferro e aço para reciclagem. Como os tempos mudaram; o ferro já valeu oito vezes mais que o ouro.
Descoberta do ferro
O ferro é conhecido desde os tempos antigos.
O primeiro ferro usado pelos humanos provavelmente veio de meteoritos.
A maioria dos objectos que caem do espaço à terra são pedregosos, mas uma pequena proporção, como o que está representado, são ‘meteoritos de ferro’ com teores de ferro superiores a 90%.
O ferro corroi facilmente, por isso os artefactos de ferro dos tempos antigos são muito mais raros que os objectos feitos de prata ou ouro. Isto torna mais difícil traçar a história do ferro do que os metais menos reactivos.
Artefactos feitos de ferro de meteorito foram encontrados datando de cerca de 5000 a.C. (e por isso têm cerca de 7000 anos de idade) – por exemplo, contas de ferro em túmulos no Egipto. (1)
Na Mesopotâmia (Iraque) há evidências de que as pessoas estavam fundindo ferro por volta de 5000 AC.
Artefactos feitos de ferro fundido foram encontrados datando de cerca de 3000 AC no Egipto e na Mesopotâmia. (1), (2), (3)
Naqueles tempos, o ferro era um metal cerimonial; era demasiado caro para ser usado na vida quotidiana. Os escritos assírios nos dizem que o ferro era oito vezes mais valioso do que o ouro. (1)
A era do ferro começou por volta de 1300-1200 AC, quando o ferro se tornou barato o suficiente para substituir o bronze.
A adição de carbono ao ferro para fazer aço foi provavelmente acidental no início – uma junção de ferro fundido e carvão vegetal do fogo de fusão. Isto provavelmente aconteceu por volta de 1000 AC. (4)
Até isto acontecer, havia poucas razões tecnológicas para a idade do bronze dar lugar à idade do ferro; as técnicas de melhorar o ferro adicionando carbono (para fazer aço) e trabalho a frio eram necessárias antes que o ferro fosse totalmente preferido ao bronze. (5)
O ferro era comumente usado na época romana. No primeiro século Plínio, o Ancião disse: “É com a ajuda do ferro que construímos casas, fendemos rochas e fazemos tantos outros escritórios úteis na vida”. (6)
A origem do símbolo químico Fe é da palavra latina ‘ferrum’ que significa ferro. A palavra ferro em si vem de ‘iren’ em anglo-saxão.
Fatos interessantes sobre o ferro
- Acredita-se que um terço da massa da Terra é de ferro, a maior parte do qual se encontra nas profundezas do planeta, no núcleo.
- A Terra tem ferro suficiente para fazer três novos planetas, cada um com a mesma massa que Marte.
- Circulação de ferro líquido nas profundezas da Terra acredita-se que cria as correntes eléctricas que criam o campo magnético do nosso planeta.
- Iron é essencial para o desenvolvimento do cérebro humano. A deficiência de ferro em crianças leva, entre outros problemas, a uma capacidade de aprendizagem prejudicada. (7)
- Nos tempos antigos, as pessoas não sabiam como o ferro era muito abundante na Terra. A sua única fonte de ferro metálico eram os meteoritos. Pelos escritos assírios aprendemos que o ferro era oito vezes mais valioso que o ouro. Além da sua raridade, o ferro também pode ter sido muito desejável porque, vindo do céu, era considerado um presente dos deuses: os antigos egípcios o chamavam de ‘ba-ne-pe’, que significava ‘metal do céu’. A ligação com o céu é reforçada por Textos em Pirâmide, que traduzem, por exemplo, para: “Os meus ossos são de ferro e os meus membros são as estrelas imperecíveis. (8) (9)
- Iron foi o primeiro metal magnético descoberto. Lodestones eram usados por antigos navegadores porque podiam ser usados como bússolas, apontando para o pólo norte magnético; isto foi descrito pelo antigo filósofo grego Thales de Miletus em 600 aC. As lousestones eram feitas de magnetita, que é um óxido de ferro que ocorre naturalmente. A fórmula da magnetita é FeO.Fe2O3.
- Alguns animais têm um sexto sentido – o sentido magnético. A magnetite tem sido encontrada numa vasta gama de animais, incluindo abelhas, pombos-correio e golfinhos. Estes animais são sensíveis ao campo magnético da Terra, ajudando a sua capacidade de navegação.
- O meteorito Hoba na Namíbia é a maior peça de ferro natural do mundo, pesando mais de 60 toneladas. É feito de 82 – 83% de ferro, 16 – 17% de níquel, cerca de 1% de cobalto, e muito pequenos vestígios de outros elementos. O meteorito Hoba é o maior meteorito único já encontrado.
- O ferro é ferromagnético. Ferromagnetismo é o tipo mais forte de magnetismo. Outros metais ferromagnéticos comuns são o níquel e o cobalto.
- Muitos poderosos ímãs podem ser feitos usando ferro, níquel ou cobalto em associação com metais de terras raras. Os ímanes NIB (Neodímio – Ferro – Boro) foram inventados no início da década de 1980. Eles são uma liga nas proporções Nd2Fe14B. São utilizados em computadores, telemóveis, equipamentos médicos, brinquedos, motores, turbinas eólicas e sistemas de áudio.
>


>
Aspecto e Características
Efeitos nocivos:
O ferro é considerado não tóxico.
Características:
O ferro é um metal dúctil, cinzento, relativamente macio e é um condutor moderadamente bom de calor e electricidade.
É atraído por ímanes e pode ser facilmente magnetizado.
O metal puro é quimicamente muito reactivo e enferruja prontamente em ar húmido, formando óxidos castanhos-avermelhados.
Existem três formas alotrópicas de ferro, conhecidas como alfa, gama, e delta.
O ferro alfa, também conhecido como ferrite, é a forma estável de ferro a temperaturas normais.
Usos do ferro
O ferro é o mais barato e o mais importante de todos os metais – importante no sentido de que o ferro é o metal mais comumente usado, sendo responsável por 95% da produção mundial de metais.
O ferro é usado para fabricar aço e outras ligas importantes na construção e fabrico.
O ferro também é vital no funcionamento dos organismos vivos, transportando oxigénio no sangue através da molécula de hemoglobina.
Abundância e Isótopos
Abundância da crosta terrestre: 5,6 % de peso, 2,1 % por moles
Abundância do sistema solar: 1000 partes por milhão de peso, 30 partes por milhão de moles
Custo, puro: $7,2 por 100g
Custo, a granel: $0,02 por 100g
Fonte: O ferro não é encontrado livre na natureza, mas é encontrado em minérios de ferro como a hematita (Fe2O3), magnetita (Fe3O4) e taconita. Comercialmente, o ferro é produzido em um forno a temperaturas de cerca de 2000 oC pela redução da hematita ou magnetita com carbono.
Isótopos: O ferro tem 24 isótopos cujas meias-vidas são conhecidas, com números de massa de 46 a 69. O ferro que ocorre naturalmente é uma mistura de quatro isótopos e são encontrados nas percentagens apresentadas: 54Fe (5,8%), 56Fe (91,8%), 57Fe (2,1%) e 58Fe (0,3%).

- Henry Maryon, Early Near Eastern Steel Swords., 65, 1961, American Journal of Archaeology p1.
- Michael D. Fenton, Mineral Commodity Profiles – Iron and Steel., 2005, U.S. Geological Survey.
- R. J. Forbes, Studies in Ancient Technology., IX, 1965, p247.
- Michael Woods, Mary B. Woods, Ancient Machines: From Wedges to Waterwheels., 2000, p30, Runestone Press.
- Vincent C. Pigott, The Archaeometallurgy of the Asian Old World, 1999, p28, UPenn Museum of Archaeology.
- Mary Elvira Weeks, Discovery of the Elements., 2003, p5, Kessinger Publishing.
- http://www.ncbi.nlm.nih.gov/pubmed/17101454.
- John G. Burke, Cosmic Debris: Meteoritos na História, 1986, p229, University of California Press.
- Robert G. Bauval, Investigação sobre as origens da pedra de Benben. 14, 1989, Discussões em Egiptologia.
- Image: CDC
Cite esta página
Para criar um link online, por favor copie e cole um dos seguintes:
<a href="https://www.chemicool.com/elements/iron.html">Iron</a>
ou
<a href="https://www.chemicool.com/elements/iron.html">Iron Element Facts</a>
Para citar esta página num documento académico, por favor use a seguinte citação compatível com a MLA:
"Iron." Chemicool Periodic Table. Chemicool.com. 06 Oct. 2012. Web. <https://www.chemicool.com/elements/iron.html>.