>

>
>
Dímeros moleculares são frequentemente formados pela reação de dois compostos idênticos, por exemplo: 2A → A-A. Neste exemplo, diz-se que o monômero “A” é dimerizado para dar ao dímero “A-A”. Um exemplo é um diaminocarbene, que dimeriza para dar um tetraaminotileno:
2 C(NR2)2 → (R2N)2C=C(NR2)2
Carbenes são altamente reativos e prontamente formam ligações.
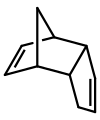
Diciclopentadieno é um dimer assimétrico de duas moléculas de ciclopentadieno que reagiram em uma reação Diels-Alder para dar o produto. Ao aquecer, ele “racha” (sofre uma reação retro-Diels-Alder) para dar monômeros idênticos:
C10H12 → 2 C5H6
Muitos elementos não metálicos ocorrem como dímeros: hidrogênio, nitrogênio, oxigênio, os halógenos, ou seja, flúor, cloro, bromo e iodo. Os gases nobres podem formar dímeros ligados por ligações van der Waals, por exemplo, diélio ou diargônio. O mercúrio ocorre como um cátion de mercúrio(I) (Hg22+), formalmente um íon dimérico. Outros metais podem formar uma proporção de dímeros em seu vapor. Os dímeros metálicos conhecidos incluem Li2, Na2, K2, Rb2 e Cs2.
Muitas pequenas moléculas orgânicas, mais notavelmente formaldeído, facilmente formam dímeros. O dímero de formaldeído (CH2O) é o dioxetano (C2H4O2).