INLEIDING
Weinig geneesmiddelengroepen zijn in de loop der jaren zo uitgebreid bestudeerd als bètablokkers (BB’s) bij patiënten met verschillende cardiovasculaire aandoeningen. In de afgelopen 3 decennia hebben zij een revolutie teweeggebracht in de cardiologie, en uitgebreide bewijzen bevestigen hun werkzaamheid bij de 4 meest voorkomende groepen cardiovasculaire ziekten: hartfalen (HF), hypertensie, aritmieën, en ischemische hartziekte. Tegelijkertijd worden er nog steeds nieuwe werkingsmechanismen van BB’s gevonden, die helpen om de redenen voor hun duidelijke voordelen beter te verklaren.1 Deze nieuwe ontdekkingen breiden de potentiële, maar nog niet geïdentificeerde toepassingen van BB’s in klinische settings verder uit.
Hier presenteren we het bestaande bewijs voor de voordelen van BB’s in verschillende klinische contexten, de werkingsmechanismen die aan deze voordelen ten grondslag liggen, en de huidige aanbevelingen.
BETA-BLOCKERS IN HARTFILURE
Omwille van hun negatieve inotrope eigenschappen werden BB’s lange tijd beschouwd als absoluut gecontra-indiceerd bij patiënten met HF. Het veld onderging een conceptuele revolutie toen men zich bedacht dat, in tegenstelling tot de heersende wijsheid, BB’s paradoxaal genoeg gunstig zouden kunnen zijn. In het eerste decennium van de 21e eeuw werd aangetoond dat deze geneesmiddelen zeer positieve effecten hadden bij patiënten met HF. Sindsdien zijn ze een hoeksteen geworden in de behandeling van HF bij patiënten met systolische disfunctie (verminderde linker ventrikel ejectiefractie , ≤ 40%; ook bekend als verminderde ejectiefractie ). HF moet echter in zijn hele spectrum worden begrepen, van asymptomatische patiënten die niettemin risico lopen op HF – stadium A van het American College of Cardiology/American Heart Association (ACC/AHA)2 – tot symptomatische patiënten met verschillende LVEF-bereiken en zelfs gehospitaliseerde patiënten of patiënten met ernstige HF-symptomen.
Hartfalen met gereduceerde ejectiefractie
Het bewijs toont onomstotelijk aan dat BB’s het risico op overlijden verlagen bij patiënten met HFrEF. Het gebruik ervan wordt algemeen erkend in de recente richtlijnen voor klinische praktijk van de European Society of Cardiology (ESC).3 Tabel 1 toont gegevens uit de belangrijkste gerandomiseerde onderzoeken4-10 die het gebruik van BB’s ondersteunen, evenals hun vermogen om de belangrijkste eindpunten te verminderen. Hoewel metoprolol, bisoprolol en carvedilol geassocieerd zijn met significante gunstige effecten, is de associatie niet zo consistent voor bucindolol en nebivolol. In de SENIORS-studie (leeftijd > 70 jaar, 64% met rEF) was nebivolol geassocieerd met een lager risico op het samengestelde eindpunt van overlijden en cardiovasculaire ziekenhuisopname, maar niet op overlijden alleen of de andere eindpunten.4 Bucindolol slaagde er in de BEST-studie niet in de mortaliteit te verminderen, maar verminderde wel het aantal ziekenhuisopnames voor HF.5 De 3 BB’s met het sterkste bewijs in deze populatie (metoprolol, bisoprolol en carvedilol) zijn geassocieerd met minder ziekteprogressie, zoals blijkt uit de lagere percentages direct gerelateerde sterfgevallen (plotseling en HF) en HF-opnames in de verschillende onderzoeken.6-8
Opzet en resultaten van de belangrijkste klinische trials met bètablokkers bij hartfalen
| Studie (j, patiënten) | Medicijn, gemiddeld (mg/d) | NYHA | LVEF | Ischemisch | Gemiddelde follow-up, mo | NYHA klasse III/IV | NNT1 leven1 j | Vermindering van risico op overlijden | Vermindering van risico op ziekenhuisopname | ||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Totaal | CV | Totaal | Door HF | Totaal | |||||||||
| CIBIS-II6 (1999, n=2647) | Bisoprolol 7.5 mg/d | III-IV | ≤35% | 50% | 15 | 100% | 23 | 34% | 29% | 44% | 26% | 20% | 36% |
| MERIT-HF7 (1999, n=3991) | Metoprolol 159 mg/d | II-IV | ≤40% | 65% | 12 | 59% | 27 | 34% | 38% | 41% | 49% | 18% | 35% |
| US carvedilol10 (1996, n=1094) | Carvedilol 45 mg/d | II-IV | ≤35% | 48% | 6 | 60% | 15 | 65% | 65% | 55% | 79% | 27% | – |
| COPERNICUS8 (2002, n=2289) | Carvedilol 37 mg/d | III-IV | 25% | 67% | 10 | 100% | 15 | 35% | – | – | – | 20% | 33% |
| COMET9 (2003, n=3029) | Carvedilol 42 mg/d vs metoprolol 85 mg/d | II-IV | 35% | 51% | 58 | 51% | – | 17% | 20% | 3%, NS | |||
| BEST5 (2001, n=2708) | Bucindolol 152 mg/d | III-IV | ≤35% | 59% | 24 | 100% | – | 10%, NS | 14%, NS | 12%, NS | 15%, NS | 8%, NS | 22% |
| SENIORS4 (2005, n=2128) | Nebivolol 7.7 mg/d | II-IV | * | 68% | 21 | 40% | – | 12%, NS | 16%, NS | – | – | 4%, NS | – |
CV, cardiovasculair; HF, hartfalen; LVEF, linker ventrikel ejectiefractie; NNT, aantal dat nodig is om te behandelen; NS, niet significant; NYHA, New York Heart Association.
Alle studies analyseerden bètablokkers versus placebo, behalve COMET (carvedilol versus metoprolol tartraat). Alle risicoreducties zijn significant, tenzij anders aangegeven.
LVEF was geen inclusiecriterium, maar 36% van de patiënten had een LVEF> 35%; de geïncludeerde patiënten waren ouder dan 70 jaar.
In de COMET-studie, de enige studie waarin 2 BB’s – carvedilol versus metoprololtartraat – rechtstreeks werden vergeleken, werd een lagere mortaliteit gevonden met carvedilol; het gebruik van kortwerkend metoprolol, in tegenstelling tot de formulering die in de MERIT-HF-studie7 werd gebruikt, zou deze verschillen echter enigszins kunnen verklaren.9 In een grote meta-analyse, voornamelijk gebaseerd op BB’s met bewezen overlevingsvoordeel, werden geen verschillen gevonden tussen de verschillende BB’s, die samen de 12-maands mortaliteit met 31% verminderden zonder interacties tussen behandeling en subgroep.11Figuur 1 toont de relatieve risicovermindering en het aantal patiënten dat op 1 jaar moet worden behandeld om de verschillende voorvallen te verminderen, op basis van de resultaten van de meta-analyse.11
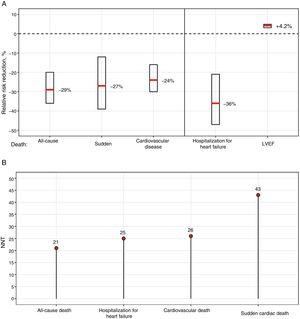
Voordelen van bètablokkers bij patiënten met hartfalen en verminderde LVEF. A: Relatieve risicovermindering en 95%-betrouwbaarheidsinterval. B: NNT na 1 jaar. LVEF, linker ventrikel ejectiefractie; NNT, number needed to treat.
In de afgelopen jaren hebben verschillende meta-analyses zich gebogen over het verband tussen de voordelen van BB’s en de hartfrequentie bij patiënten met rEF. Het verband tussen een hogere hartfrequentie en een slechtere prognose is duidelijk aangetoond. Niettemin bleek uit een subanalyse van de HF-ACTION-studie dat het voordeel groter is in aanwezigheid van hoge doses BB’s, ongeacht de hartfrequentie.12 Anderzijds hebben andere recente meta-analyses aangetoond dat het aan hartfrequentieverlaging gerelateerde voordeel van BB’s alleen wordt bereikt bij patiënten met sinusritme of ten minste lager is bij patiënten met atriumfibrilleren (AF).13 Een subanalyse van de AF-CHF-studie toonde echter aan dat BB’s ook de mortaliteit bij patiënten met AF en rEF verbeterden.14
Een bijzondere kwestie vormen patiënten met asymptomatische rEF. Bij deze patiënten voorkomen BB’s theoretisch de ongunstige ventriculaire remodelleringsprocessen die de progressie naar symptomatische HF bevorderen. De REVERT-studie, de enige studie waarbij asymptomatische patiënten in stadium I van de New York Heart Association (NYHA) en met rEF (stadium B van de ACC/AHA) werden gerandomiseerd,1 toonde aan dat metoprololsuccinaat geassocieerd was met verminderde volumes en een verhoogde LVEF na 1 jaar.15 De CAPRICORN-studie (postinfarct LVEF
40%) toonde minder progressie naar symptomatische stadia en verbeterde remodellering en ventrikelfunctie.16 In een observationele studie verminderde het gebruik van BB het aantal episoden van symptomatische HF met 60%.17 Hartfalen met midrange of behouden systolische functie
Prospectieve klinische studies zijn schaars en hebben doorgaans indirecte eindpunten zoals echocardiografische parameters of kleine steekproefgroottes die alleen een schatting van het effect op klinische eindpunten mogelijk maken. Een observationele studie, gebaseerd op propensity score adjustment met een grote populatie van gehospitaliseerde patiënten, en verscheidene meta-analyses geven aan dat BB’s de mortaliteit kunnen verminderen bij patiënten met een LVEF > 40%.18 Onlangs heeft een substudie van de TOPCAT-trial (LVEF> 45%) aangetoond dat BB’s, met name bij patiënten zonder eerder infarct, geassocieerd waren met een toename van ongunstige cardiovasculaire voorvallen.19 Na de aanbeveling in de laatste Europese richtlijnen om patiënten met een LVEF in het middengebied (40%-49%) als een aparte subgroep te beschouwen, bleek echter uit een afzonderlijke meta-analyse waarin de LVEF van elke patiënt in de spilklinische trials was opgenomen, dat patiënten in sinusritme wel degelijk baat kunnen hebben bij BB-therapie wat de mortaliteit betreft.20
Zwaar acuut of gedecompenseerd hartfalen
Voor patiënten die met rEF in het ziekenhuis worden opgenomen, vermindert voortzetting van BB’s tijdens de opname het risico op overlijden met 40%, terwijl initiatie van BB-therapie bij BB-naïeve patiënten het risico met bijna 60% vermindert.21 Daarentegen verdubbelt terugtrekking van BB’s tijdens de opname de mortaliteit.22 De COPERNICUS-studie evalueerde patiënten met ernstige HF (NYHA-klasse III-IV en LVEF
25%), met inbegrip van gehospitaliseerde of gedecompenseerde patiënten die intraveneuze diuretica gebruikten. Het gebruik van carvedilol verminderde het totale risico op overlijden met 35%.7 Bovendien vergemakkelijkte BB-initiatie tijdens de ziekenhuisopname de therapietrouw aan BB tijdens de follow-up.23 In een andere subanalyse van de MERIT-HF-studie, die patiënten met ernstigere klinische verslechtering (NYHA-klasse III-IV en LVEF 25%) omvatte, was het voordeel van metoprolol duidelijk en zelfs groter.24BÈTA-BLOCKERS IN HYPERTENSIE
Vergeleken met placebo is niet aangetoond dat BB’s de mortaliteit door alle oorzaken of de cardiovasculaire mortaliteit verminderen bij patiënten met ongecompliceerde essentiële hypertensie.25-27 Zij kunnen echter wel de cardiovasculaire voorvallen verminderen, vooral beroertes. In vergelijking met diuretica verminderen BB’s het aantal cardiovasculaire voorvallen niet en kunnen ze zelfs geassocieerd zijn met een hogere incidentie van beroerten.28 Deze hoge incidentie van beroerten lijkt samen te hangen met leeftijd, waardoor het risico van BB’s toeneemt bij personen ouder dan 60 jaar.29 In vergelijking met calciumantagonisten of angiotensine-converterende enzymremmers/angiotensine-receptorblokkers zijn BB’s geassocieerd met een verhoogd risico op beroerte.26,27 De resultaten van het gebruik van BB’s als eerstelijns geneesmiddelen bij de behandeling van hypertensie versus andere geneesmiddelengroepen zijn weergegeven in figuur 2.
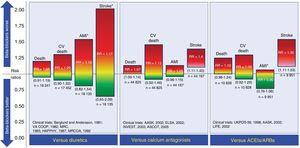
Vergelijking van bètablokkers met andere geneesmiddelen die als eerstelijnsstrategie worden gebruikt voor de behandeling van essentiële hypertensie. De risicoverhoudingen zijn uitgezet met hun 95%-betrouwbaarheidsintervallen (tussen haakjes). ACEI’s, angiotensine-converterende enzymremmers; AMI, acuut myocardinfarct; ARB’s, angiotensine II-receptorblokkers; CV, cardiovasculair; RR, risicoverhouding. *Gevallen waarvan de risicoratio en het bijbehorende betrouwbaarheidsinterval een lage mate van zekerheid hebben volgens de classificaties van het bewijskrachtniveau van de GRADE-werkgroep. De informatie is gebaseerd op de meta-analyse van Wiysonge et al.27
Omdat BB’s een heterogene groep geneesmiddelen vormen, moeten conclusies die uit meta-analyses worden getrokken over het algemeen met de nodige voorzichtigheid worden gehanteerd. Tabel 2 geeft een overzicht van de resultaten van de belangrijkste klinische trials waarin de rol van de verschillende BB’s bij de behandeling van hypertensie is geanalyseerd.30-45
Belangrijkste klinische studies waarin bètablokkers bij de behandeling van essentiële hypertensie zijn geanalyseerd
| Studie | Populatie | Bètablokkers | Bètablokkers | Bètablokkers | .blokker | Vergelijking | Resultaat | |
|---|---|---|---|---|---|---|---|---|
| Berglund en Andersson30 | 47-54 jaar | Propranolol | Thiazide | Geen verschil in mortaliteit | ||||
| VA COOP31 | 21-65 jaar | Propranolol | Thiazide | Geen verschil in mortaliteit, AMI, of beroerte | ||||
| MRC32 | 35-64 jaar | Propranolol | ThiazidePlacebo | Lager risico op beroerte versus placebo; geen verschil in AMI of mortaliteitHoger risico op beroerte vs thiazide | ||||
| Coope en Warrender33 | 60-79 jaar | Atenolol±thiazide | Placebo | Lager risico op beroerte vs placebo; geen verschil in AMI of mortaliteit | ||||
| HAPPHY34 | 40-65 jaar (alleen mannen) | MetoprololAtenolol | Thiazide | Tendens voor minder beroerte versus diureticaGeen verschil in sterfte of AMI | ||||
| MAPHY35 | 40-64 jaar (alleen blanke mannen) | Metoprolol | Thiazide | Vermindering van totale mortaliteit, AMI, en beroerte | ||||
| STOP-Hypertension36 | 70-84 y | PindololMetoprololAtenolol | Placebo | Vermindering van cardiovasculaire mortaliteit, AMI, en beroerte | ||||
| MRCOA37 | 65-74 y | AtenololDiuretica | Placebo | Geen verschil in cardiovasculaire sterfte, beroerte, of AMI vs placebo (diuretica vs placebo verminderden dergelijke voorvallen wel) | ||||
| UKPDS38 | Diabetische patiënten | Atenolol | Captopril | Geen verschil in totale mortaliteit, AMI, of beroerte | ||||
| STOP-239 | 70-84 y | PindololMetoprololAtenolol | Enalapril Lisinopril Felodipine Isradipine | Geen verschil in sterfte, AMI, of beroerte | ||||
| CAPPP40 | 20-66 jaar | MetoprololAtenolol | Captopril | Tendens voor hogere cardiovasculaire mortaliteit Geen verschil in AMILager risico op beroerte | ||||
| ELSA41 | Carotis atherosclerose | Atenolol | Lacidipine | Verhoogde progressie van atherosclerotische plaque | ||||
| LIFE42 | 55-80 jaar | Atenolol | Losartan | Zelfde cardiovasculaire mortaliteitZelfde risico op AMIME meer beroerteMeer DM | ||||
| INVEST43 | ≥50 jIschemische hartziekte | Atenolol±thiazide | Verapamil±trandolapril | Geen verschil in mortaliteit, AMI, of beroerte | ||||
| CONVINCE44 | ≥ 55 jaar met 1 CVRF | Atenolol | Verapamil | Geen verschil in sterfte, AMI, of beroerte | ||||
| ASCOT-BPLA45 | 40-79 jaarHoog cardiovasculair risico | Atenolol±thiazide | Amlodipine±perindopril | Tendens voor hoger risico op AMIHoger risico op beroerteHogere cardiovasculaire mortaliteitHoger risico op DM |
AMI, acuut myocardinfarct; CVRF, cardiovasculaire risicofactoren; DM, diabetes mellitus.
De nieuwe Europese richtlijnen inzake hypertensie46 sluiten BB’s uit als eerstelijns geneesmiddelentherapie voor ongecompliceerde hypertensie.
BETA-BLOCKERS EN CARDIAC ARRHYTHMIAS
β1-receptoren vormen 80% van de adrenerge receptoren in het hart. Door deze receptoren te blokkeren, gaan BB’s het pro-aritmische effect van sympathische activiteit op het myocard tegen.47 Het antiaritmische effect van BB’s is enerzijds het resultaat van hun directe cardiale elektrofysiologische werking, die op verschillende manieren wordt gemedieerd: door verlaging van de hartfrequentie, vermindering van de spontane activering van ectopische pacemakers, vertraging van de geleiding van elektrische impulsen, of verhoging van de refractaire periode van de atrioventriculaire knoop. Anderzijds worden hun antiaritmische eigenschappen beïnvloed door andere mechanismen die, hoewel ze geen directe elektrofysiologische cardiale activiteit hebben, wel bijdragen tot het voorkomen van hartritmestoornissen, via remming van de sympathische activiteit, vermindering van myocardischemie, een effect op de baroreflexfunctie, en verminderde mechanische stress. Deze effecten onderscheiden BB’s van andere antiaritmica, die hun activiteit uitoefenen via directe modulatie van ionenkanalen in de cardiomyocyten. BB’s hebben beperkte pro-aritmische effecten en hebben dus een uitstekend werkzaamheids- en veiligheidsprofiel.
Atriumfibrilleren
BB’s zijn eerstelijns geneesmiddelen voor de controle van de hartfrequentie in de context van AF bij patiënten zonder contra-indicaties.48 Hoewel therapie voor snelheidscontrole een fundamentele rol speelt in de behandeling van AF, is sympathische activiteit gerelateerd aan zowel het begin als het behoud van AF.49 Niettemin is de rol van BB’s in de ritmecontrole secundair, hoewel het waar is dat, in een gerandomiseerde studie versus placebo, metoprolol de terugkeer van AF met 11% verminderde.50 Bovendien kunnen bij patiënten met HF of een acuut myocardinfarct (AMI), BB’s de incidentie van AF verminderen.51
Ventriculaire aritmieën
BB’s zijn met name nuttig voor de bestrijding van ventriculaire aritmieën die verband houden met sympathische activiteit, zoals perioperatieve aritmieën en aritmieën die verband houden met stress, AMI en HF.52 Ze voorkomen plotse hartdood door kwaadaardige ventriculaire aritmieën in verschillende contexten te verminderen, voornamelijk onder acute ischemische, systolische disfunctie- en channelopathieomstandigheden. In de setting van een AMI verhogen BB’s de drempel voor ventrikelfibrilleren tijdens acute ischemie.53,54 In een stabielere fase zijn ze vooral nuttig voor het voorkomen van littekengerelateerde ventriculaire aritmieën na een bevestigde AMI, die zich over het algemeen presenteren als aanhoudende monomorfe ventriculaire tachycardie. Bij patiënten met rEF is een absolute vermindering van het aantal plotselinge hartdoodgevallen van ongeveer 2% tot 3% aangetoond (∼40% relatieve vermindering ten opzichte van placebo).55 Bij patiënten met kanaalopathieën, met name die met het lange QT-syndroom en catecholaminerge ventriculaire tachycardie, zijn BB’s het middel van keuze. In dit verband toonde een retrospectieve studie van 233 patiënten met het lange QT-syndroom en een voorgeschiedenis van syncope een duidelijke vermindering van de mortaliteit met BB’s ten opzichte van placebo.56 Voor patiënten met catecholaminerge polymorfe ventriculaire tachycardie zijn BB’s het middel van keuze, met name nadolol.57 De klinische situaties waarin het nut van BB’s voor de preventie van plotselinge hartdood als gevolg van ventriculaire aritmieën is aangetoond, zijn weergegeven in figuur 3.
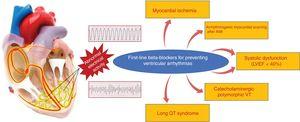
Clinische situaties met bewezen voordelen van bètablokkers voor de preventie van plotseling overlijden als gevolg van ventriculaire aritmieën. AMI, acuut myocardinfarct; LVEF, linker ventrikel ejectiefractie; VT, ventriculaire tachycardie.
BETA-BLOCKERS IN ISCHEMISCHE HARTZIEKTE
BBs worden al enkele decennia gebruikt om ischemische hartziekte te beheersen in contexten zoals tijdens AMI (intraveneuze toediening), bij chronische toediening na AMI, of bij patiënten met coronaire ziekte zonder eerdere AMI. Meerdere studies in het prereperfusietijdperk onderzochten het gunstige effect van BB’s in de setting van AMI en toonden een duidelijke vermindering van de mortaliteit op lange termijn.58
Intraveneuze bètablokkers in de acute fase van infarct
Tijdens het verloop van AMI treedt catecholaminegemedieerde sympathische activiteit op als reactie op pijn, angst en verminderde cardiale output. Deze toename van de sympathische tonus heeft negatieve gevolgen, zoals een verhoogde myocardiale zuurstofbehoefte die myocardiale necrose versnelt en een verlaagde ventriculaire fibrillatiedrempel die het risico op plotse hartdood verhoogt. De verhoogde sympathische activiteit activeert ook verschillende soorten circulerende cellen, zoals bloedplaatjes en neutrofielen. Deze laatste dragen in belangrijke mate bij aan het verschijnsel dat bekend staat als reperfusieschade.59
De meeste trials die zijn uitgevoerd in het prereperfusietijdperk vergeleken het gebruik van intraveneuze BB’s onmiddellijk na de diagnose van AMI, gevolgd door orale BB’s versus placebo.58 De vroege start van intraveneuze BB werd onderzocht als een interventie die de omvang van de necrose kon beperken, maar de resultaten waren niet doorslaggevend. In afwezigheid van reperfusie is het moeilijk om een voordeel te vinden in het beperken van de omvang van de necrose. In het tijdperk van de farmacologische reperfusie (fibrinolyse) was intraveneuze atenolol in een gerandomiseerde studie niet doeltreffend om de omvang van het infarct te verminderen.60 Een andere niet-gerandomiseerde studie toonde echter aan dat intraveneuze metoprolol geassocieerd was met een kleinere omvang van het infarct.61 De eerste klinische studie over deze kwestie bij patiënten die door primaire angioplastie werden gereperfundeerd, was de METOCARD-CNIC studie, uitgevoerd in Spanje.62 In deze studie werd de toediening van metoprolol geassocieerd met een kleinere infarctomvang53 en een hogere LVEF op lange termijn.63 Een andere studie die daarop volgde, de EARLY-BAMI studie, kon de cardioprotectieve effecten van vroegtijdige toediening van metoprolol bij patiënten met AMI die primaire angioplastie ondergingen, niet bevestigen.64 Het verschil tussen de 2 onderzoeken lijkt te wijten te zijn aan het tijdstip van toediening van metoprolol (veel vroeger in METOCARD-CNIC), want hoe langer de tijd tussen de intraveneuze toediening van metoprolol en de reperfusie, des te groter het cardioprotectieve effect.65 Het mechanisme dat ten grondslag ligt aan het vermogen van metoprolol om de infarctgrootte te verminderen wanneer het vroeg vóór de reperfusie intraveneus wordt toegediend, lijkt een direct effect te hebben op de circulerende neutrofielen en hun aggregatie met bloedplaatjes, wat resulteert in verminderde reperfusieschade en verminderde microvasculaire obstructie.66
Het vroege gebruik van intraveneuze BB’s bij AMI is ter discussie gesteld vanwege het potentiële vermogen om de incidentie van cardiogene shock te verhogen. Deze bezorgdheid is gebaseerd op de resultaten van de COMMIT-studie.54 In deze studie werd de vroege toediening van metoprolol aan patiënten met AMI geassocieerd met een significante vermindering van ventrikelfibrilleren, maar een toename van shock. De COMMIT-populatie omvatte echter patiënten met gevorderde ziekte. Bovendien onderging de helft geen reperfusie. Bovendien hadden de patiënten die cardiogene shock ontwikkelden duidelijke tekenen van acute HF samen met tachycardie en hypotensie. Daarentegen heeft een meta-analyse die alle trials omvatte waarbij vroegtijdig intraveneuze BB’s werden toegediend, wat neerkwam op meer dan 73.000 patiënten, aangetoond dat deze strategie veilig is indien toegepast op patiënten zonder tekenen van HF en ook de frequentie van ventrikelfibrilleren aanzienlijk vermindert.67
Op basis van de nieuwe trials uitgevoerd bij patiënten die primaire angioplastiek ondergingen, bevelen de ESC-richtlijnen voor de behandeling van patiënten met AMI met ST-segmentstijging het vroege gebruik van intraveneuze BB’s (klasse IIa A) aan bij afwezigheid van HF-tekenen of systolische hypotensie (
mmHg).68Houding bètablokkers na infarct
Het gebruik van BB’s na AMI is in het prereperfusietijdperk uitvoerig onderzocht.58 Afgezien van de COMMIT-studie54 , met een follow-up van slechts 1 maand, is de enige klinische studie waarin de rol van orale onderhouds-BB’s na AMI is onderzocht, de CAPRICORN-studie.16 In deze studie werden 1950 post-AMI-patiënten met LVEF ≤ 40% gerandomiseerd naar carvedilol of placebo. BB-gebruik werd geassocieerd met een verlaging van de totale mortaliteit.16 Omdat veel van de trials gericht op HFrEF (tabel 1) post-AMI-patiënten includeerden, wordt aangenomen dat alle patiënten die een AMI hebben doorgemaakt met een LVEF ≤ 40% een indicatie hebben voor BB’s. Er is echter een gebrek aan bewijs over de voordelen van BBs voor post-AMI-patiënten met een LVEF> 40%. Talrijke observationele studies hebben geprobeerd licht te werpen op deze kwestie, maar hebben allemaal grote beperkingen en bieden dus geen definitieve informatie (een aspect dat is beoordeeld door Ibáñez et al.1).
Gezien al het bovenstaande bevelen de ESC-richtlijnen voor klinische praktijk voor patiënten met AMI sterk (klasse IA) BB-gebruik aan wanneer de LVEF ≤ 40% is, ongeacht of patiënten ST-segment of non-ST-segment elevatie AMI hebben. De aanbeveling voor patiënten die een AMI hebben gehad met een LVEF> 40% is echter zwakker.1
Figuur 4 toont de klinische situaties met bewezen voordeel van BB’s in de context van AMI.
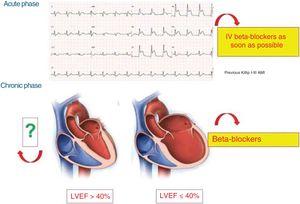
Huidige status van bètablokkers in de verschillende fasen van het acuut coronair syndroom. AMI, acuut myocardinfarct; IV, intraveneus; LVEF, linker ventrikel ejectiefractie.
Wegens dit gebrek aan bewijs over een zo belangrijk aspect van de dagelijkse klinische zorg, zijn in Europa 3 grote pragmatische klinische studies aan de gang om de rol van BB’s te onderzoeken bij patiënten zonder verminderde LVEF die een AMI hebben gehad. Aan de REBOOT klinische studie (NCT03596385), die wordt geleid door het National Center for Cardiovascular Research (CNIC) in Spanje, wordt deelgenomen door meer dan 70 Spaanse en Italiaanse centra. Ongeveer 8500 post-AMI patiënten met LVEF> 40% zullen worden geïncludeerd in deze grote Spaanse studie. Bovendien worden de REDUCE-SWEDEHEART (NCT03278509) en BETAMI (NCT03646357) studies uitgevoerd in respectievelijk Zweden en Noorwegen; hun opzet is vergelijkbaar met die van REBOOT. Deze grote klinische proeven zullen een duidelijke invloed hebben op de klinische praktijk in deze setting.
Tabel 3 geeft een overzicht van de resultaten van de verschillende klinische proeven16,53,54,60,64,69-72 waarin de rol van BB’s is geanalyseerd, hetzij in de acute fase van AMI of in de onderhoudsperiode na de acute gebeurtenis.
Belangrijkste trials over het gebruik van bètablokkers bij acuut coronair syndroom
| Studie (y) | Reperfusie | Drug | Nr. | Criteria | Resultaten |
|---|---|---|---|---|---|
| Intraveneuze toediening in acute fase | |||||
| ISIS-I69 (1986)* | Geen | Atenolol | 16 027 | Verwachte AMI op elke plaats | 15% reductie in mortaliteit |
| MIAMI70 (1985)* | Geen | Metoprolol | 5778 | Verdenking AMI op elke | 29% reductie in mortaliteit |
| MILIS71 (1986) | Nee | Propranolol | 269 | Verwachte AMI op elke plaats | Geen reductie in mortaliteit of AMI-grootte |
| Van de Werf et al.60 (1993) | Ja (fibrinolyse) | Atenolol | 292 | Verwachte AMI op elke plaats | Geen reductie in mortaliteit of AMI grootte |
| METOCARD-CNIC53 (2013)* | Ja (angioplastiek) | Metoprolol | 270 | Verdenking van eerdere AMI | Vermindering van AMI-grootte en vervolgens toename van LVEF |
| EARLY-BAMI64 (2016) | Ja (angioplastiek) | Metoprolol | 683 | Verdenking op AMI op elke locatie | Geen afname in infarctgrootte |
| Chronische toediening na infarct | |||||
| BHAT72 (1982)* | Nee | Propranolol | 3837 | Infarct op elke plaats | 26% reductie in mortaliteit |
| CAPRICORN16 (2001)* | Ja (fibrinolyse) | Carvedilol | 1959 | Infarct op elke plaats en LVEF ≤ 40% | 23% reductie in mortaliteit |
| COMMIT54 (2005) | Fibrinolyse: 54% van de steekproef; 46% niet gereperfundeerd | Metoprolol | 45 852 | Infarct op elke locatie zonder LVEF-beperking | Geen reductie in mortaliteit. |
AMI, acuut myocardinfarct; LVEF, linker ventrikel ejectiefractie; VF, ventriculair fibrilleren.
Studies met positieve (gunstige) resultaten voor bètablokkers.
Stabiele ischemische hartziekte
De antianginale effecten van BB’s zijn goed vastgesteld en zijn opgenomen in de richtlijnen voor de klinische praktijk.73 Vergeleken met calciumkanaalblokkers verminderen BB’s angina-episoden en de tijd tot het begin van ischemie bij inspanningstests.74 Er is echter geen klinische studie verricht waarin op gerandomiseerde wijze en met voldoende statistische power is onderzocht of BB’s de overleving van patiënten met stabiele coronaire ziekte maar zonder AMI of rEF verbeteren. In een systematische review en meta-analyse bleek het gebruik ervan de mortaliteit niet te verminderen.75 Het REACH-register, dat meer dan 40 000 Zweedse patiënten omvatte, vond na propensity score adjustment geen voordeel bij patiënten met stabiele coronaire ziekte maar zonder eerdere AMI. Verschillende onderzoeken ondersteunen de conclusie dat, in aanwezigheid van stabiele coronaire ziekte en zonder eerdere AMI, BB-gebruik geen gunstige effecten heeft op mortaliteit en ongunstige cardiovasculaire gebeurtenissen.76
CONCLUSIES
BB’s zijn een groep geneesmiddelen die deel uitmaken van het standaard therapeutische arsenaal voor verschillende cardiovasculaire aandoeningen. Hun voordelen bij patiënten met HF en ventrikeldisfunctie zijn duidelijk vastgesteld, evenals hun antiaritmische effecten. In de context van AMI vermindert de vroege toediening van intraveneuze BB’s de incidentie van ventrikelfibrilleren en kan zij de infarctgrootte verminderen, hoewel nog moet worden aangetoond of dit zich vertaalt in een verbetering van de morbiditeit en mortaliteit op lange termijn. Het voordeel van chronische BB’s bij patiënten zonder ventrikeldisfunctie die een AMI hebben doorgemaakt, is niet vastgesteld. Hoewel ze in het verleden vaak werden gebruikt, heeft de rol van BBs bij patiënten met hypertensie zonder andere comorbiditeiten aan belang ingeboet. Ondanks meer dan 4 decennia gebruik van BB’s zijn er nog steeds klinische en experimentele vragen die moeten worden opgelost, hetgeen deze groep geneesmiddelen tot een van de meest fascinerende maakt waarover wij beschikken.
FONDSEN
B. Ibáñez leidt projecten met betrekking tot het onderwerp van deze review voor de Spaanse Vereniging voor Cardiologie (2017 Translational Research Project) en het MICINN (Spaanse Ministerie van Wetenschap, Innovatie en Universiteiten) via het Instituto de Salud Carlos III Health Research Fund (PI16/02110) en het Europees Fonds voor Regionale Ontwikkeling (EFRO: SAF2013-49663-EXP). Het CNIC (Nationaal Centrum voor Cardiovasculair Onderzoek) wordt gefinancierd door het MICINN, het ISCiii, en de ProCNIC Foundation en is een Severo Ochoa Center of Excellence (SEV-2015-0505).
CONFLICTS OF INTEREST
None declared.