Introduction
Volgens de Wereldgezondheidsorganisatie treft depressie wereldwijd naar schatting 350 miljoen mensen (Organization, 2017). Patiënten met een depressie vertonen symptomen van angststoornissen en gaan gepaard met een onvermogen om plezier en interesse te ervaren, concentratieverlies, zelftwijfel, sociale angst, slaap- en eetluststoornissen (Namola et al., 2015). De belangrijkste factoren die depressie veroorzaken zijn chemische stoffen of hormonen die uit balans zijn in de hersenen. Het belangrijkste hormoon dat in verband wordt gebracht met depressie is serotonine. Andere hormonen zijn noradrenaline en dopamine (Yi et al., 2008). Deze hormonen zijn nodig voor een normale hersenfunctie en om gevoelens te controleren. De vernietiging van deze hormonen kan chemische onbalans in de hersenen veroorzaken met depressie tot gevolg.
Depressie kan, afhankelijk van de ernst ervan, worden behandeld met psychotherapie of medicatie. Antidepressiva zijn de belangrijkste soorten medicatie die worden gebruikt om depressie te behandelen. Er zijn veel verschillende soorten antidepressiva beschikbaar, en ze verschillen alleen in de manier waarop ze op de hersenen inwerken, hun kosten en hun bijwerkingenprofiel. In de eerstelijnsbehandeling krijgen de meeste patiënten ofwel een tricyclisch antidepressivum (TCA) ofwel een selectieve serotonine heropname remmer (SSRI; McCarthy e.a., 2016) voorgeschreven. De middelen die veel gebruikt worden voor angstbehandelingen zijn benzodiazepinen. Hoewel er veel antidepressiva op de markt zijn die gebruikt worden om depressie te behandelen, zijn de nawerkingen van het gebruik van deze middelen een grote bron van zorg (Binfaré et al., 2009). Een alternatieve therapie van depressie is het gebruik van kruidengeneesmiddelen (Fajemiroye et al., 2016). Het gebruik van kruidenextracten wordt steeds breder geaccepteerd door de medische wereld en door patiënten. De meerderheid van de kruidengeneesmiddelen die worden gebruikt voor de behandeling van depressie zijn ruwe of gehalveerde extracten (Calixto et al., 2000; Carlini, 2003; Guan en Liu, 2016).
Er is schaarste in rapporten over onderzoek waarbij het actieve principe is betrokken dat in staat is om activiteit op het centrale zenuwstelsel (CZS) te induceren. Een review van Carlini (2003) bevat alleen informatie over psychoanaleptische, psycholeptische, en psychodysleptische effecten. Een recente review van Guan en Liu (2016) besprak de structuur-activiteitsrelatie van de antidepressieve effecten van flavonoïden geïsoleerd uit natuurlijke en synthetische bronnen. Synthetische indoolalkaloïden, hun activiteit, en potentieel gebruik in de geneeskunde zijn al in verschillende artikelen besproken (de Sa et al., 2009). Er is echter nog geen overzichtsartikel gepubliceerd waarin de geïsoleerde indoolalkaloïden uit planten in verband worden gebracht met antidepressieve activiteit. Dit overzicht geeft informatie over het potentieel van natuurlijke indoolalkaloïden voor de behandeling van neurologische stoornissen, structuur-activiteitsrelatie studies, en de mate waarin deze andere bioactieve metabolieten als potentiële antidepressieve drug leads vanuit het perspectief van de chemische structuur. Het is samengesteld door bibliografisch onderzoek van wetenschappelijke tijdschriften en relevante literatuur geïdentificeerd via Web of Science elektronische databases.
Antidepressieve Planten
Dit overzichtsartikel handelt over planten die activiteit bezitten op het CZS. Hoewel vele soorten planten in deze categorie vallen, zullen we alleen planten belichten die antidepressieve eigenschappen vertonen. Twee planten die indoolalkaloïden bevatten zijn Passiflora incarnata L. (passiebloem) en Mitragyna speciosa (Korth.) Havil (kratom), terwijl de andere twee planten die geen indoolalkaloïden vertoonden, Piper methysticum G. Forst (kava) en Valeriana officinalis L., speciale aandacht verdienen. De chemische structuur van geïsoleerde verbindingen uit deze planten kan worden gebruikt als basis voor de ontwikkeling van nieuwe geneesmiddelen.
Passiflora incarnata en andere soorten zoals P. alata Curtis, P. coerulea L. en P. edulis Sims worden veel gebruikt als kalmerend middel in de traditionele geneeskunde in de meeste Europese landen en in Amerika (Houghton en Seth, 2003). De structuur van benzodiazepinen bestaat uit een benzeenring die versmolten is met een diazepinesysteem dat bestaat uit een zevenhoekig heterocyclisch deel met twee stikstofatomen op posities 1 en 2 van de ring. Indoolalkaloïden geïsoleerd uit P. incarnata namelijk harman, harmol, harmine, harmalol en harmaline bestaan uit een benzeenring gefuseerd met een vijflidige heterocyclus die één stikstofatoom bevat.
Verschillende studies hebben aangegeven dat P. incarnata een farmacologisch profiel heeft dat vergelijkbaar is met benzodiazepinen en werkt via gamma-aminoboterzuur (GABA) receptoren (Jawna-Zboiñska et al., 2016). De bladeren van M. speciosa zijn gebruikt als traditioneel medicijn om diarree, diabetes te behandelen en de bloedcirculatie te verbeteren (Vicknasingam et al., 2010). Mitragynine is de belangrijkste indoolalkaloïde die aanwezig is in M. speciosa met zijn analogen, speciogynine, paynantheine en speciociliatine (León et al., 2009). Twee studies uitgevoerd naar het waterige extract en het alkaloïde extract van M. speciosa induceerden een antidepressivum-achtig effect op muizenmodellen van gedragsstoornis (Kumarnsit et al., 2007). Een studie uitgevoerd door Idayu et al. (2011) over mitragynine toont het effect van antidepressiva aan in dierlijke gedragsmodellen van depressie door de interactie met de hypothalamus-hypofyse-bijnier (HPA) as in het neuro-endocriene systeem (Idayu et al., 2011).
Piper methysticum G. Forst wordt geconsumeerd als een drank genaamd kava die een aangename mentale toestand opwekt in de richting van een opgewekt gevoel terwijl het vermoeidheid en angst vermindert (Bilia et al., 2002). De studie toont aan dat de meeste farmacologische activiteiten behouden blijven in het vetoplosbare extract vergeleken met het waterige extract. Het vetoplosbare extract bevat ten minste zeven pyrones, bekend als kavalactone. Kavalactonen werken in het algemeen in op de dopaminerge, serotonine-, gamma-aminoboterzuur (GABA) en glutamaterge neurotransmissie, voorkomen monoamine-oxidase B (MOB) en hebben ook een aantal effecten op ionenkanalen (Grunze et al., 2001). Dihydromethysticine is een van de zes belangrijkste kavalactonen die in de kava plant gevonden worden. De structuur van dihydromethysticine bestaat uit een arylethyleen-α-pyron gebonden aan een indoolachtig deel met twee oxygenen in plaats van nitrogenen. Het draagt bij tot de anxiolytische activiteit en werkt als antidepressivum. Dubbelblind placebo-gecontroleerd onderzoek heeft aangetoond dat kavalactonen een anxiolytische werking hebben zonder de mentale en motorische functies te onderdrukken en de kwaliteit van de slaap verbeteren. Kavalactonen is een alternatief om het gebruik van benzodiazepinen in depressietherapie te vervangen (Malsch en Kieser, 2001).
Valeriana officinalis L., ook bekend als valeriaan wordt in veel landen veel gebruikt als kalmerend middel, anticonvulsivum, voor hypnotiserende effecten, en anxiolytische activiteit (Ghaderi en Jafari, 2014). Valerenic zuur en valepotriaten zijn gerapporteerd als actieve ingrediënten in farmaceutische preparaten en valeriaan commerciële ruwe extracten zijn geregistreerd gebruik in vele landen (Bos et al., 2002). Valepotriaten, die bestaan uit triësters van polyhydroxycyclopenta-(c)-pyranen met de carbonzuren: azijnzuur, valeriaanzuur, isovaleriaanzuur, α-isovaleroxy-isovaleriaanzuur, β-methylvaleriaanzuur, β-acetoxy-isovaleriaanzuur, β-hydroxyisovaleriaanzuur en β-acetoxy-β-methylvaleriaanzuur, worden gebruikt als kalmeringsmiddel. Valepotriaten zijn onstabiel, thermolabiel en ontleden snel onder zure of alkalische omstandigheden in water, alsook in alcoholische oplossingen (Bos et al., 2002). Valepotriaten zijn nuttig bij het verbeteren van de omstandigheden bij dieren en mensen tijdens het ontwennen van benzodiazepinen (Poyares et al, 2002).
Hoewel er een verscheidenheid is aan verschillende chemische bestanddelen, wordt het werkingsmechanisme gerapporteerd als interactie van valeriaan met het GABA-systeem in de hersenen door remming van GABA-transaminase, de interactie met de GABA-receptor/benzodiazepine en interferentie in de opname en opname rekrutering van GABA in synaptosomen (Sichardt et al., 2007). Verschillende modellen zijn gebruikt om antidepressieve effecten van planten te onderzoeken. Farmacodynamische modellen, waaronder in vitro, in vivo en klinische modellen werden gebruikt om de effecten te beoordelen (Tabel 1). De meeste van de geselecteerde plantensoorten werden in vivo bestudeerd, enkele bestuderen in vitro en alleen kava werd klinisch onderzocht. In alle gevallen moet meer onderzoek worden verricht om de actieve bestanddelen en de meest effectieve dosis vast te stellen en om na te gaan of deze verschilt naargelang de verschillende soorten depressies.

TABLE 1. Informatie van farmacologische studies van beoordeelde planten.
Indole Alkaloïden
Indole alkaloïden hebben een bicyclische structuur, bestaande uit een zeskoppige benzeenring versmolten met een vijfkoppige stikstofhoudende pyrrolring. Deze pyrrolring met stikstofatoom geeft aanleiding tot de basiseigenschappen van indoolalkaloïden die hen bijzonder farmacologisch actief maken (El-Sayed en Verpoorte, 2007). Indoolalkaloïden zijn wijdverspreid in planten die behoren tot de families Apocynaceae, Loganiaceae, Rubiaceae, en Nyssaceae. Belangrijke indoolalkaloïden die uit planten zijn geïsoleerd, zijn onder meer het antihypertensivum reserpine uit Rauvolfia serpentina (Sagi et al., 2016) en de krachtige antitumormiddelen vinblastine en vincristine uit Catharanthus roseus (El-Sayed en Verpoorte, 2007). Onderzoek naar de effectiviteit van indoolalkaloïden bij de behandeling van depressie is niet nieuw en wordt al sinds 1952 uitgevoerd, maar momenteel is er door de wetenschappelijke gemeenschap zeer weinig aandacht besteed aan de voordelen van het therapeutisch nut van planten begiftigd met antidepressieve eigenschappen.
Indole alkaloïden worden vaak in verband gebracht met de functie van G-eiwitreceptoren, in het bijzonder voor neuronale signaaloverdracht via receptoren voor serotonine (5-HT/hydroxytryptamine). Afgezien van de waterstofdonor via de vrije N-H, draagt de aanwezigheid van π-elektronendichtheid bij tot de hoogste bezette moleculaire orbitaal (HOMO) energie van het vlakke indoolskelet. Dit maakt interactie mogelijk met nucleobasen, in het bijzonder geprotoneerde atomen, alsook met doeleiwitten (de Sa et al., 2009). De chemische structuur van de neurotransmitter serotonine is gebaseerd op een elektron-rijke aromatische indoolring. De aanwezigheid van een stikstofatoom in de indoolring is om het aromatische systeem in stand te houden en maakt de binding N-H zuur in plaats van stikstof basisch. De indoolring is in staat waterstofbruggen te vormen via het N-H gedeelte en π-π stacking of kation-π interacties, via het aromatische gedeelte (Shimazaki et al., 2009). De hydrofobiciteit van indoolringen is bijna gelijk aan die van de fenylgroep en minder hydrofoob dan de klassieke isosterische benzothiofeen- en benzofuraanring. De N-H indoolgroep speelt een beslissende rol in de interactie met de doelbioreceptor, terwijl gesynthetiseerde benzothiofeen- en benzofuraanderivaten een matige tot beperkte affiniteit voor de doelbioreceptor vertonen (de Sa et al., 2009). Reserpine is een van de voorbeelden van indoolalkaloïden die in de afgelopen 60 jaar zijn geïsoleerd en een sedatieve werking op het CZS vertonen. Overigens zijn twee chemische stoffen, namelijk tryptamine en serotonine, die in de hersenen worden aangetroffen, ook indoolalkaloïde derivaten.
Het is nog onduidelijk welke actieve bestanddelen van plantenextracten verantwoordelijk zijn voor het antidepressieve effect. Daarom proberen we een paar belangrijke chemische structuren te identificeren die geïsoleerd zijn uit plantenextracten die antidepressieve activiteiten vertonen en nagaan welke overeenkomsten er zijn in het skeletpatroon die zouden kunnen bijdragen aan de antidepressieve activiteit. Er zijn al vroeg pogingen gedaan om structurele overeenkomsten te identificeren tussen serotonine en indoolalkaloïden. De meest opvallende overeenkomst bestaat uit zes leden tellende heterocyclische ringen die versmolten zijn met vijf leden tellende ringen. Het verschil zit in de aanwezigheid van een stikstofatoom of de verdeling van π elektronen (figuur 1). Nichols (2012) rapporteerde door middel van een structuur-activiteitsrelatiestudie dat de variatie in activiteit van verschillende soorten moleculen suggereert dat de receptor zeer gevoelig is voor de aard van de tryptamine. Andere chemische verbindingen die met succes zijn geïsoleerd uit antidepressieve planten worden in dit overzichtsartikel genoemd omdat het misschien specifieke agonisten zijn met bepaalde substitutiepatronen die in staat zijn om selectief een subset van effectoren te activeren. Dit fenomeen staat nu bekend als functionele selectiviteit.
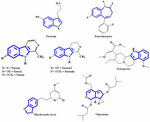
FIGUUR 1. Chemische structuren van serotonine, benzodiazepine en geïsoleerde verbindingen van antidepressieve planten. Gelijkenis in het skeletpatroon, dat bestaat uit zes gelideerde heterocyclische ringen, verbonden met vijf gelideerde ringen.
Serotonine, wordt veel gebruikt in de hersenfunctie en cognitie als endogene receptor agonist (Fink en Göthert, 2007). Serotonine oefent zijn functies uit via zeven families van receptoren (5-HT1-5-HT7) die lid zijn van de G-eiwit gekoppelde receptorfamilie. Van een aantal verbindingen met een indoolgroep is bekend dat zij affiniteit hebben met verschillende serotoninereceptoren (Kochanowska-Karamyan en Hamann, 2010). De structurele gelijkenis van indoolalkaloïden (exogene agonisten) met endogene neurotransmitters zoals serotonine heeft onderzoekers ertoe gebracht de potentiële neurologische activiteit van deze moleculen te voorspellen. Schematische weergave van de processen die gepaard gaan met de neurotransmissie van exogene agonisten is beschreven in figuur 2.
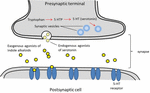
FIGUUR 2. Schematische weergave van de processen die met de neurotransmissie samenhangen. Exogene agonisten van indoolalkaloïden uit planten die qua structuur overeenkomsten vertonen met serotonine, waardoor zij zich kunnen binden aan serotoninereceptoren (5-HT-receptoren).
De indoolring staat ook bekend als bioisosteres en heeft een vergelijkbare chemische en fysische structuur als biologische moleculen. Deze gelijkenis wordt gebruikt bij de ontwikkeling van het prototype van het geneesmiddel dat gericht is op de verbetering van de farmacologische activiteit en de optimalisering van het farmacokinetische profiel. In een andere studie van farmacologische beoordeling van benzofuranen en thienopyrrool leidde dit tot bioisosterische moleculen die dimethyltryptamine-achtige activiteit bezitten. Vroeg werk met benzothiofenen en 3-indenalkylamines toonde aan dat voor verbindingen zonder ringsubstituenten, het vermogen om als agonisten te werken in de ratten fundus ongeveer gelijk was aan tryptamines. De resultaten toonden aan dat de indool NH niet essentieel was om de 5-HT2 receptor in de rat fundus te activeren (Nichols, 2012). Een reeks 2-aryl indool NK1 receptor antagonisten en hun derivaten zijn goede liganden maar hebben een lage orale biologische beschikbaarheid bij ratten. Om de oplosbaarheid en absorptie te verhogen, werd de basische stikstof geïntroduceerd, wat leidde tot het analoog azaindool en verwante verbindingen die dezelfde NK1-bindingsaffiniteit vertonen als de reeks 2-aryl indool NK1-receptorantagonisten (Cooper et al., 2001). Moleculaire docking van 2 fenyl-indool afgeleide liganden met serotonine 5-HT6 en melanocortine-4 receptoren geeft aan dat de geprivilegieerde scaffold kan accommoderen afhankelijk van de aard geconserveerde subpocket en niet-geconserveerde binding pocket. Interacties van niet-geconserveerde delen van de bindingszak zijn verantwoordelijk voor belangrijke verschillen in de moleculaire herkenning door de corresponderende doelreceptor (Bondensgaard et al, 2004).
Volgens de Sa et al. (2009) zijn veel voorkomende indoolalkaloïden uit natuurlijke bronnen tryptofaanaminozuren in de menselijke voeding en de ontdekking van plantenhormonen die therapeutische effecten hebben, zoals ontstekingsremmers, een fosfodiësteraseremmer, 5-HT-receptoragonisten en -antagonisten, cannabinoïde-receptoragonisten en HMG-CoA-reductaseremmers. De indool scaffold heeft bindingspockets en bezit een gemeenschappelijk complementair bindingsdomein met de doelreceptor, die behoort tot een klasse van GPCR’s (G-eiwit belangrijke membraanreceptoren gekoppeld). De meeste geneesmiddelen op de markt bevatten de indool substructuur. Deze omvatten indomethacine, ergotamine, frovatriptan, ondansetron, en tadalafil.
Conclusie
Uit dit overzicht bleek dat een meerderheid van de op planten gebaseerde remedies die werden aangegeven voor de behandeling van psychiatrische aandoeningen, ruw of halfzuiver waren. De resultaten voor in vivo en in vitro varieerden en waren niet reproduceerbaar omdat in verschillende biogeografische regio’s het gehalte aan secundaire metabolieten van de planten correleert met de beschikbaarheid van voedingsstoffen, het klimaat en ecologische omstandigheden. Bovendien kan de bioactiviteit van planten worden bijgedragen door een enkele verbinding of een mengsel van verbindingen. De auteurs suggereren dat de inspanningen om actieve principes te verkrijgen, fytochemische identificatie, en metabolomics studie moeten worden uitgevoerd met inspecties in vitro en in vivo voor een betere karakterisering van plantaardige geneesmiddelen. In de meeste gevallen werd de synthese van indoolalkaloïden geïnspireerd door de natuurlijk voorkomende moleculen en hun gelijkenis met serotonine.
De indoolalkaloïden uit plantaardige bronnen zijn vrij complex in vergelijking met synthetische. Het belang van synthetische indoolalkaloïden is reeds vastgesteld omdat de structuur beschikbaar is in verschillende ligandreceptoren, enzymremmers en modulatoren bioreceptor. Sommige van de natuurlijk voorkomende indoolalkaloïden kunnen niet met de thans bekende methoden worden gesynthetiseerd. Bovendien is de meeste informatie over de werkzaamheid van indoolalkaloïden afkomstig van synthetische indoolalkaloïden. Als gevolg hiervan is het potentieel van veel natuurlijk voorkomende indoolalkaloïden als nieuwe geneesmiddelen voor diverse psychiatrische stoornissen nog steeds onbenut. In het verleden zijn op planten gebaseerde verbindingen de bron geweest van een aantal van de meest succesvolle medicijnaanleidingen of geneesmiddelen die in de geneeskunde worden gebruikt. Dit is een aanwijzing dat er nog meer te ontdekken valt.
Concluderend, verschillende indoolalkaloïden zijn gebruikt als antidepressiva of vormen aanknopingspunten voor de ontwikkeling ervan. Op basis van onze bevindingen bevatten planten een reservoir van indoolalkaloïden die waardevolle aanknopingspunten zijn voor de ontwikkeling van toekomstige antidepressiva.
Author Contributions
HH: Voorbereiden manuscript. MY: Redactie Engels taal en suggereren enkele belangrijke informatie om het manuscript te verbeteren. AR: Bijdragen voor het begrijpen van de schematische van processen geassocieerd met neurotransmissie.
Funding
Support voor dit werk werd verstrekt door Universiti Malaysia Pahang via onderzoek subsidie UMP RDU170302 aan HH.
Conflict of Interest Statement
De auteurs verklaren dat het onderzoek werd uitgevoerd in afwezigheid van enige commerciële of financiële relaties die zouden kunnen worden opgevat als een potentieel belangenconflict.
Bilia, A. R., Gallori, S., en Vincieri, F. F. (2002). Kava-kava en angst: groeiende kennis over de werkzaamheid en veiligheid. Life Sci. 70, 2581-2597. doi: 10.1016/S0024-3205(02)01555-2
PubMed Abstract | CrossRef Full Text | Google Scholar
Binfaré, R. W., Rosa, A. O., Lobato, K. R., Santos, A. R., and Rodrigues, A. L. S. (2009). Toediening van ascorbinezuur veroorzaakt een antidepressivum-achtig effect: bewijs voor de betrokkenheid van monoaminerge neurotransmissie. Prog. Neuropsychopharmacol. Biol. Psychiatry 33, 530-540. doi: 10.1016/j.pnpbp.2009.02.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Bondensgaard, K., Ankersen, M., Thøgersen, H., Hansen, B. S., Wulff, B. S., and Bywater, R. P. (2004). Herkenning van geprivilegieerde structuren door G-eiwit gekoppelde receptoren. J. Med. Chem. 47, 888-899. doi: 10.1021/jm0309452
PubMed Abstract | CrossRef Full Text | Google Scholar
Bos, R., Woerdenbag, H. J., and Pras, N. (2002). Bepaling van valepotriaten. J. Chromatogr. A 967, 131-146. doi: 10.1016/S0021-9673(02)00036-5
CrossRef Full Text | Google Scholar
Calixto, J. B., Beirith, A., Ferreira, J., Santos, A. R., and Yunes, R. A. (2000). Natuurlijk voorkomende antinociceptieve stoffen uit planten. Phytother. Res. 14, 401-418. doi: 10.1002/1099-1573(200009)14:6<401::AID-PTR762>3.0.CO;2-H
PubMed Abstract | CrossRef Full Text | Google Scholar
Carlini, E. (2003). Planten en het centrale zenuwstelsel. Farmacol. Biochem. Behav. 75, 501-512. doi: 10.1016/S0091-3057(03)00112-6
CrossRef Full Text | Google Scholar
Cooper, L. C., Chicchi, G. G., Dinnell, K., Elliott, J. M., Hollingworth, G. J., Kurtz, M. M., et al. (2001). 2-Aryl indool NK 1 receptor antagonisten: optimalisatie van de indool substitutie. Bioorg. Med. Chem. Lett. 11, 1233-1236. doi: 10.1016/S0960-894X(01)00182-2
CrossRef Full Text | Google Scholar
de Sa, A., Fernando, R., Barreiro, E. J., Fraga, M., and Alberto, C. (2009). From nature to drug discovery: the indole scaffold as a ‘privileged structure’. Mini Rev. Med. Chem. 9, 782-793. doi: 10.2174/138955709788452649
CrossRef Full Text | Google Scholar
El-Sayed, M., and Verpoorte, R. (2007). Catharanthus terpenoid indole alkaloids: biosynthese en regulatie. Phytochem. Rev. 6, 277-305. doi: 10.1007/s11101-006-9047-8
CrossRef Full Text | Google Scholar
Fajemiroye, J. O., Silva, D. M., Oliveira, D. R., and Costa, E. A. (2016). Behandeling van angst en depressie: medicinale planten in retrospect. Fundam. Clin. Farmacol. 30, 198-215. doi: 10.1111/fcp.12186
PubMed Abstract | CrossRef Full Text | Google Scholar
Fiebich, B. L., Knörle, R., Appel, K., Kammler, T., and Weiss, G. (2011). Pharmacological studies in an herbal drug combination of St. John’s Wort (Hypericum perforatum) and passion flower (Passiflora incarnata): in vitro and in vivo evidence of synergy between Hypericum and Passiflora in antidepressant pharmacological models. Fitoterapia 82, 474-480. doi: 10.1016/j.fitote.2010.12.006
PubMed Abstract | CrossRef Full Text | Google Scholar
Fink, K. B., and Göthert, M. (2007). 5-HT receptor regulatie van neurotransmitter afgifte. Pharmacol. Rev. 59, 360-417. doi: 10.1124/pr.59.07103
CrossRef Full Text | Google Scholar
Ghaderi, N., and Jafari, M. (2014). Efficiënte plantenregeneratie, genetische trouw en accumulatie op hoog niveau van twee farmaceutische verbindingen in geregenereerde planten van Valeriana officinalis L. S. Afr. J. Bot. 92, 19-27. doi: 10.1016/j.sajb.2014.01.010
CrossRef Full Text | Google Scholar
Grunze, H., Langosch, J., Schirrmacher, K., Bingmann, D., Von Wegerer, J., and Walden, J. (2001). Kava pyrones exert effecten op neuronale transmissie en transmembraneous cation currents vergelijkbaar met gevestigde stemming stabilisatoren-een overzicht. Prog. Neuropsychopharmacol. Biol. Psychiatry 25, 1555-1570.
Google Scholar
Guan, L.-P., and Liu, B.-Y. (2016). Antidepressiva-achtige effecten en mechanismen van flavonoïden en verwante analogen. Eur. J. Med. Chem. 121, 47-57. doi: 10.1016/j.ejmech.2016.05.026
PubMed Abstract | CrossRef Full Text | Google Scholar
Hattesohl, M., Feistel, B., Sievers, H., Lehnfeld, R., Hegger, M., and Winterhoff, H. (2008). Extracten van Valeriana officinalis L. sl vertonen anxiolytische en antidepressieve effecten, maar noch sedatieve noch myorelaxerende eigenschappen. Phytomedicine 15, 2-15. doi: 10.1016/j.phymed.2007.11.027
PubMed Abstract | CrossRef Full Text | Google Scholar
Houghton, P. J., and Seth, P. (2003). Planten en het centrale zenuwstelsel. Pharmacol. Biochem. Behav. 75, 497-499. doi: 10.1016/S0091-3057(03)00161-8
CrossRef Full Text | Google Scholar
Idayu, N. F., Hidayat, M. T., Moklas, M., Sharida, F., Raudzah, A. N., Shamima, A., et al. (2011). Antidepressivum effect van mitragynine geïsoleerd uit Mitragyna speciosa Korth in muizenmodel van depressie. Phytomedicine 18, 402-407. doi: 10.1016/j.phymed.2010.08.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Jawna-Zboiñska, K., Blecharz-Klin, K., Joniec-Maciejak, I., Wawer, A., Pyrzanowska, J., Piechal, A., et al. (2016). Passiflora incarnata L. verbetert het ruimtelijk geheugen, vermindert stress, en beïnvloedt de neurotransmissie bij ratten. Phytother. Res. 30, 781-789. doi: 10.1002/ptr.5578
PubMed Abstract | CrossRef Full Text | Google Scholar
Kochanowska-Karamyan, A. J., and Hamann, M. T. (2010). Marine indole alkaloids: potential new drug leads for the control of depression and anxiety. Chem. Rev. 110, 4489-4497. doi: 10.1021/cr900211p
PubMed Abstract | CrossRef Full Text | Google Scholar
Kumarnsit, E., Vongvatcharanon, U., Keawpradub, N., and Intasaro, P. (2007). Fos-like immunoreactivity in rat dorsal raphe nuclei induced by alkaloid extract of Mitragyna speciosa. Neurosci. Lett. 416, 128-132. doi: 10.1016/j.neulet.2007.01.061
PubMed Abstract | CrossRef Full Text | Google Scholar
León, F., Habib, E., Adkins, J. E., Furr, E. B., McCurdy, C. R., and Cutler, S. J. (2009). Phytochemical characterization of the leaves of Mitragyna speciosa grown in USA. Nat. Prod. Commun. 4, 907-910.
PubMed Abstract | Google Scholar
Malsch, U., and Kieser, M. (2001). Efficacy of kava-kava in the treatment of non-psychotic anxiety, following prereatment with benzodiazepines. Psychopharmacology 157, 277-283. doi: 10.1007/s002130100792
PubMed Abstract | CrossRef Full Text
McCarthy, A., Wafford, K., Shanks, E., Ligocki, M., Edgar, D. M., and Dijk, D.-J. (2016). REM slaap homeostase in de afwezigheid van REM slaap: Effecten van antidepressiva. Neuropharmacology 108, 415-425. doi: 10.1016/j.neuropharm.2016.04.047
PubMed Abstract | CrossRef Full Text | Google Scholar
Namola, V., Ratan, P., and Kothiyal, P. (2015). Depressie en rol van mariene biomaterialen: een review. Eur. J. Biomed. Pharm. Sci. 2, 137-148.
Nichols, D. E. (2012). Structuur-activiteitsrelaties van serotonine 5-HT 2A agonisten. WIREs Membr. Transp. Signaling 1, 559-579. doi: 10.1002/wmts.42
CrossRef Full Text | Google Scholar
Organisatie, W. H. (2017). Depressie Factsheet 2016. Beschikbaar op: http://www.who.int/mediacentre/factsheets/fs369/en/
Google Scholar
Poyares, D. R., Guilleminault, C., Ohayon, M. M., and Tufik, S. (2002). Kan valeriaan de slaap verbeteren van slapelozen na benzodiazepineontwenning? Prog. Neuropsychopharmacol. Biol. Psychiatry 26, 539-545.
PubMed Abstract | Google Scholar
Sagi, S., Avula, B., Wang, Y.-H., and Khan, I. A. (2016). Kwantificering en karakterisering van alkaloïden uit wortels van Rauwolfia serpentina met behulp van ultra-high performance liquid chromatography-photo diode array-massaspectrometrie. Anal. Bioanal. Chem. 408, 177-190. doi: 10.1007/s00216-015-9093-4
PubMed Abstract | CrossRef Full Text | Google Scholar
Sarris, J., Kavanagh, D., Byrne, G., Bone, K., Adams, J., and Deed, G. (2009). De Kava Anxiety Depression Spectrum Study (KADSS): een gerandomiseerde, placebo-gecontroleerde cross-over studie met een waterig extract van Piper methysticum. Psychopharmacology 205, 399-407. doi: 10.1007/s00213-009-1549-9
PubMed Abstract | CrossRef Full Text | Google Scholar
Shimazaki, Y., Yajima, T., Takani, M., and Yamauchi, O. (2009). Metaalcomplexen met indoolringen: structuren en effecten van metaal-indool interacties. Coördinatie. Chem. Rev. 253, 479-492. doi: 10.1016/j.ccr.2008.04.012
CrossRef Full Text | Google Scholar
Sichardt, K., Vissiennon, Z., Koetter, U., Brattström, A., and Nieber, K. (2007). Modulation of postsynaptic potentials in rat cortical neurons by valerian extracts macerated with different alcohols: involvement of adenosine A1-and GABAA-receptors. Phytother. Res. 21, 932-937. doi: 10.1002/ptr.2197
PubMed Abstract | CrossRef Full Text | Google Scholar
Vicknasingam, B., Narayanan, S., Beng, G. T., and Mansor, S. M. (2010). Het informele gebruik van ketum (Mitragyna speciosa) voor opioïdenontwenning in de noordelijke staten van het schiereiland Maleisië en implicaties voor drugvervangingstherapie. Int. J. Drug Policy 21, 283-288. doi: 10.1016/j.drugpo.2009.12.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Vijeepallam, K., Pandy, V., Kunasegaran, T., Murugan, D. D., and Naidu, M. (2016). Mitragyna speciosa leaf extract exhibits antipsychotic-like effect with the potential to alleviate positive and negative symptoms of psychosis in mice. Front. Pharmacol. 7:464. doi: 10.3389/fphar.2016.00464
PubMed Abstract | CrossRef Full Text | Google Scholar
Yi, L.-T., Li, J.-M., Li, Y.-C., Pan, Y., Xu, Q., and Kong, L.-D. (2008). Antidepressiva-achtige gedrags- en neurochemische effecten van de met citrusvruchten geassocieerde chemische stof apigenine. Life Sci. 82, 741-751. doi: 10.1016/j.lfs.2008.01.007
PubMed Abstract | CrossRef Full Text | Google Scholar