Nome generico: eritromicina etilsuccinato
Forma farmaceutica: compressa, granulo per sospensione orale
Medicamente rivisto da Drugs.com. Last updated on Feb 1, 2020.
- Overview
- Side Effects
- Dosage
- Professional
- Interactions
- More
Rx only
Per ridurre lo sviluppo di batteri resistenti ai farmaci e mantenere l’efficacia di E.E.S. e altri farmaci antibatterici, E.E.S. dovrebbe essere usato solo per trattare o prevenire infezioni che sono provate o fortemente sospettate di essere causate da batteri.
Descrizione E.E.S.
L’eritromicina è prodotta da un ceppo di Saccharopolyspora erythraea (precedentemente Streptomyces erythraeus) e appartiene al gruppo di antibiotici macrolidi. È basica e forma facilmente sali con gli acidi. La base, il sale stearato e gli esteri sono scarsamente solubili in acqua. L’eritromicina etilsuccinato è un estere dell’eritromicina adatto alla somministrazione orale. L’eritromicina etilsuccinato è conosciuto chimicamente come eritromicina 2′-(etilsuccinato). La formula molecolare è C43H75NO16 e il peso molecolare è 862,06. La formula strutturale è:
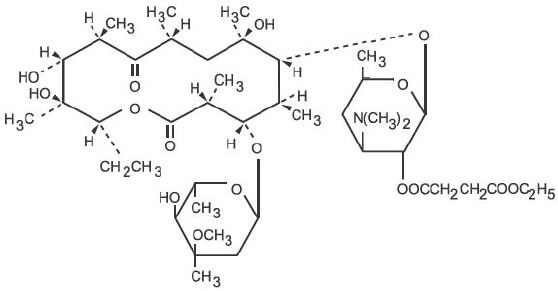
E.E.S. I granuli sono destinati alla ricostituzione con acqua. Ogni cucchiaino da 5 mL di sospensione ricostituita al gusto di ciliegia contiene eritromicina etilsuccinato equivalente a 200 mg di eritromicina.
I liquidi dal sapore gradevole, al gusto di frutta, sono forniti pronti per la somministrazione orale.
E.E.S. 200 liquido: Ogni cucchiaino da 5 mL di sospensione al gusto di frutta contiene eritromicina etilsuccinato equivalente a 200 mg di eritromicina.
E.E.S. 400 liquido: Ogni cucchiaino da 5 mL di sospensione al gusto di arancia contiene eritromicina etilsuccinato equivalente a 400 mg di eritromicina.
Granuli e sospensioni pronte sono intesi principalmente per uso pediatrico ma possono anche essere usati negli adulti.
E.E.S. 400 compresse rivestite con film: Ogni compressa contiene eritromicina etilsuccinato equivalente a 400 mg di eritromicina.
Le compresse rivestite con film sono destinate principalmente agli adulti o ai bambini più grandi.
Ingredienti non attivi
E.E.S. Granuli: Acido citrico, FD&C Red No. 3, magnesio silicato di alluminio, sodio carbossimetilcellulosa, sodio citrato, saccarosio e aroma artificiale.
E.E.S. 400 compresse rivestite con film: Polimeri cellulosici, zucchero per pasticceria (contiene amido di mais), amido di mais, D&C Red No. 30, D&C Yellow No. 10, FD&C Red No. 40, magnesio stearato, polacrilina potassio, polietilenglicole, propilenglicole, sodio citrato, acido sorbico e biossido di titanio.
E.E.S. 200 Liquid: FD&C Rosso No. 40, metilparaben, polisorbato 60, propilparaben, citrato di sodio, saccarosio, acqua, gomma xantana e aromi naturali e artificiali.
E.E.S. 400 liquido: D&C Yellow No. 10, FD&C Yellow No. 6, metilparaben, polisorbato 60, propilparaben, sodio citrato, saccarosio, acqua, gomma xantana e aromi naturali e artificiali.
EES – Farmacologia clinica
Le sospensioni e le compresse rivestite con film di eritromicina etilsuccinato somministrate per via orale vengono assorbite prontamente e in modo affidabile. Livelli sierici comparabili di eritromicina sono raggiunti negli stati di digiuno e non digiuno.
L’eritromicina si diffonde facilmente nella maggior parte dei fluidi corporei. Solo basse concentrazioni sono normalmente raggiunte nel fluido spinale, ma il passaggio del farmaco attraverso la barriera emato-encefalica aumenta nella meningite. In presenza di funzione epatica normale, l’eritromicina è concentrata nel fegato ed escreta nella bile; l’effetto della disfunzione epatica sull’escrezione di eritromicina dal fegato nella bile non è noto. Meno del 5% della dose di eritromicina somministrata per via orale viene escreta in forma attiva nelle urine.
Eritromicina attraversa la barriera placentare, ma i livelli plasmatici fetali sono bassi. Il farmaco viene escreto nel latte umano.
Microbiologia
Meccanismo d’azione
Eritromicina agisce tramite inibizione della sintesi proteica legando le subunità ribosomiali 50S degli organismi suscettibili. Non influisce sulla sintesi dell’acido nucleico.
Resistenza
La principale via di resistenza è la modifica dell’rRNA 23S nella subunità ribosomiale 50S all’insensibilità mentre l’efflusso può anche essere significativo.
Interazioni con altri antimicrobici
L’antagonismo esiste in vitro tra eritromicina e clindamicina, lincomicina e cloramfenicolo.
Attività antimicrobica
L’eritromicina ha dimostrato di essere attiva contro la maggior parte degli isolati dei seguenti microorganismi sia in vitro che in infezioni cliniche.
Batteri aerobi
Batteri Gram-positivi:
Corynebacterium diphtheriae
Corynebacterium minutissimum
Listeria monocytogenes
Staphylococcus aureus (organismi resistenti possono emergere durante il trattamento)
Streptococcus pneumoniae
Streptococcus pyogenes
Batteri Gram-negativi:
Bordetella pertussis
Haemophilus influenzae
Legionella pneumophila
Neisseria gonorrhoeae
Altri microorganismi:
Chlamydia trachomatis
Entamoeba histolytica
Mycoplasma pneumoniae
Treponema pallidum
Ureaplasma urealyticum
I seguenti dati in vitro sono disponibili, ma il loro significato clinico è sconosciuto. Almeno il 90% dei seguenti batteri mostra una concentrazione minima inibitoria (MIC) in vitro inferiore o uguale al breakpoint di suscettibilità per l’eritromicina contro isolati di genere o gruppo di organismi simili. Tuttavia, l’efficacia dell’eritromicina nel trattamento delle infezioni cliniche causate da questi batteri non è stata stabilita in studi clinici adeguati e ben controllati.
Batteri aerobi
Batteri Gram-positivi:
Streptococchi del gruppo Viridans
Batteri Gram-negativi:
Moraxella catarrhalis
Test di suscettibilità
Per informazioni specifiche riguardanti i criteri interpretativi del test di suscettibilità e metodi di test associati e standard di controllo qualità riconosciuti dalla FDA per questo farmaco, vedere: https://www.fda.gov/STIC.
Indicazioni e uso per EES
Per ridurre lo sviluppo di batteri resistenti ai farmaci e mantenere l’efficacia di E.E.S. e altri farmaci antibatterici, E.E.S. deve essere usato solo per trattare o prevenire infezioni che sono provate o fortemente sospettate di essere causate da batteri sensibili. Quando sono disponibili informazioni sulla coltura e sulla suscettibilità, queste dovrebbero essere considerate nella selezione o nella modifica della terapia antibatterica. In assenza di tali dati, l’epidemiologia locale e i modelli di suscettibilità possono contribuire alla selezione empirica della terapia.
E.E.S. è indicato nel trattamento delle infezioni causate da ceppi suscettibili degli organismi designati nelle malattie elencate di seguito:
Infezioni del tratto respiratorio superiore di grado lieve o moderato causate da Streptococcus pyogenes, Streptococcus pneumoniae, o Haemophilus influenzae (quando usato in concomitanza con dosi adeguate di sulfamidici, poiché molti ceppi di H. influenzae non sono suscettibili alle concentrazioni di eritromicina normalmente raggiunte). (Vedere l’etichettatura appropriata della sulfamidica per informazioni sulla prescrizione.)
Infezioni del tratto respiratorio inferiore di gravità da lieve a moderata causate da Streptococcus pneumoniae o Streptococcus pyogenes.
Listeriosi causata da Listeria monocytogenes.
Pertussis (pertosse) causata da Bordetella pertussis. L’eritromicina è efficace nell’eliminare l’organismo dal rinofaringe degli individui infetti rendendoli non infettivi. Alcuni studi clinici suggeriscono che l’eritromicina può essere utile nella profilassi della pertosse in individui esposti suscettibili.
Infezioni del tratto respiratorio dovute a Mycoplasma pneumoniae.
Infezioni della pelle e della struttura della pelle di gravità da lieve a moderata causate da Streptococcus pyogenes o Staphylococcus aureus (stafilococchi resistenti possono emergere durante il trattamento).
Difterite: Infezioni dovute a Corynebacterium diphtheriae, come aggiunta all’antitossina, per prevenire la formazione di portatori e per eradicare l’organismo nei portatori.
Eritrasma: Nel trattamento delle infezioni dovute a Corynebacterium minutissimum.
Amebiasi intestinale causata da Entamoeba histolytica (solo eritromicina orale). L’amebiasi extraenterica richiede il trattamento con altri agenti.
Malattia infiammatoria pelvica acuta causata da Neisseria gonorrhoeae: Come farmaco alternativo nel trattamento della malattia infiammatoria pelvica acuta causata da N. gonorrhoeae in pazienti donne con una storia di sensibilità alla penicillina. I pazienti devono avere un test sierologico per la sifilide prima di ricevere eritromicina come trattamento della gonorrea e un test sierologico di follow-up per la sifilide dopo 3 mesi.
Sifilide causata da Treponema pallidum: Eritromicina è una scelta alternativa di trattamento per la sifilide primaria in pazienti allergici alle penicilline. Nel trattamento della sifilide primaria, gli esami del liquido spinale devono essere fatti prima del trattamento e come parte del follow-up dopo la terapia.
Le eritromicine sono indicate per il trattamento delle seguenti infezioni causate da Chlamydia trachomatis: congiuntivite del neonato, polmonite dell’infanzia e infezioni urogenitali durante la gravidanza. Quando le tetracicline sono controindicate o non tollerate, l’eritromicina è indicata per il trattamento delle infezioni uretrali, endocervicali o rettali non complicate negli adulti dovute a Chlamydia trachomatis.
Quando le tetracicline sono controindicate o non tollerate, l’eritromicina è indicata per il trattamento delle uretriti non gonococciche causate da Ureaplasma urealyticum.
Malattia dei legionari causata da Legionella pneumophila: Anche se non sono stati condotti studi controllati di efficacia clinica, in vitro e limitati dati clinici preliminari suggeriscono che l’eritromicina può essere efficace nel trattamento della malattia dei legionari.
Profilassi
Prevenzione degli attacchi iniziali di febbre reumatica
La penicillina è considerata dall’American Heart Association il farmaco di scelta nella prevenzione degli attacchi iniziali di febbre reumatica (trattamento delle infezioni da Streptococcus pyogenes del tratto respiratorio superiore, ad es, tonsillite o faringite). L’eritromicina è indicata per il trattamento di pazienti allergici alla penicillina.1 La dose terapeutica deve essere somministrata per 10 giorni.
Prevenzione degli attacchi ricorrenti di febbre reumatica
Penicillina o sulfamidici sono considerati dall’American Heart Association i farmaci di scelta nella prevenzione degli attacchi ricorrenti di febbre reumatica. Nei pazienti allergici alla penicillina e ai sulfamidici, l’American Heart Association raccomanda l’eritromicina orale nella profilassi a lungo termine della faringite streptococcica (per la prevenzione degli attacchi ricorrenti di febbre reumatica).1
Contraindicazioni
Eritromicina è controindicata nei pazienti con ipersensibilità conosciuta a questo antibiotico.
Eritromicina è controindicata nei pazienti che prendono terfenadina, astemizolo, pimozide o cisapride (vedi PRECAUZIONI – Interazioni farmacologiche).
Non usate eritromicina in concomitanza con inibitori di HMG CoA reductase (statine) che sono ampiamente metabolizzati da CYP 3A4 (lovastatin o simvastatin), a causa del rischio aumentato di miopatia, incluso rabdomiolisi.
Avvertenze
Epatotossicità
Sono stati riportati casi di disfunzione epatica, incluso aumento degli enzimi epatici, ed epatite epatocellulare e/o colestatica, con o senza ittero, in pazienti che ricevono prodotti di eritromicina orale.
Prolungamento del QT
Eritromicina è stata associata con prolungamento dell’intervallo QT e casi poco frequenti di aritmia. Casi di torsades de pointes sono stati riportati spontaneamente durante la sorveglianza post-marketing in pazienti che ricevono eritromicina. Sono stati riportati casi mortali. L’eritromicina deve essere evitata in pazienti con noto prolungamento dell’intervallo QT, pazienti con condizioni proaritmiche in corso come ipokaliemia non corretta o ipomagnesiemia, bradicardia clinicamente significativa, e in pazienti che ricevono agenti antiaritmici di classe IA (chinidina, procainamide) o classe III (dofetilide, amiodarone, sotalolo). I pazienti anziani possono essere più suscettibili agli effetti associati al farmaco sull’intervallo QT.
Sifilide in gravidanza
Ci sono stati rapporti che suggeriscono che l’eritromicina non raggiunge il feto in concentrazione adeguata per prevenire la sifilide congenita. I bambini nati da donne trattate durante la gravidanza con eritromicina orale per sifilide precoce devono essere trattati con un appropriato regime di penicillina.
Diarrea associata a Clostridium difficile
La diarrea associata a Clostridium difficile (CDAD) è stata riportata con l’uso di quasi tutti gli agenti antibatterici, incluso E.E.S., e può variare in gravità da diarrea lieve a colite fatale. Il trattamento con agenti antibatterici altera la flora normale del colon portando alla crescita eccessiva di C. difficile.
C. difficile produce tossine A e B che contribuiscono allo sviluppo di CDAD. I ceppi di C. difficile che producono ipertossine causano una maggiore morbilità e mortalità, poiché queste infezioni possono essere refrattarie alla terapia antimicrobica e possono richiedere la colectomia. La CDAD deve essere considerata in tutti i pazienti che presentano diarrea dopo l’uso di antibiotici. È necessaria un’attenta anamnesi poiché è stato riportato che la CDAD si verifica oltre due mesi dopo la somministrazione di agenti antibatterici.
Se la CDAD è sospettata o confermata, può essere necessario interrompere l’uso di antibiotici in corso non diretti contro il C. difficile. La gestione appropriata dei fluidi e degli elettroliti, l’integrazione di proteine, il trattamento antibiotico di C. difficile e la valutazione chirurgica devono essere istituiti come clinicamente indicato.
Interazioni farmacologiche
Sono state riportate gravi reazioni avverse in pazienti che assumono eritromicina in concomitanza con substrati CYP3A4. Questi includono tossicità con colchicina; rabdomiolisi con simvastatina, lovastatina e atorvastatina; e ipotensione con bloccanti dei canali del calcio metabolizzati dal CYP3A4 (es, verapamil, amlodipina, diltiazem) (vedi PRECAUZIONI – Interazioni farmacologiche).
Ci sono state segnalazioni post-marketing di tossicità da colchicina con uso concomitante di eritromicina e colchicina. Questa interazione è potenzialmente pericolosa per la vita e può verificarsi durante l’uso di entrambi i farmaci alle dosi raccomandate (vedi PRECAUZIONI – Interazioni farmacologiche).
Rabdomiolisi con o senza insufficienza renale è stata riportata in pazienti gravemente malati che ricevono eritromicina in concomitanza con lovastatina. Pertanto, i pazienti che ricevono lovastatina ed eritromicina in concomitanza devono essere attentamente monitorati per la creatina chinasi (CK) e i livelli di transaminasi nel siero. (Vedi foglietto illustrativo per lovastatina.)
Precauzioni
Generale
Prescrivere E.E.S. in assenza di un’infezione batterica provata o fortemente sospettata o di un’indicazione profilattica è improbabile che fornisca beneficio al paziente e aumenta il rischio di sviluppo di batteri resistenti ai farmaci.
Siccome l’eritromicina è principalmente escreta dal fegato, deve essere esercitata cautela quando l’eritromicina è somministrata a pazienti con funzione epatica compromessa (vedi sezioni FARMACOLOGIA CLINICA e AVVERTENZE).
Esacerbazione di sintomi di miastenia gravis e nuova insorgenza di sintomi di sindrome miastenica sono stati riportati in pazienti che ricevono terapia con eritromicina.
Ci sono stati rapporti di stenosi pilorica ipertrofica infantile (IHPS) che si verificano in neonati dopo terapia con eritromicina. In una coorte di 157 neonati che sono stati dati eritromicina per la profilassi della pertosse, sette neonati (5%) hanno sviluppato sintomi di vomito non-bilious o irritabilità con l’alimentazione e sono stati successivamente diagnosticati come aventi IHPS che richiedono pyloromyotomy chirurgico. Un possibile effetto dose-risposta è stato descritto con un rischio assoluto di IHPS del 5,1% per i neonati che hanno assunto eritromicina per 8-14 giorni e del 10% per i neonati che hanno assunto eritromicina per 15-21 giorni.2 Poiché l’eritromicina può essere usata nel trattamento di condizioni nei neonati che sono associate a mortalità o morbilità significative (come la pertosse o le infezioni neonatali da Chlamydia trachomatis), il beneficio della terapia con eritromicina deve essere valutato rispetto al potenziale rischio di sviluppare IHPS. I genitori devono essere informati di contattare il loro medico se si verifica vomito o irritabilità con l’alimentazione.
L’uso prolungato o ripetuto di eritromicina può provocare una crescita eccessiva di batteri o funghi non suscettibili. Se si verifica una superinfezione, l’eritromicina deve essere interrotta e deve essere istituita una terapia appropriata.
Quando indicato, incisione e drenaggio o altre procedure chirurgiche devono essere eseguite insieme alla terapia antibiotica.
Informazioni per i pazienti
I pazienti devono essere consigliati che i farmaci antibatterici, compresi E.E.S., devono essere utilizzati solo per trattare le infezioni batteriche. Non trattano le infezioni virali (ad esempio, il comune raffreddore). Quando l’E.E.S. viene prescritto per trattare un’infezione batterica, ai pazienti deve essere detto che anche se è comune sentirsi meglio all’inizio della terapia, il farmaco deve essere preso esattamente come indicato. Saltare le dosi o non completare l’intero corso della terapia può (1) diminuire l’efficacia del trattamento immediato e (2) aumentare la probabilità che i batteri sviluppino resistenza e non siano trattabili da E.E.S. o da altri farmaci antibatterici in futuro.
La diarrea è un problema comune causato dagli antibiotici che di solito finisce quando l’antibiotico viene interrotto. A volte, dopo aver iniziato il trattamento con antibiotici, i pazienti possono sviluppare feci acquose e sanguinolente (con o senza crampi allo stomaco e febbre) anche più tardi, due o più mesi dopo aver preso l’ultima dose di antibiotico. Se questo si verifica, i pazienti devono contattare il loro medico il più presto possibile.
Interazioni farmacologiche
Teofillina
L’uso di eritromicina in pazienti che stanno ricevendo alte dosi di teofillina può essere associato ad un aumento dei livelli sierici di teofillina e potenziale tossicità della teofillina. In caso di tossicità della teofillina e/o livelli elevati di teofillina nel siero, la dose di teofillina deve essere ridotta mentre il paziente riceve una terapia concomitante con eritromicina.
Ci sono stati rapporti pubblicati che suggeriscono che quando l’eritromicina orale è data in concomitanza con teofillina c’è una diminuzione delle concentrazioni sieriche di eritromicina di circa 35%. Il meccanismo con cui si verifica questa interazione è sconosciuto. La diminuzione delle concentrazioni di eritromicina dovuta alla co-somministrazione di teofillina potrebbe risultare in concentrazioni subterapeutiche di eritromicina.
Verapamil
Ipotensione, bradiaritmie e acidosi lattica sono state osservate in pazienti che ricevono verapamil in concomitanza, appartenente alla classe di farmaci calcioantagonisti.
Digossina
La somministrazione concomitante di eritromicina e digossina è stata riportata come risultato di elevati livelli sierici di digossina.
Anticoagulanti
Sono stati riportati effetti anticoagulanti aumentati quando eritromicina e anticoagulanti orali sono stati usati contemporaneamente. Gli effetti di anticoagulazione aumentati dovuti alle interazioni di eritromicina con vari anticoagulanti orali possono essere più pronunciati negli anziani.
Eritromicina è un substrato e inibitore della sottofamiglia dell’isoforma 3A del sistema enzimatico del citocromo p450 (CYP3A). La co-somministrazione di eritromicina e di un farmaco principalmente metabolizzato dal CYP3A può essere associata ad aumenti delle concentrazioni del farmaco che potrebbero aumentare o prolungare sia gli effetti terapeutici che quelli avversi del farmaco concomitante. Aggiustamenti del dosaggio possono essere considerati e, quando possibile, le concentrazioni sieriche dei farmaci principalmente metabolizzati dal CYP3A devono essere monitorate attentamente nei pazienti che ricevono eritromicina in concomitanza.
I seguenti sono esempi di alcune interazioni farmacologiche basate sul CYP3A clinicamente significative. Interazioni con altri farmaci metabolizzati dall’isoforma CYP3A sono anche possibili. Le seguenti interazioni farmacologiche basate sul CYP3A sono state osservate con prodotti a base di eritromicina nell’esperienza post-marketing:
Ergotamina/diidroergotamina
I rapporti post-marketing indicano che la co-somministrazione di eritromicina con ergotamina o diidroergotamina è stata associata a tossicità acuta da ergot caratterizzata da vasospasmo e ischemia delle estremità e altri tessuti incluso il sistema nervoso centrale. La somministrazione concomitante di eritromicina con ergotamina o diidroergotamina è controindicata (vedi CONTRAINDICAZIONI).
Triazolobenzodiazepine (come triazolam e alprazolam) e relative benzodiazepine
Eritromicina è stata riportata per diminuire la clearance di triazolam e midazolam, e quindi, può aumentare l’effetto farmacologico di queste benzodiazepine.
Inibitori della HMG-CoA Reduttasi
Eritromicina è stata segnalata per aumentare le concentrazioni degli inibitori della HMG-CoA Reduttasi (es, lovastatina e simvastatina). Rari rapporti di rabdomiolisi sono stati riportati in pazienti che assumono questi farmaci in concomitanza.
Sildenafil (Viagra)
Eritromicina è stato segnalato per aumentare l’esposizione sistemica (AUC) di sildenafil. Deve essere presa in considerazione la riduzione del dosaggio di sildenafil. (Vedi foglietto illustrativo del Viagra.)
Ci sono state segnalazioni spontanee o pubblicate di interazioni basate sul CYP3A di eritromicina con ciclosporina, carbamazepina, tacrolimus, alfentanil, disopiramide, rifabutina, chinidina, metilprednisolone, cilostazolo, vinblastina e bromocriptina.
Somministrazione concomitante di eritromicina con cisapride, pimozide, astemizole o terfenadine è controindicata (vedi CONTRAINDICAZIONI).
Inoltre, ci sono state segnalazioni di interazioni di eritromicina con farmaci che non si pensa siano metabolizzati dal CYP3A, inclusi esobarbital, fenitoina e valproato.
Eritromicina è stata riportata per alterare significativamente il metabolismo degli antistaminici non sedativi terfenadina e astemizolo quando presi in concomitanza. Sono stati osservati rari casi di gravi eventi avversi cardiovascolari, incluso prolungamento dell’intervallo QT/QTc elettrocardiografico, arresto cardiaco, torsades de pointes e altre aritmie ventricolari (vedi CONTRAINDICAZIONI). Inoltre, i decessi sono stati riportati raramente con la somministrazione concomitante di terfenadina ed eritromicina.
Ci sono stati rapporti post-marketing di interazioni farmacologiche quando l’eritromicina è co-somministrata con cisapride, con conseguente prolungamento del QT, aritmie cardiache, tachicardia ventricolare, fibrillazione ventricolare e torsades de pointes, molto probabilmente a causa dell’inibizione del metabolismo epatico di cisapride da parte di eritromicina. Sono stati riportati casi mortali (vedi CONTRAINDICAZIONI).
Colchicina
La colchicina è un substrato sia per il CYP3A4 che per il trasportatore di efflusso P-glicoproteina (P-gp). L’eritromicina è considerata un moderato inibitore del CYP3A4. Si prevede un aumento significativo della concentrazione plasmatica della colchicina quando viene co-somministrata con moderati inibitori del CYP3A4 come l’eritromicina. Se la co-somministrazione di colchicina ed eritromicina è necessaria, la dose iniziale di colchicina può essere necessario ridurre, e la dose massima di colchicina deve essere abbassata. I pazienti devono essere monitorati per i sintomi clinici della tossicità della colchicina (vedi AVVERTENZE).
Interazioni farmaco/test di laboratorio
Eritromicina interferisce con la determinazione fluorometrica delle catecolamine urinarie.
Carcinogenesi, mutagenesi, compromissione della fertilità
Studi dietetici orali a lungo termine condotti con eritromicina stearato nei ratti fino a 400 mg/kg/giorno e nei topi fino a circa 500 mg/kg/giorno (circa 1 o 2 volte la dose umana massima sulla base della superficie del corpo) non hanno fornito prove di tumorigenicità. L’eritromicina stearato non ha mostrato un potenziale genotossico nei test di Ames e del linfoma del topo né ha indotto aberrazioni cromosomiche nelle cellule CHO. Non c’è stato alcun effetto apparente sulla fertilità maschile o femminile nei ratti trattati con eritromicina base per via orale a 700 mg/kg/giorno (circa 3 volte la dose massima umana su una base di superficie corporea).
Gravidanza
Effetti teratogeni
Non ci sono prove di teratogenicità o qualsiasi altro effetto avverso sulla riproduzione in ratti femmina nutriti con eritromicina base per via orale a 350 mg/kg/giorno (circa due volte la dose massima raccomandata per l’uomo su una base di superficie corporea) prima e durante l’accoppiamento, durante la gestazione e fino allo svezzamento.
Nessuna prova di teratogenicità o embriotossicità è stata osservata quando l’eritromicina base è stata somministrata per via orale a ratti e topi gravidi a 700 mg/kg/giorno e a conigli gravidi a 125 mg/kg/giorno (circa 1 a 3 volte la dose massima raccomandata per l’uomo).
Lavoro e parto
L’effetto dell’eritromicina sul lavoro e sul parto è sconosciuto.
Madri che allattano
Eritromicina viene escreta nel latte umano. Cautela deve essere esercitata quando l’eritromicina viene somministrata ad una donna che allatta.
Uso pediatrico
Vedere le sezioni INDICAZIONI E USO e DOSAGGIO E AMMINISTRAZIONE.
Uso geriatrico
Pazienti anziani, particolarmente quelli con funzione renale o epatica ridotta, possono essere a rischio aumentato di sviluppare perdita dell’udito indotta da eritromicina (vedi REAZIONI AVVERSE e DOSAGGIO E AMMINISTRAZIONE).
I pazienti anziani possono essere più suscettibili allo sviluppo di aritmie torsades de pointes rispetto ai pazienti più giovani (vedi AVVERTENZE).
I pazienti anziani possono sperimentare effetti aumentati della terapia anticoagulante orale durante il trattamento con eritromicina (vedi PRECAUZIONI – Interazioni farmacologiche).
E.E.S.® Granules contiene 25,9 mg (1,1 mEq) di sodio per dose individuale.
La popolazione geriatrica può rispondere con una natriuresi attenuata al carico di sale. Questo può essere clinicamente importante per quanto riguarda le malattie come l’insufficienza cardiaca congestizia.
E.E.S. 400 rivestito con pellicola contiene 47 mg (2 mEq) di sodio per compressa e 10,0 mg (0,3 mEq) di potassio per compressa.
Reazioni avverse
Gli effetti collaterali più frequenti delle preparazioni orali di eritromicina sono gastrointestinali e sono legati alla dose. Essi includono nausea, vomito, dolore addominale, diarrea e anoressia. Sintomi di epatite, disfunzione epatica e/o risultati anormali dei test di funzionalità epatica possono verificarsi (vedi sezione AVVERTENZE).
La comparsa di sintomi di colite pseudomembranosa può verificarsi durante o dopo il trattamento antibatterico (vedi sezione AVVERTENZE).
Eritromicina è stata associata con prolungamento del QT e aritmie ventricolari, incluso tachicardia ventricolare e torsades de pointes (vedi AVVERTENZE).
Si sono verificate reazioni allergiche che vanno da orticaria ad anafilassi. Reazioni cutanee che vanno da lievi eruzioni a eritema multiforme, sindrome di Stevens-Johnson e necrolisi epidermica tossica sono state riportate raramente.
Ci sono state segnalazioni di nefrite interstiziale in coincidenza con l’uso di eritromicina.
Ci sono state rare segnalazioni di pancreatite e convulsioni.
Ci sono stati rapporti isolati di perdita reversibile dell’udito che si verificano principalmente in pazienti con insufficienza renale e in pazienti che ricevono alte dosi di eritromicina.
Sovradosaggio
In caso di sovradosaggio, eritromicina deve essere interrotta. Il sovradosaggio deve essere gestito con l’eliminazione rapida del farmaco non assorbito e tutte le altre misure appropriate devono essere istituite.
Eritromicina non viene rimosso dalla dialisi peritoneale o emodialisi.
Dosaggio e amministrazione
Eritromicina etilsuccinato sospensioni e compresse rivestite con film può essere somministrato senza considerare i pasti.
Bambini
Età, peso e gravità dell’infezione sono fattori importanti nel determinare il dosaggio adeguato. Nelle infezioni da lievi a moderate, il dosaggio usuale di eritromicina etilsuccinato per i bambini è da 30 a 50 mg/kg/giorno in dosi equamente divise ogni 6 ore. Per le infezioni più gravi, questo dosaggio può essere raddoppiato. Se si desidera un dosaggio due volte al giorno, la metà della dose totale giornaliera può essere somministrata ogni 12 ore. Le dosi possono anche essere date tre volte al giorno somministrando un terzo della dose totale giornaliera ogni 8 ore.
Il seguente schema di dosaggio è suggerito per le infezioni da lievi a moderate:
| Peso corporeo | Dose giornaliera totale |
|---|---|
| Sotto 10 libbre | da 30 a 50 mg/kg/giorno 15 a 25 mg/lb/giorno |
| 10 a 15 lbs | 200 mg |
| 16 a 25 lbs | 400 mg |
| 26 a 50 lbs | 800 mg |
| 51 a 100 lbs | 1200 mg |
| oltre 100 lbs | 1600 mg |
Adulti
400 mg di eritromicina etilsuccinato ogni 6 ore è la dose usuale. Il dosaggio può essere aumentato fino a 4 g al giorno secondo la gravità dell’infezione. Se si desidera un dosaggio due volte al giorno, la metà della dose totale giornaliera può essere somministrata ogni 12 ore. Le dosi possono anche essere date tre volte al giorno somministrando un terzo della dose giornaliera totale ogni 8 ore.
Per il calcolo del dosaggio per gli adulti, usare un rapporto di 400 mg di attività di eritromicina come etilsuccinato a 250 mg di attività di eritromicina come stearato, base o estolato.
Nel trattamento delle infezioni streptococciche, un dosaggio terapeutico di eritromicina etilsuccinato dovrebbe essere somministrato per almeno 10 giorni. Nella profilassi continua contro le recidive delle infezioni streptococciche in persone con una storia di malattia reumatica del cuore, il dosaggio usuale è 400 mg due volte al giorno.
Per il trattamento dell’uretrite dovuta a C. trachomatis o U. urealyticum
800 mg tre volte al giorno per 7 giorni.
Per il trattamento della sifilide primaria
Adulti
48 a 64 g dati in dosi divise in un periodo di 10 a 15 giorni.
Per Amebiasis intestinale
Adulti
400 mg quattro volte al giorno per 10 a 14 giorni.
Bambini
30 a 50 mg/kg/giorno in dosi divise per 10 a 14 giorni.
Per uso nella pertosse
Anche se il dosaggio ottimale e la durata non sono stati stabiliti, le dosi di eritromicina utilizzate negli studi clinici riportati erano 40-50 mg/kg/giorno, dati in dosi divise per 5 a 14 giorni.
Per il trattamento della malattia dei legionari
Anche se le dosi ottimali non sono state stabilite, le dosi utilizzate nei dati clinici riportati erano quelle raccomandate sopra (da 1,6 a 4 g al giorno in dosi divise).
Direzioni per la miscelazione dei granuli E.E.S.
100 mL
Aggiungere 77 mL di acqua e agitare vigorosamente. Questo fa 100 mL di sospensione.
200 mL
Aggiungi 154 mL di acqua e agita vigorosamente. Questo fa 200 mL di sospensione.
Come viene fornito EES
E.E.S. Granuli 200 mg per 5 mL (eritromicina etilsuccinato per sospensione orale, USP) sono granuli rosa con un aroma di ciliegia e sono forniti in bottiglie da 100 mL (NDC 24338-134-02) e 200 mL (NDC 24338-136-10). Dopo la ricostituzione i granuli E.E.S. diventano una sospensione rosa opaca con un aroma di ciliegia.
E.E.S. 400 compresse rivestite con film (compresse di eritromicina etilsuccinato, USP) 400 mg, sono fornite come compresse ovali rosa con l’indicazione di due lettere, EE, in:
Flaconi da 30 (NDC 24338-100-03) Flaconi da 100 (NDC 24338-100-13)
conservazione consigliata
conservare a 20° a 25°C (68° a 77°F).
Conservare i granuli, prima della miscelazione, a 20° a 25°C (68° a 77°F). Dopo la miscelazione, refrigerare e utilizzare entro 10 giorni.
- Commissione sulla febbre reumatica, endocardite e malattia di Kawasaki del Consiglio sulle malattie cardiovascolari nei giovani, l’American Heart Association: Prevenzione della febbre reumatica. Circolazione. 78(4):1082-1086, ottobre 1988.
- Honein, M.A., et al: Infantile stenosi ipertrofica pilorica dopo la profilassi della pertosse con eritromicina: una revisione dei casi e studio di coorte. The Lancet 1999:354 (9196): 2101-5.
Revised: Aprile 2018
EES-PI-03
Arbor Pharmaceuticals, LLC
Atlanta, GA 30328
(Nos. 5729, 6369)
PANNELLO DI VISUALIZZAZIONE PRINCIPALE – Etichetta della bottiglia della compressa da 400 mg
NDC 24338-100-03
30 compresse
E.E.S. 400®
compresse rivestite con film
ETROMICINA
ETILSUCCINATO
Compresse, USP
400 mg
Eritromicina
attività
Rx solo
arbor
PHARMACEUTICALS, LLC

Pannello espositivo principale – Etichetta del flacone da 100 mL
NDC 24338-134-02
100 mL (quando miscelato)
per sospensione orale
E.E.S.® Granuli
ERITROMICINA
ETILSUCCINATO PER
SUSPENSIONE ORALE, USP
Eritromicina attività
200 mg per 5 mL
ricostituito
Solo Rx
arbor®
PHARMACEUTICALS, INC.

Pannello di visualizzazione principale – Etichetta del flacone da 5 mL
NDC 24338-136-10
200 mL (quando mescolato)
per sospensione orale
E.E.S.® Granulato
ERITROMICINA
ETILSUCCINATO PER
SUSPENSIONE ORALE, USP
Attività dell’eritromicina
200 mg per 5 mL
quando ricostituito
Solo Rx
arbor®
PHARMACEUTICALS, INC.

| E.E.S 400 eritromicina etilsuccinato compressa |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
| E.E.S erythromycin ethylsuccinate granule, for suspension |
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
| E.E.S erythromycin ethylsuccinate granule, for suspension |
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
|
||||||||||||||||
Labeler – Arbor Pharmaceuticals, Inc. (781796417)
Frequently asked questions
- Can you take antibiotics while pregnant?
More about E.E.S. Granuli (eritromicina)
- Effetti collaterali
- Durante la gravidanza o l’allattamento
- Informazioni sul dosaggio
- Interazioni farmacologiche
- Prezzi & Buoni sconto
- En Español
- Classe del farmaco: macrolidi
Risorse per i consumatori
- Lettura avanzata
Risorse professionali
- Informazioni sulla prescrizione
- Eritromicina compresse (FDA)
Altre marche Ery-Tab, EryPed, Erythrocin, Eryc, PCE Dispertab
Guide correlate al trattamento
- Prevenzione dell’endocardite batterica
- Bartonellosi
- Preparazione intestinale
- Bronchite
- … +21 più
Disconoscimento medico