Die Bestimmung von organischen Spurenstoffen in der Lebensmittelanalytik ist von großer Bedeutung für die Lebensmittelqualität und Lebensmittelsicherheit. Sowohl die Abtrennung des Analyten von möglichen Störfaktoren in der Lebensmittelmatrix als auch die qualitative und quantitative Bestimmung der Zielverbindung sind wesentliche Schritte in der analytischen Lebensmittelchemie.
Definition
Die Flüssigchromatographie (LC, hier High Performance LC – HPLC) ist eine physikalische Trenntechnik für die Spurenanalyse. Sie beruht auf der Wechselwirkung eines Analyten mit einer stationären Phase (Säule mit Partikeln) und einer mobilen Phase (flüssiger Eluent oder ein Gemisch von Eluenten). Die Massenspektrometrie (MS) ist das analytische Werkzeug zur Messung der Zusammensetzung einer Probe. Die MS liefert nützliche Informationen über das Molekulargewicht und die Struktur von Analyten und hilft bei der Aufklärung unbekannter Verbindungen.
Die Kombination LC/MS, LC-MS ist aufgrund ihrer sehr hohen Empfindlichkeit (bis in den ppt-Bereich) und Spezifität eine leistungsstarke Technik. Im Bereich der organischen Spurenanalytik wird die MS für viele Anwendungen eingesetzt, aber im Gegensatz zur GC/MS (Gaschromatographie, gekoppelt mit Massenspektrometrie) ist sie für die Analyse von Proben bestimmt, die nichtflüchtige analytische Ziele enthalten, typischerweise mit einer Masse zwischen 200 – 800u, die thermisch labil sind, eine hohe Polarität aufweisen oder eine hohe Molekülmasse haben.
Webinar: Strategie zur Vorbeugung von Lebensmittelbetrug – eine globale Perspektive auf Prüfung, Überwachung und Verifizierung
Dieses Webinar erörtert die Rolle, die die Prüfung der Lebensmittelechtheit in einer Strategie zur Vorbeugung von Lebensmittelbetrug spielen kann. Außerdem wird die Notwendigkeit einer ganzheitlichen Sichtweise hervorgehoben, die die Identifizierung von Risiken, die Umsetzung eines Plans zur Vorbeugung von Lebensmittelbetrug, das Management der Lieferkette, die Unternehmenskultur für Lebensmittelsicherheit und die Labortests umfasst.
JETZT ANMELDEN
Arbeitsprinzip
Im Prinzip muss ein LC/MS-Gerät die vier Arbeitsschritte ausführen, darunter:
- Chromatographische Trennung der Analyten durch eine Trennsäule
- Ionisierung des Analyten
- Isolierung der Ionen und
- Identifizierung der Ionen
Im Allgemeinen ist es nicht trivial, ein HPLC-System mit einem Massenspektrometer zu koppeln, da die Schwierigkeit darin besteht, einen gelösten Stoff in ein Gasphasen-Ion zu verwandeln. Die Herausforderung besteht darin, das Lösungsmittel loszuwerden und gleichzeitig ein angemessenes Vakuum im Massenspektrometer aufrechtzuerhalten und die Gasphasen-Ionen zu erzeugen. Daher werden die von der Chromatographiesäule eluierten Komponenten über eine spezielle Schnittstelle in das Massenspektrometer eingeführt.
Die beiden am häufigsten verwendeten Ionisierungsschnittstellensysteme, die chemische Ionisierung bei Atmosphärendruck (APCI) und die Elektrospray-Ionisierung (ESI), werden in Abhängigkeit von den physikalisch-chemischen Eigenschaften der Analyten (d. h. Polarität und Säuregehalt) ausgewählt. Die Ionisierung findet bei Atmosphärendruck statt, und beide gelten als weiche Ionisierungsmethoden, d. h. das Massenspektrum liefert hauptsächlich Informationen über das Molekulargewicht, es sei denn, es werden Fragmentierungstechniken verwendet.
Da Verbindungen teilweise aus dem chromatographischen System miteluieren, ist eine eindeutige Zuordnung der einzelnen Fragmente mit der reinen LC-MS, bei der nur Molekülionenmassen verfügbar sind, nicht möglich. Um dieses Problem zu überwinden, wird heutzutage hauptsächlich die Tandem-Massenspektrometrie (MS/MS) eingesetzt, die mehrere Schritte der Massenselektion oder -analyse umfasst (LC/MS/MS oder LC/MSn). Diese Systeme sind in der Lage, Rückstände im unteren ppt-Bereich zu bestimmen. Für die Qualifizierung organischer Moleküle ist ein anderer technischer MS-Aufbau erforderlich. Ein möglicher Ansatz für die Qualifizierung ist die Verwendung eines MS, das Ionen erzeugt, sie in eine lineare Ionenfalle leitet und sie dann in einem Hochfrequenzfeld speichert. Danach ermöglichen verschiedene technische Möglichkeiten die Qualifizierung der Ionen und damit der unbekannten Verbindung.
Anwendungen
Seit ihrer Einführung in die Routineanalytik vor etwa zehn Jahren hat sich die LC/MS in den meisten Bereichen der analytischen Chemie etabliert, z.B. in der Qualitätskontrolle, der Grundlagen- und angewandten Forschung und der behördlichen Kontrolle.
Die folgenden Beispiele geben einen kurzen Überblick:
a) Pharmazie
- Pharmakokinetische Untersuchungen von Arzneimitteln, z.B. Abbauprozesse von Medikamenten
- Arzneimittelentwicklung, z.B. Metabolit-Identifizierung oder Identifizierung von Verunreinigungen
b) Molekularbiologie
- Proteomics, z. B. groß angelegte Untersuchung von Proteinen, insbesondere deren Strukturen und Funktionen
- Metabolomics, z.z. B. Bestimmung von Stoffwechselintermediaten, Hormonen und anderen Signalmolekülen
c) Umwelt
- Abwasser, z. B. endokrine Verbindungen
- Boden, z.B. metallorganische Verbindungen
d) Lebensmittel
- Inhaltsstoffe, z.B. Aminosäuren, Lipide
- Kontaminanten, z.B. Multirückstandsanalyse von Pestiziden, Toxinen in Meeresfrüchten, Tierarzneimittelrückständen, Bestimmung von Farbstoffen, Acrylamid, Analyse von Microcystinen
- Naturstoffe, z. B. Terpene, Steroide
Perfluorierte Tenside (PFC) als Beispiel in der Lebensmittelanalytik
Hintergrund
PFC ist ein hervorragendes Beispiel für die Kombination komplexer Probenvorbereitung mit hochentwickelten LC/MS-Geräten und fundierten Kenntnissen der analytischen Chemie. Die einzigartigen Eigenschaften von PFT machen sie für eine Reihe industrieller und kommerzieller Produkte, wie Kühlflüssigkeiten, Polymere und als Bestandteile von Arzneimitteln und Pestiziden, nützlich. Insbesondere perfluorierte Carboxylate (z. B. PFOA – Perfluoroctansäure) und perfluorierte Sulfonate (z. B. PFOS – Perfluoroctansulfonsäure) werden als Tenside verwendet, z. B. zur Imprägnierung von Textilien und Teppichen, in Feuerlöschschäumen und für fettabweisende Behandlungen in der Papierindustrie. PFC werden seit über 50 Jahren hergestellt und inzwischen weltweit vertrieben. Wenn C-H-Bindungen nicht vollständig durch C-F-Bindungen, eine der stärksten bekannten chemischen Bindungen, ersetzt werden, ist ein Abbau immer noch möglich.
Nur PFOA und PFOS sind toxikologisch bewertet (chronisch toxisch und krebserregend), alle anderen homologen Verbindungen, Isomere usw. sind noch nicht bewertet. Physikalisch gesehen sind PFC sowohl persistent (d. h. nicht abbaubar) als auch mobil (d. h. sie können aus kontaminierten Böden ins Grundwasser sickern). Dies stellt eine ständige Bedrohung im Zusammenhang mit der Entnahme und/oder Aufbereitung von Trinkwasser dar. Darüber hinaus gelangen diese Verbindungen durch Pflanzen in die Nahrungskette.
Die Entdeckung hoher PFC-Kontaminationen in zwei deutschen Flüssen im Jahr 2006 lenkte das öffentliche Interesse auf diese Verbindungen.
Die Verschmutzung im Jahr 2006 könnte von organischem Klärschlamm stammen, der als Düngemittel für landwirtschaftliche Zwecke ausgebracht wurde. Es wurde nachgewiesen, dass der Boden bis zu 600 µg PFC/kg enthält, was zu einer Verunreinigung des Trinkwassers und der Versorgungsanlagen führte. Bislang haben sieben Bundesländer PFC-Belastungen gemeldet.
Fraunhofer IME
Eine der Kernkompetenzen des Fraunhofer-Instituts für Molekularbiologie und Angewandte Oekologie ist die Entwicklung praktikabler und zuverlässiger Methoden zur Identifizierung und Analyse chemischer Kontaminanten in Lebensmitteln und Umweltmatrices.
Seit 1999 führt das Fraunhofer IME Projekte zur Messung der PFC-Belastung in verschiedenen Umweltmatrices durch. Diese Arbeiten wurden im Auftrag von Industriepartnern durchgeführt und konzentrierten sich insbesondere auf PFC-Carboxylate und PFC-Sulfonate. Weitere Untersuchungen wurden im Auftrag des Monitoring-Programms der Umweltprobenbank des Bundes durchgeführt, die auch menschliche Blutproben einschlossen. Im Jahr 2005 wurden die ersten Untersuchungen im Bereich der Lebensmittel durchgeführt und 2006 wurden die Ergebnisse ausgewählter Lebensmittelproben (z.B. Muttermilch, Pommes frites) auch in den Medien diskutiert. Größere Projekte mit den Schwerpunkten Pflanzentransfer, Kartoffel und Produkte, Humanmatrices (Blut und Muttermilch) sowie Umweltproben (z.B. Abwasser, Schlamm und Boden) wurden 2007 durchgeführt.
Analytische Lösung
Drei verschiedene Probenvorbereitungen wurden angewandt, um alle möglichen Probenmatrices abzudecken:
- IPE (Ionenpaar-Extraktion). Verwendung des Ionenpaars Tetra-n-butylammoniumhydrogensulfat, gefolgt von einer Flüssig-Fest-Extraktion (z.B. Umweltproben)
- AAE (saure alkalische Extraktion). Entfernung der Lipide mit Hexan bei pH 14 (flüssige Ammoniaklösung), Einstellung auf pH 1 mit Salzsäure und Extraktion mit tert-Butylmethylether (z. B. Muttermilch)
- SPE (Festphasenextraktion, derzeit meist zitierte Methode) mit Kartuschen unterschiedlicher Polarität je nach Ionencharakter der PFC in einem gepufferten Medium (z.z. B. Kartoffel)
Die Verwendung interner Standards zur Kalibrierung wird dringend empfohlen; derzeit umfassen unsere Methoden neun massenmarkierte PFC-Standards. Bevor die Proben in die LC/MS eingeführt werden, muss das Gerät selbst auf teflonbeschichtete Ersatzteile überprüft werden, da diese emittierende PFC enthalten, die die Ergebnisse in nicht reproduzierbarer Weise beeinflussen. Diese Teile müssen ausgetauscht werden, was eine bessere Kenntnis der LC/MS-Komponenten erfordert.
Analysebeispiel
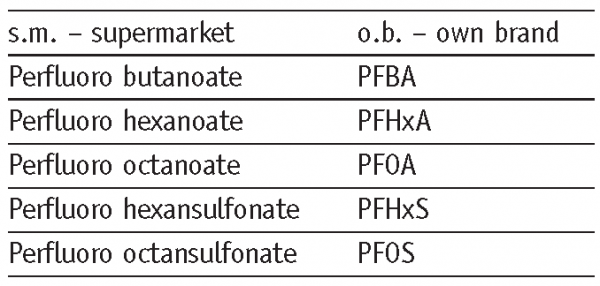
Für die Analyse von rohen Kartoffeln und Kartoffelprodukten haben wir unsere LC/MS/MS (HPLC Alliance 2695 mit Quattro Ultima Pt im Electrospray Negative Mode, beide Waters; 150 x 2 mm Luna 3 µm C18(2) Säule, Phenomenex) System für die Zielmassen von 9 Perfluorcarbonsäuren (C4 – C12) und 3 Perfluorsulfonsäuren (C4, C6, C8) unter Verwendung von 13C-markierten Referenzmaterialien (LOQ 0.5 µg/Kg) nach einer SPE-Probenvorbereitung.
PFCs zeigten eine unterschiedliche Verteilung in rohen Kartoffeln und in Kartoffelprodukten (Tabelle 1), was die Annahme einer Kontamination während der Verarbeitung sowie einer Bodenkontamination zulässt. Dies kann durch unsere PFC-Pommes-Untersuchungen aus dem Jahr 2006 gestützt werden, bei denen wir Pommes frites aus Fast-Food-Restaurants analysierten und bis zu 2,8 µg PFOA/kg und bis zu 0,9 µg PFOS/kg fanden.
Analytischer Ausblick
Das Fraunhofer IME verfügt über eine erhebliche Expertise und Erfahrung in der PFC-Analytik, die auf viele noch nicht untersuchte Bereiche der PFC-Kontamination von Umwelt und Lebensmitteln angewendet werden könnte. Viele kurz- und langkettige PFC sind bereits in unserem Untersuchungsprogramm enthalten, aber unsere analytischen Fähigkeiten könnten durch die Einbeziehung weiterer PFC verbessert werden. Die zusätzlichen PFC müssen mittels LC/MS identifiziert werden, da keine kommerziellen Standards verfügbar sind. Dies wird zu konsolidierten Erkenntnissen über die Vorläuferstoffe, die Wege der Lebensmittelkontamination und den Abbau während der Verarbeitung von Lebensmitteln führen.