Introduction
Potrivit Organizației Mondiale a Sănătății, depresia afectează aproximativ 350 milioane de oameni din întreaga lume (Organization, 2017). Pacienții cu depresie indică simptome de tulburări de anxietate și sunt însoțite de incapacitatea de a experimenta plăcerea și interesul, pierderea concentrării, îndoială de sine, anxietate socială, tulburări de somn și de apetit (Namola et al., 2015). Principalii factori care cauzează depresia sunt dezechilibrele chimice sau hormonale din creier. Principalul hormon asociat cu depresia este serotonina. Alți hormoni sunt norepinefrina și dopamina (Yi et al., 2008). Acești hormoni sunt necesari pentru funcționarea normală a creierului și pentru a controla sentimentele. Distrugerea acestor hormoni poate provoca un dezechilibru chimic în creier care duce la depresie.
Depresia poate fi tratată, în funcție de gravitatea ei, prin psihoterapie sau medicamente. Antidepresivele sunt principalele tipuri de medicamente utilizate pentru tratarea depresiei. Există multe tipuri diferite de medicamente antidepresive disponibile, iar acestea diferă doar prin modul în care acționează asupra creierului, prin costul lor și prin profilul efectelor secundare. În prima linie de tratament, celor mai mulți pacienți li se prescrie fie un antidepresiv triciclic (TCA), fie un inhibitor selectiv al recaptării serotoninei (SSRI; McCarthy et al., 2016). Medicamentele care sunt utilizate în mod obișnuit pentru tratamentele anxietății sunt benzodiazepinele. Deși pe piață există multe medicamente antidepresive utilizate pentru tratarea depresiei, efectele secundare ale utilizării acestor medicamente sunt de mare îngrijorare (Binfaré et al., 2009). O terapie alternativă a depresiei este utilizarea medicamentelor pe bază de plante (Fajemiroye et al., 2016). Utilizarea extractelor pe bază de plante este din ce în ce mai bine acceptată de către profesia medicală și de către pacienți. Majoritatea remediilor pe bază de plante utilizate pentru tratamentul depresiei sunt extracte brute sau semipurificate (Calixto et al., 2000; Carlini, 2003; Guan și Liu, 2016).
Există o raritate în rapoartele privind cercetările care implică principiul activ capabil să inducă activitate asupra sistemului nervos central (SNC). O trecere în revistă realizată de Carlini (2003) include informații doar despre efectele psihanaleptice, psiholeptice și psihodisleptice. O recenzie recentă realizată de Guan și Liu (2016) a discutat relația structură-activitate a efectelor antidepresive ale flavonoidelor izolate din surse naturale și sintetice. Alcaloizii indolici sintetici, activitatea lor și utilizarea potențială în medicină au fost deja analizate în mai multe articole (de Sa et al., 2009). Cu toate acestea, nu a fost publicat niciun articol de analiză care să coreleze alcaloizii indolici din plante izolați cu activitatea antidepresivă. Această recenzie oferă informații cu privire la potențialul alcaloizilor indolici naturali pentru tratamentul tulburărilor neurologice, studii privind relația structură-activitate și măsurarea acestora cu alți metaboliți bioactivi ca potențiale piste de medicamente antidepresive din perspectiva structurii chimice. Acesta este compilat prin investigarea bibliografică a revistelor științifice și a literaturii relevante identificate prin intermediul bazelor de date electronice Web of Science.
Plante antidepresive
Acest articol de sinteză tratează plantele care posedă activitate asupra SNC. Deși multe tipuri de plante se încadrează în această categorie, vom evidenția doar plantele care prezintă proprietăți antidepresive. Două plante care conțin alcaloizi indolici sunt Passiflora incarnata L. (floarea pasiunii) și Mitragyna speciosa (Korth.) Havil (kratom), în timp ce celelalte două plante care nu au evidențiat prezența alcaloizilor indolici sunt Piper methysticum G. Forst (kava) și Valeriana officinalis L., merită o atenție deosebită. Structura chimică a compușilor izolați din aceste plante poate fi folosită ca bază pentru dezvoltarea de noi medicamente.
Passiflora incarnata și alte specii, cum ar fi P. alata Curtis, P. coerulea L. și P. edulis Sims, sunt utilizate pe scară largă ca sedative în medicina tradițională în majoritatea țărilor europene și în America (Houghton și Seth, 2003). Structura medicamentelor benzodiazepine este formată dintr-un inel benzenic fuzionat cu un sistem diazepinic care cuprinde o fracțiune heterociclică cu șapte membri, cu doi atomi de azot în pozițiile 1 și 2 ale inelului. Alcaloizii indolici izolați din P. incarnata, și anume harman, harmol, harmină, harmalol și harmalină, constau dintr-un inel benzenic fuzionat cu un heterociclu cu cinci membri care conține un atom de azot.
Diverse studii au indicat faptul că P. incarnata are un profil farmacologic similar benzodiazepinelor și acționează prin intermediul receptorilor de acid gama-aminobutiric (GABA) (Jawna-Zboiñska et al., 2016). Frunzele de M. speciosa au fost utilizate ca medicament tradițional pentru a trata diareea, diabetul și pentru a îmbunătăți circulația sângelui (Vicknasingam et al., 2010). Mitraginina este principalul alcaloid indolic prezent în M. speciosa, cu analogii săi, specioginina, paynantheina și speciociliatina (León et al., 2009). Două studii efectuate pe extractul apos și pe extractul alcaloidal de M. speciosa au indus un efect antidepresiv în modelele de deznădejde comportamentală la șoareci (Kumarnsit et al., 2007). Un studiu efectuat de Idayu et al. (2011) asupra mitragininei arată efectul antidepresiv în modelul comportamental animal de depresie prin interacțiunea cu axa hipotalamo-hipofizo-suprarenală (HPA) în sistemul neuroendocrin (Idayu et al., 2011).
Piper methysticum G. Forst este consumat sub formă de băutură numită kava care induce o stare mentală plăcută spre o senzație de veselie, reducând în același timp oboseala și anxietatea (Bilia et al., 2002). Studiul arată că cea mai mare parte a activităților farmacologice se păstrează din extractul liposolubil în comparație cu extractul apos. Extractul solubil în lipide conține cel puțin șapte pirone, cunoscute sub numele de kavalactone. Kavalactonele interacționează, în general, cu neurotransmisiile dopaminergice, serotoninice, ale acidului gama aminobutiric (GABA), glutamatergice, previne monoaminooxidază B (MOB) și, de asemenea, oferă o varietate de efecte asupra canalelor ionice (Grunze et al., 2001). Dihidromethysticin este una dintre cele șase kavalactone majore care se găsesc în planta kava. Structura dihidrometisticinei cuprinde o ariletilenă-α-pironă legată de o fracțiune de tip indol care cuprinde doi oxigeni în loc de azot. Aceasta contribuie la activitatea anxiolitică și acționează ca medicament antidepresiv. Studiile dublu-orb controlate cu placebo au demonstrat că kavalactonii au efecte anxiolitice fără a deprima funcțiile mentale și motorii și îmbunătățesc calitatea somnului. Kavalactonii reprezintă o alternativă pentru a înlocui utilizarea benzodiazepinelor în terapia depresiei (Malsch și Kieser, 2001).
Valeriana officinalis L., cunoscută și sub numele de valeriană este utilizată pe scară largă de multe țări ca sedativ, anticonvulsivant, pentru efecte hipnotice și activitate anxiolitică (Ghaderi și Jafari, 2014). Acidul valrenic și valepotriatele au fost raportate ca ingrediente active în preparate farmaceutice, iar extractele brute comerciale de valeriană au înregistrat o utilizare în multe țări (Bos et al., 2002). Valepotriații care cuprind triesteri ai polihidroxiciclopenta-(c)-piranilor cu acizii carboxilici: acetic, valeric, izovaleric, α-isovaleroxi-isovaleric, β-metilvaleric, β-acetoxi-isovaleric, β-hidroxi-isovaleric și β-acetoxi-β-metilvaleric, sunt utilizați ca sedative. Valepotriații sunt instabili, termolabili și se descompun rapid în condiții acide sau alcaline în apă, precum și în soluții alcoolice (Bos et al., 2002). Valepotriatele sunt utile în îmbunătățirea stării animalelor și oamenilor în timpul retragerii benzodiazepinelor (Poyares et al., 2002).
Deși există o varietate de constituenți chimici diferiți, mecanismul de acțiune este raportat ca o interacțiune a valerianei cu sistemul GABA din creier prin inhibarea GABA transaminazei, interacțiunea cu receptorul GABA/benzodiazepină și interferența în absorbția și recrutarea aportului de GABA în sinaptosomi (Sichardt et al., 2007). Diverse modele au fost utilizate pentru a investiga efectele antidepresive ale plantelor. Modelele farmacodinamice includ modelele in vitro, in vivo și clinice au fost utilizate pentru a evalua efectele (tabelul 1). Majoritatea speciilor de plante selectate analizate au fost studiate la nivel in vivo, câteva au fost studiate in vitro și doar kava a fost supusă unor studii clinice. În toate cazurile, trebuie efectuate mai multe cercetări pentru a stabili compușii activi, doza cea mai eficientă și pentru a determina dacă aceasta variază în funcție de diferitele tipuri de depresii.

TABEL 1. Informații din studiile farmacologice ale plantelor recenzate.
Alcaloizi indolici
Alcaloizii indolici au o structură biciclică, formată dintr-un inel benzenic cu șase membri fuzionat cu un inel pirrolic cu cinci membri care conține azot. Acest inel de pirrol cu atom de azot dă naștere la proprietățile de bază ale alcaloizilor indolici care îi fac deosebit de activi din punct de vedere farmacologic (El-Sayed și Verpoorte, 2007). Alcaloizii indolici sunt larg răspândiți în plantele aparținând familiilor Apocynaceae, Loganiaceae, Rubiaceae și Nyssaceae. Printre alcaloizii indolici importanți care au fost izolați din plante se numără medicamentul antihipertensiv, reserpina din Rauvolfia serpentina (Sagi et al., 2016) și puternicele medicamente antitumorale, vinblastina și vincristina din Catharanthus roseus (El-Sayed și Verpoorte, 2007). Studiile privind eficacitatea alcaloizilor indolici în tratarea depresiei nu sunt noi și au fost efectuate încă din 1952, dar în prezent comunitatea științifică a acordat foarte puțină atenție beneficiilor utilității terapeutice a plantelor înzestrate cu proprietăți antidepresive.
Alcaloizii indolici sunt adesea asociați cu funcția receptorilor de proteină G, în special pentru transmiterea semnalelor neuronale prin intermediul receptorilor pentru serotonină (5-HT/hidroxitriptamină). În afară de donatorul de hidrogen prin intermediul N-H liber, prezența densității de electroni π contribuie la energia celui mai înalt orbital molecular ocupat (HOMO) al scheletului plan al indolului. Acest lucru permite interacțiunea cu nucleobaze, în special cu atomul protonat, precum și cu proteinele țintă (de Sa et al., 2009). Structura chimică a neurotransmițătorului serotonină se bazează pe un inel indol aromatic bogat în electroni. Prezența atomului de azot în inelul indol are rolul de a menține sistemul aromatic și face ca legarea N-H să fie mai degrabă acidă decât azotată bazică. Inelul indol este capabil să formeze legături de hidrogen prin intermediul fracțiunii N-H și interacțiuni de suprapunere π-π sau cation-π, prin intermediul fracțiunii aromatice (Shimazaki et al., 2009). Hidrofobicitatea inelelor indolice este aproape aceeași cu cea a subunității fenilice și mai puțin hidrofobă decât cea a inelelor izosterice clasice de benzotiofen și benzofuran. Grupul N-H indol joacă un rol decisiv în interacțiunea cu bioreceptorul țintă, în timp ce derivații sintetizați de benzotiofen și benzofuran prezintă o afinitate moderată sau limitată pentru bioreceptorul țintă (de Sa et al., 2009). Reserpina este unul dintre exemplele de alcaloizi indolici izolați în ultimii 60 de ani care prezintă acțiune sedativă asupra SNC. De altfel, două substanțe chimice, și anume triptamina și serotonina care se găsesc în creier sunt, de asemenea, derivați alcaloizi indolici.
În prezent, constituenții activi din extractele de plante responsabili de efectul antidepresiv sunt încă neclari. Astfel, încercăm să identificăm câteva structuri chimice importante izolate din extracte de plante care prezintă activități antidepresive și să constatăm similitudinea modelului scheletului care ar putea contribui la activitatea antidepresivă. S-au făcut încercări timpurii de identificare a similitudinilor structurale între serotonină și alcaloizii indolici. Cea mai evidentă asemănare constă în inele heterociclice cu șase membri fuzionate cu inele cu cinci membri. Diferența constă în prezența unui atom de azot sau în distribuția electronilor π (figura 1). Printr-un studiu privind relația structură-activitate, Nichols (2012) a raportat că variația în activitatea diferitelor tipuri de molecule sugerează că receptorul este foarte sensibil la natura triptaminei. Alți compuși chimici care sunt izolați cu succes din plante antidepresive sunt menționați în această lucrare de analiză, deoarece sunt poate agoniști specifici cu modele de substituție particulare care sunt capabili să activeze selectiv un subset de efectori. Acest fenomen este acum cunoscut sub numele de selectivitate funcțională.
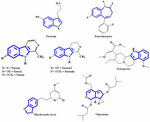
FIGURA 1. Structurile chimice ale serotoninei, benzodiazepinelor și ale compușilor izolați din plante antidepresive. Asemănare în modelul scheletului, care constă din inele heterociclice cu șase membri, atașate cu inele cu cinci membri.
Serotonina, este utilizată pe scară largă în funcționarea creierului și în cogniție ca agonist al receptorilor endogeni (Fink și Göthert, 2007). Serotonina își exercită funcțiile prin intermediul a șapte familii de receptori (5-HT1-5-HT7) care sunt membri ai familiei de receptori cuplați cu proteina G. A fost descrisă o serie de compuși purtând fracțiunea indol care posedă afinitate față de diferiți receptori ai serotoninei (Kochanowska-Karamyan și Hamann, 2010). Similitudinea structurală a alcaloizilor indolici (agoniști exogeni) cu neurotransmițătorii endogeni, cum ar fi serotonina, i-a determinat pe cercetători să prezică potențiala activitate neurologică a acestor molecule. Schema proceselor asociate cu neurotransmisia agoniștilor exogeni este descrisă în figura 2.
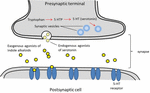
FIGURA 2. Schemă a proceselor asociate cu neurotransmisia. Agoniști exogeni de alcaloizi indolici din plante care împărtășesc similitudini de structură cu serotonina, ceea ce le permite să se lege în receptorii de serotonină (receptorii 5-HT).
Anchiul indolic este cunoscut și sub numele de bioizotere și are caracteristici chimice și fizice similare cu moleculele biologice. Această similitudine este utilizată în dezvoltarea medicamentului prototip care are ca scop îmbunătățirea activității farmacologice și optimizarea profilului farmacocinetic. Într-un alt studiu de evaluare farmacologică a benzofuranilor și a tienopirrolului a condus la molecule bioizosterice care posedă o activitate asemănătoare cu cea a dimetiltriptaminei. Lucrările timpurii cu benzotiofeni și 3-indenalchilamine au demonstrat că, în cazul compușilor lipsiți de substituenți inelari, capacitatea de a acționa ca agoniști în fundul de șobolan a fost aproximativ aceeași cu cea a triptaminei. Rezultatele au arătat că NH-ul indolului nu era esențial pentru a activa receptorul 5-HT2 în fundul de șobolan (Nichols, 2012). O serie de antagoniști ai receptorilor NK1 2-aril-indolici și derivații acestora sunt liganzi buni, dar au o biodisponibilitate orală scăzută la șobolani. Pentru a crește solubilitatea și absorbția, a fost introdus azotul bazic, ceea ce a dus la analogul azaindol și la compușii înrudiți care prezintă aceeași afinitate de legare a NK1 cu seria de antagoniști ai receptorilor NK1 2-aril indolici (Cooper et al., 2001). Docarea moleculară a 2 liganzi derivați din fenil-indol cu receptorii de serotonină 5-HT6 și melanocortina-4 indică faptul că schela privilegiată se poate adapta în funcție de natura subpocketului conservat și a buzunarului de legare neconservat. Interacțiunile părților neconservate ale buzunarului de legare sunt responsabile de diferențe importante în recunoașterea moleculară de către receptorul țintă corespunzător (Bondensgaard et al., 2004).
Potrivit lui de Sa et al. (2009) alcaloizii indolici comuni care se găsesc în surse naturale sunt aminoacizii triptofanici în nutriția umană și descoperirea de hormoni vegetali care au efecte terapeutice, cum ar fi antiinflamatorii, un inhibitor al fosfodiesterazei, agoniști și antagoniști ai receptorilor 5-HT, agoniști ai receptorilor canabinoizi și inhibitori ai HMG-CoA reductazei. Scheletul indolului are buzunare de legare și posedă un domeniu de legare complementar comun cu receptorul țintă, care aparține unei clase de GPCR (receptori membranari cuplați importanți pentru proteinele G). Majoritatea medicamentelor de pe piață conțin substructura indol. Printre acestea se numără indometacinul, ergotamina, frovatriptanul, ondansetronul și tadalafilul.
Concluzie
Această trecere în revistă a constatat că majoritatea remediilor pe bază de plante indicate pentru tratamentul afecțiunilor psihiatrice erau brute sau semipurificate. Rezultatele pentru in vivo și in vitro variază și nu au fost reproductibile, deoarece în diferite regiuni biogeografice conținutul de metaboliți secundari al plantelor se corelează cu disponibilitatea nutrienților, climatul și condițiile ecologice. În plus, la bioactivitatea plantelor poate contribui un singur compus sau un amestec de compuși. Autorii sugerează că efortul de obținere a principiilor active, identificarea substanțelor fitochimice și studiul metabolomic ar trebui să fie efectuat cu inspecții in vitro și in vivo pentru o mai bună caracterizare a medicamentelor pe bază de plante. În cele mai multe cazuri, sinteza alcaloizilor indolici au fost inspirate de moleculele naturale și de similitudinea lor cu serotonina.
Alcaloizii indolici din surse vegetale sunt destul de complecși în comparație cu cei sintetici. Importanța alcaloizilor indolici sintetici este deja stabilită, deoarece structura este disponibilă în diverși liganzi receptori, inhibitori enzimatici și modulatori de bioreceptori. Unii dintre alcaloizii indolici naturali nu pot fi sintetizați prin metodele cunoscute în prezent. În plus, majoritatea informațiilor privind eficacitatea alcaloizilor indolici au fost raportate din alcaloizi indolici sintetici. Prin urmare, potențialul multor alcaloizi indolici naturali ca noi piste medicamentoase pentru diferite tulburări psihiatrice este încă neexploatat. Din punct de vedere istoric, compușii pe bază de plante au fost sursa câtorva dintre cele mai de succes piste medicamentoase sau medicamente utilizate în medicină. Acest lucru indică faptul că ar putea fi descoperite și mai multe.
În concluzie, mai mulți alcaloizi indolici au fost folosiți ca antidepresive sau oferă structuri-pilot pentru dezvoltarea acestora. Pe baza constatărilor noastre, plantele conțin un rezervor de alcaloizi indolici care sunt puncte de plecare valoroase pentru dezvoltarea unor viitoare antidepresive.
Contribuții ale autorilor
HH: Pregătirea manuscrisului. MY: Editarea limbii engleze și sugerarea unor informații importante în vederea îmbunătățirii manuscrisului. AR: Contribuie la înțelegerea schemelor proceselor asociate cu neurotransmisia.
Finanțare
Sprijinul pentru această lucrare a fost oferit de Universiti Malaysia Pahang prin grantul de cercetare UMP RDU170302 către HH.
Declarație privind conflictul de interese
Autorii declară că cercetarea a fost efectuată în absența oricăror relații comerciale sau financiare care ar putea fi interpretate ca un potențial conflict de interese.
Bilia, A. R., Gallori, S., și Vincieri, F. F. (2002). Kava-kava și anxietatea: creșterea cunoștințelor despre eficacitate și siguranță. Life Sci. 70, 2581-2597. doi: 10.1016/S0024-3205(02)01555-2
PubMed Abstract | CrossRef Full Text | Google Scholar
Binfaré, R. W., Rosa, A. O., Rosa, A. O., Lobato, K. R., Santos, A. R., și Rodrigues, A. L. S. (2009). Administrarea de acid ascorbic produce un efect de tip antidepresiv: dovezi pentru implicarea neurotransmisiei monoaminergice. Prog. Neuropsychopharmacol. Biol. Psychiatry 33, 530-540. doi: 10.1016/j.pnpbp.2009.02.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Bondensgaard, K., Ankersen, M., Thøgersen, H., Hansen, B. S., Wulff, B. S., și Bywater, R. P. (2004). Recunoașterea structurilor privilegiate de către receptorii cuplați cu proteina G. J. Med. Chem. 47, 888-899. doi: 10.1021/jm0309452
PubMed Abstract | Full CrossRef Text | Google Scholar
Bos, R., Woerdenbag, H. J., și Pras, N. (2002). Determinarea valepotriatelor. J. Chromatogr. A 967, 131-146. doi: 10.1016/S0021-9673(02)00036-5
CrossRef Full Text | Google Scholar
Calixto, J. B., Beirith, A., Ferreira, J., Santos, A. R., și Yunes, R. A. (2000). Substanțe antinociceptive naturale din plante. Phytother. Res. 14, 401-418. doi: 10.1002/1099-1573(200009)14:6<401::AID-PTR762>3.0.CO;2-H
PubMed Abstract | Publicitate | Textul integral | Google Scholar
Carlini, E. (2003). Plantele și sistemul nervos central. Pharmacol. Biochem. Behav. 75, 501-512. doi: 10.1016/S0091-3057(03)00112-6
CrossRef Full Text | Google Scholar
Cooper, L. C., Chicchi, G. G., Dinnell, K., Elliott, J. M., Hollingworth, G. J., Kurtz, M. M., et al. (2001). Antagoniști ai receptorilor NK 1 de 2-aril-indol: optimizarea substituției indolului. Bioorg. Med. Chem. Lett. 11, 1233-1236. doi: 10.1016/S0960-894X(01)00182-2
CrossRef Full Text | Google Scholar
de Sa, A., Fernando, R., Barreiro, E. J., Fraga, M., și Alberto, C. (2009). De la natură la descoperirea de medicamente: scheletul indolului ca „structură privilegiată”. Mini Rev. Med. Chem. 9, 782-793. doi: 10.2174/138955709788452649
CrossRef Full Text | Google Scholar
El-Sayed, M., și Verpoorte, R. (2007). Catharanthus terpenoid indole alcaloizi: biosinteză și reglementare. Phytochem. Rev. 6, 277-305. doi: 10.1007/s11101-006-9047-8
CrossRef Full Text | Google Scholar
Fajemiroye, J. O., Silva, D. M., Silva, D. M., Oliveira, D. R., și Costa, E. A. (2016). Tratamentul anxietății și depresiei: plante medicinale în retrospectivă. Fundam. Clin. Pharmacol. 30, 198-215. doi: 10.1111/fcp.12186
PubMed Abstract | Full CrossRef Text | Google Scholar
Fiebich, B. L., Knörle, R., Appel, K., Kammler, T. și Weiss, G. (2011). Studii farmacologice într-o combinație de medicamente pe bază de plante de sunătoare (Hypericum perforatum) și floarea pasiunii (Passiflora incarnata): dovezi in vitro și in vivo de sinergie între Hypericum și Passiflora în modelele farmacologice antidepresive. Fitoterapia 82, 474-480. doi: 10.1016/j.fitote.2010.12.006
PubMed Abstract | CrossRef Full Text | Google Scholar
Fink, K. B., și Göthert, M. (2007). Reglarea receptorilor 5-HT de eliberare a neurotransmițătorilor. Pharmacol. Rev. 59, 360-417. doi: 10.1124/pr.59.07103
CrossRef Full Text | Google Scholar
Ghaderi, N., și Jafari, M. (2014). Regenerarea eficientă a plantelor, fidelitatea genetică și acumularea la nivel înalt a doi compuși farmaceutici în plantele regenerate de Valeriana officinalis L. S. Afr. J. Bot. 92, 19-27. doi: 10.1016/j.sajb.2014.01.010
CrossRef Full Text | Google Scholar
Grunze, H., Langosch, J., Schirrmacher, K., Bingmann, D., Von Wegerer, J., și Walden, J. (2001). Pironele Kava exercită efecte asupra transmisiei neuronale și a curenților cationici transmembranari similare cu cele ale stabilizatorilor de dispoziție stabiliți – o analiză. Prog. Neuropsychopharmacol. Biol. Psychiatry 25, 1555-1570.
Google Scholar
Guan, L.-P., și Liu, B.-Y. (2016). Efecte antidepresive asemănătoare cu cele antidepresive și mecanismele de flavonoide și analogi înrudiți. Eur. J. Med. Chem. 121, 47-57. doi: 10.1016/j.ejmech.2016.05.026
PubMed Abstract | CrossRef Full Text | Google Scholar
Hattesohl, M., Feistel, B., Sievers, H., Lehnfeld, R., Hegger, M., și Winterhoff, H. (2008). Extractele de Valeriana officinalis L. sl prezintă efecte anxiolitice și antidepresive, dar nu au proprietăți sedative și nici miorelaxante. Phytomedicine 15, 2-15. doi: 10.1016/j.phymed.2007.11.027
PubMed Abstract | CrossRef Full Text | Google Scholar
Houghton, P. J., and Seth, P. (2003). Plantele și sistemul nervos central. Pharmacol. Biochem. Behav. 75, 497-499. doi: 10.1016/S0091-3057(03)00161-8
CrossRef Full Text | Google Scholar
Idayu, N. F., Hidayat, M. T., Moklas, M., Sharida, F., Raudzah, A. N., Shamima, A., et al. (2011). Efectul de tip antidepresiv al mitragininei izolate din Mitragyna speciosa Korth în modelul de depresie la șoareci. Phytomedicine 18, 402-407. doi: 10.1016/j.phymed.2010.08.011
PubMed Abstract | CrossRef Full Text | Google Scholar
Jawnana-Zboiñska, K., Blecharz-Klin, K., Joniec-Maciejak, I., Wawer, A., Pyrzanowska, J., Piechal, A., et al. (2016). Passiflora incarnata L. Îmbunătățește memoria spațială, reduce stresul și afectează neurotransmisia la șobolani. Phytother. Res. 30, 781-789. doi: 10.1002/ptr.5578
PubMed Abstract | Text integral | Google Scholar
Kochanowska-Karamyan, A. J., și Hamann, M. T. (2010). Marine indole alkaloids: potential new drug leads for the control of depression and anxiety. Chem. Rev. 110, 4489-4497. doi: 10.1021/cr900211p
PubMed Abstract | Full Text | Google Scholar
Kumarnsit, E., Vongvatcharanon, U., Keawpradub, N., și Intasaro, P. (2007). Imunoreactivitatea Fos-like în nucleele raphe dorsale de șobolan indusă de extractul alcaloid de Mitragyna speciosa. Neurosci. Lett. 416, 128-132. doi: 10.1016/j.neulet.2007.01.061
PubMed Abstract | Refef Full Text | Google Scholar
León, F., Habib, E., Adkins, J. E., Furr, E. B., McCurdy, C. R., și Cutler, S. J. (2009). Phytochemical characterization of the leaves of Mitragyna speciosa grown in USA. Nat. Prod. Commun. 4, 907-910.
PubMed Abstract | Google Scholar
Malsch, U., și Kieser, M. (2001). Eficacitatea kava-kava în tratamentul anxietății non-psihotice, în urma pretratamentului cu benzodiazepine. Psychopharmacology 157, 277-283. doi: 10.1007/s002130100792
PubMed Abstract | CrossRef Full Text
McCarthy, A., Wafford, K., Shanks, E., Ligocki, M., Edgar, D. M., și Dijk, D.-J. (2016). Homeostazia somnului REM în absența somnului REM: Efectele antidepresivelor. Neuropharmacology 108, 415-425. doi: 10.1016/j.neuropharm.2016.04.047
PubMed Abstract | CrossRef Full Text | Google Scholar
Namola, V., Ratan, P., și Kothiyal, P. (2015). Depresia și rolul biomaterialelor marine: o revizuire. Eur. J. Biomed. Pharm. Sci. 2, 137-148.
Nichols, D. E. (2012). Relațiile structură-activitate ale agoniștilor serotoninei 5-HT 2A. WIREs Membr. Transp. Signaling 1, 559-579. doi: 10.1002/wmts.42
CrossRef Full Text | Google Scholar
Organizare, W. H. (2017). Depression Fact Sheet 2016 (în engleză). Disponibil la: http://www.who.int/mediacentre/factsheets/fs369/en/
Google Scholar
Poyares, D. R., Guilleminault, C., Ohayon, M. M., și Tufik, S. (2002). Poate valeriana să îmbunătățească somnul insomniacilor după retragerea benzodiazepinelor? Prog. Neuropsychopharmacol. Biol. Psychiatry 26, 539-545.
PubMed Abstract | Google Scholar
Sagi, S., Avula, B., Wang, Y.-H., și Khan, I. A. (2016). Cuantificarea și caracterizarea alcaloizilor din rădăcinile de Rauwolfia serpentina folosind cromatografia lichidă ultra-înaltă performanță-cromatografie-foto diode array-spectrometrie de masă. Anal. Bioanal. Chem. 408, 177-190. doi: 10.1007/s00216-015-9093-4
PubMed Abstract | CrossRef Full Text | Google Scholar
Sarris, J., Kavanagh, D., Byrne, G., Bone, K., Adams, J., and Deed, G. (2009). The Kava Anxiety Depression Spectrum Study (KADSS): un studiu încrucișat randomizat, controlat cu placebo, care utilizează un extract apos de Piper methysticum. Psychopharmacology 205, 399-407. doi: 10.1007/s00213-009-1549-9
PubMed Abstract | CrossRef Full Text | Google Scholar
Shimazaki, Y., Yajima, T., Takani, M. și Yamauchi, O. (2009). Complecși metalici care implică inele de indol: structuri și efecte ale interacțiunilor metal-indol. Coord. Chem. Rev. 253, 479-492. doi: 10.1016/j.ccr.2008.04.012
CrossRef Full Text | Google Scholar
Sichardt, K., Vissiennon, Z., Koetter, U., Brattström, A., și Nieber, K. (2007). Modularea potențialelor postsinaptice în neuronii corticali de șobolan prin extracte de valeriană macerate cu diferiți alcooli: implicarea adenozinei A1 și a receptorilor GABAA. Phytother. Res. 21, 932-937. doi: 10.1002/ptr.2197
PubMed Abstract | Text integral | Google Scholar
Vicknasingam, B., Narayanan, S., Beng, G. T., și Mansor, S. M. (2010). Utilizarea informală a ketum-ului (Mitragyna speciosa) pentru sevrajul opioidelor în statele nordice ale Malaeziei peninsulare și implicațiile pentru terapia de substituție a drogurilor. Int. J. Drug Policy 21, 283-288. doi: 10.1016/j.drugpo.2009.12.003
PubMed Abstract | CrossRef Full Text | Google Scholar
Vijeepallam, K., Pandy, V., Kunasegaran, T., Murugan, D. D., și Naidu, M. (2016). Extractul de frunze de Mitragyna speciosa prezintă un efect de tip antipsihotic cu potențialul de a atenua simptomele pozitive și negative ale psihozei la șoareci. Front. Pharmacol. 7:464. doi: 10.3389/fphar.2016.00464
PubMed Abstract | CrossRef Full Text | Google Scholar
Yi, L.-T., Li, J.-M., Li, Y.-C., Pan, Y., Xu, Q., și Kong, L.-D. (2008). Efecte comportamentale și neurochimice de tip antidepresiv ale apigeninei chimice asociate cu citricele. Life Sci. 82, 741-751. doi: 10.1016/j.lfs.2008.01.007
PubMed Abstract | CrossRef Full Text | Google Scholar
.