Pierwiastek chemiczny żelazo jest klasyfikowany jako metal przejściowy. Znany jest już od czasów starożytnych. Jego odkrywca i data odkrycia nie są znane.

Strefa danych
| Klasyfikacja: | Żelazo jest metalem przejściowym |
| Kolor: | srebrzysto-szary |
| Waga atomowa: | 55.847 |
| Stan: | stały |
| Temperatura topnienia: | 1535,1 oC, 1808.2 K |
| Punkt wrzenia: | 2750 oC, 3023 K |
| Elektrony: | 26 |
| Protony: | 26 |
| Neutrony w najobficiej występującym izotopie: | 30 |
| Powłoki elektronowe: | 2,8,14,2 |
| Konfiguracja elektronów: | 3d6 4s2 |
| Gęstość @ 20oC: | 7.87 g/cm3 |
Pokaż więcej, w tym: Ciepła, Energie, Utlenianie,
Reakcje, Związki, Promienie, Przewodności
| Objętość atomowa: | 7,1 cm3/mol |
| Struktura: | bcc: body-centered cubic |
| Twardość: | 4,0 mohs |
| Ciepło właściwe | 0,44 J g-1 K-1 |
| Ciepło topnienia | 13.80 kJ mol-1 |
| Ciepło atomizacji | 415 kJ mol-1 |
| Ciepło parowania | 349.60 kJ mol-1 |
| 1. energia jonizacji | 759,3 kJ mol-1 |
| 2. energia jonizacji | 1561.1 kJ mol-1 |
| 3. energia jonizacji | 2957,3 kJ mol-1 |
| powinowactwo elektronowe | 15.7 kJ mol-1 |
| Minimalna liczba utlenienia | -2 |
| Min. wspólna liczba utlenienia | 0 |
| Maksymalna liczba utlenienia | 6 |
| Maksymalna wspólna liczba utlenienia. | 3 |
| Elektroujemność (skala Paulinga) | 1,9 |
| Objętość polaryzacji | 8.4 Å3 |
| Reakcja z powietrzem | łagodna, ⇒ Fe3O4 |
| Reakcja z 15 M HNO3 | pasywowana |
| Reakcja z 6 M HCl | energiczna, ⇒ H2, FeCl2 |
| Reakcja z 6 M NaOH | – |
| Tlenek(i) | FeO, Fe2O3 (hematyt), Fe3O4 (magnetyt) |
| Wodorek(i) | brak |
| Chlorek(i) | FeCl2, FeCl3 |
| Promień atomowy | 140 pm |
| Promień jonowy (jon 1+) | – |
| Promień jonowy (2+ jon) | 77 pm |
| Promień jonowy (3+ jon) | 63 pm |
| Promień jonowy (1- jon) | – |
| Promień jonowy (2- jon) | – |
| Promień jonowy (3- jon) | – |
| Przewodność cieplna | 80.4 W m-1 K-1 |
| Przewodność elektryczna | 11.2 x 106 S m-1 |
| Temperatura zamarzania/topnienia: | 1535.1 oC, 1808,2 K |
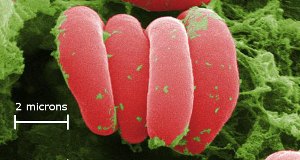
Czerwone krwinki – kolor pochodzi od żelaza w hemoglobinie. Komórki są powiększone x10,000. Gdybyś powiększył je x10 000, mógłbyś postawić stopy w Seattle, a rękami dotknąć Perth w Australii. Żelazo w hemoglobinie przenosi tlen w naszym ciele. Obraz Ref. (10)

Zbliżenie meteorytu żelaznego: Meteoryty takie jak ten były prawdopodobnie pierwszym źródłem żelaza dla naszych przodków. Jest to fragment meteorytu Sikhote-Alin – około 93% żelaza, 6% niklu i 1% innych pierwiastków. Powierzchnia meteorytu została stopiona na kształt odcisku kciuka podczas jego przelotu przez atmosferę naszej planety. Zdjęcie autorstwa Carla Allena, NASA JSC Photo S94-43472.

Złom żelaza i stali do recyklingu. Jakże czasy się zmieniły; żelazo było kiedyś warte osiem razy więcej niż złoto.
Odkrycie żelaza
Żelazo jest znane od czasów starożytnych.
Pierwsze żelazo używane przez ludzi prawdopodobnie pochodziło z meteorytów.
Większość obiektów spadających na Ziemię z kosmosu jest kamienna, ale niewielka część, taka jak ta na zdjęciu, to „meteoryty żelazne” o zawartości żelaza przekraczającej 90 procent.
Żelazo łatwo koroduje, więc żelazne artefakty z czasów starożytnych są znacznie rzadsze niż przedmioty wykonane ze srebra lub złota. To sprawia, że trudniej jest prześledzić historię żelaza niż mniej reaktywnych metali.
Artefakty wykonane z żelaza meteorytowego zostały znalezione około 5000 lat p.n.e. (a więc mają około 7000 lat) – na przykład żelazne koraliki w grobach w Egipcie. (1)
W Mezopotamii (Irak) istnieją dowody na to, że ludzie wytapiali żelazo około 5000 lat p.n.e.
Artefakty wykonane z wytapianego żelaza zostały znalezione w Egipcie i Mezopotamii od około 3000 r. p.n.e. (1), (2), (3)
W tamtych czasach żelazo było metalem ceremonialnym; było zbyt drogie, by używać go w życiu codziennym. Pisma asyryjskie mówią nam, że żelazo było osiem razy cenniejsze od złota. (1)
Era żelaza rozpoczęła się około 1300-1200 p.n.e., kiedy żelazo stało się wystarczająco tanie, by zastąpić brąz.
Dodawanie węgla do żelaza w celu wytworzenia stali było początkowo prawdopodobnie przypadkowe – połączenie roztopionego żelaza i węgla drzewnego z ognia przy wytopie. Stało się to prawdopodobnie około 1000 r. p.n.e. (4)
Dopóki to się nie stało, istniało niewiele technologicznych powodów, by epoka brązu ustąpiła miejsca epoce żelaza; techniki ulepszania żelaza przez dodawanie węgla (by zrobić stal) i obróbka na zimno były potrzebne, zanim żelazo stało się całkowicie preferowane od brązu. (5)
Żelazo było powszechnie używane w czasach rzymskich. W pierwszym wieku Pliniusz Starszy powiedział: „To z pomocą żelaza budujemy domy, rozłupujemy skały i wykonujemy tak wiele innych pożytecznych czynności w życiu.” (6)
Pochodzenie symbolu chemicznego Fe pochodzi od łacińskiego słowa „ferrum” oznaczającego żelazo. Samo słowo żelazo pochodzi od 'iren’ w języku anglosaskim.
Interesujące fakty o żelazie
- Uważa się, że jedna trzecia masy Ziemi to żelazo, z czego większość leży głęboko w planecie, w jej jądrze.
- Ziemia ma wystarczająco dużo żelaza, by stworzyć trzy nowe planety, każda o masie takiej samej jak Mars.
- Uważa się, że cyrkulacja płynnego żelaza głęboko w Ziemi tworzy prądy elektryczne, które tworzą pole magnetyczne naszej planety.
- Żelazo jest niezbędne dla rozwoju ludzkiego mózgu. Niedobór żelaza u dzieci prowadzi, wśród innych problemów, do upośledzenia zdolności uczenia się. (7)
- W czasach starożytnych ludzie nie wiedzieli, jak obficie występuje żelazo na Ziemi. Ich jedynym źródłem metalicznego żelaza były meteoryty. Z pism asyryjskich dowiadujemy się, że żelazo było osiem razy cenniejsze od złota. Oprócz swojej rzadkości, żelazo mogło być również bardzo pożądane, ponieważ, pochodząc z nieba, było uważane za dar od bogów: starożytni Egipcjanie nazywali je „ba-ne-pe”, co oznacza „metal z nieba”. Związek z niebem jest wzmocniony przez Teksty Piramid, które tłumaczą się na przykład na: 'moje kości to żelazo, a moje kończyny to nieśmiertelne gwiazdy’. (8) (9)
- Żelazo było pierwszym odkrytym metalem magnetycznym. Kamienie lodu były używane przez starożytnych nawigatorów, ponieważ mogły być używane jako kompasy, wskazując magnetyczny biegun północny; zostało to opisane przez starożytnego greckiego filozofa Talesa z Miletu w 600 r. p.n.e. Kamienie lodowcowe były wykonane z magnetytu, który jest naturalnie występującym tlenkiem żelaza. Wzór magnetytu to FeO.Fe2O3.
- Niektóre zwierzęta mają szósty zmysł – zmysł magnetyczny. Magnetyt został znaleziony w szerokiej gamie zwierząt, w tym pszczół miodnych, gołębi pocztowych i delfinów. Zwierzęta te są wrażliwe na ziemskie pole magnetyczne, co pomaga im w nawigacji.
- Meteoryt Hoba w Namibii jest największym naturalnie występującym kawałkiem żelaza na świecie, ważącym ponad 60 ton. Składa się z 82 – 83% żelaza, 16 – 17% niklu, około 1% kobaltu i bardzo małych śladów innych pierwiastków. Meteoryt Hoba jest największym pojedynczym meteorytem, jaki kiedykolwiek znaleziono.
- Żelazo jest ferromagnetykiem. Ferromagnetyzm jest najsilniejszym rodzajem magnetyzmu. Innymi popularnymi metalami ferromagnetycznymi są nikiel i kobalt.
- Bardzo silne magnesy mogą być wykonane przy użyciu żelaza, niklu lub kobaltu w połączeniu z metalami ziem rzadkich. Magnesy NIB (Neodym – Żelazo – Bor) zostały wynalezione na początku lat 80-tych. Są one stopem w proporcjach Nd2Fe14B. Są stosowane w komputerach, telefonach komórkowych, sprzęcie medycznym, zabawkach, silnikach, turbinach wiatrowych i systemach audio.



Wygląd i właściwości
Szkodliwe skutki:
Żelazo jest uważane za nietoksyczne.
Właściwości:
Żelazo jest plastycznym, szarym, stosunkowo miękkim metalem i jest umiarkowanie dobrym przewodnikiem ciepła i elektryczności.
Jest przyciągane przez magnesy i może być łatwo namagnesowane.
Czysty metal jest chemicznie bardzo reaktywny i łatwo rdzewieje w wilgotnym powietrzu, tworząc czerwono-brązowe tlenki.
Istnieją trzy alotropowe formy żelaza, znane jako alfa, gamma i delta.
Żelazo alfa, znane również jako ferryt, jest stabilną formą żelaza w normalnych temperaturach.
Użytki żelaza
Żelazo jest najtańszym i najważniejszym ze wszystkich metali – ważnym w tym sensie, że żelazo jest przeważnie najczęściej używanym metalem, stanowiącym 95 procent światowej produkcji metali.
Żelazo jest używane do produkcji stali i innych stopów ważnych w budownictwie i produkcji.
Żelazo jest również istotne dla funkcjonowania organizmów żywych, transportując tlen we krwi poprzez cząsteczkę hemoglobiny.
Abundance and Isotopes
Abundance earth’s crust: 5.6 % weight, 2.1 % by moles
Abundance solar system: 1000 parts per million by weight, 30 parts per million by moles
Cost, pure: $7.2 per 100g
Cost, bulk: $0.02 per 100g
Source: Żelazo nie występuje w stanie wolnym w przyrodzie, ale znajduje się w rudach żelaza, takich jak hematyt (Fe2O3), magnetyt (Fe3O4) i takonit. W handlu żelazo jest produkowane w piecu w temperaturze około 2000 oC przez redukcję hematytu lub magnetytu węglem.
Izotopy: Żelazo posiada 24 izotopy, których okresy półtrwania są znane, o liczbach masowych od 46 do 69. Naturalnie występujące żelazo jest mieszaniną czterech izotopów i występują one w podanych procentach: 54Fe (5,8%), 56Fe (91,8%), 57Fe (2,1%) i 58Fe (0,3%).

- Henry Maryon, Early Near Eastern Steel Swords., 65, 1961, American Journal of Archaeology p1.
- Michael D. Fenton, Mineral Commodity Profiles – Iron and Steel., 2005, U.S. Geological Survey.
- R. J. Forbes, Studies in Ancient Technology., IX, 1965, p247.
- Michael Woods, Mary B. Woods, Ancient Machines: From Wedges to Waterwheels., 2000, p30, Runestone Press.
- Vincent C. Pigott, The Archaeometallurgy of the Asian Old World, 1999, p28, UPenn Museum of Archaeology.
- Mary Elvira Weeks, Discovery of the Elements., 2003, p5, Kessinger Publishing.
- http://www.ncbi.nlm.nih.gov/pubmed/17101454.
- John G. Burke, Cosmic Debris: Meteorites in History, 1986, p229, University of California Press.
- Robert G. Bauval, Investigation on the origins of the benben stone. 14, 1989, Dyskusje w egiptologii.
- Image: CDC
Cite this Page
W przypadku linkowania online, proszę skopiować i wkleić jeden z następujących elementów:
<a href="https://www.chemicool.com/elements/iron.html">Iron</a>
lub
<a href="https://www.chemicool.com/elements/iron.html">Iron Element Facts</a>
Aby zacytować tę stronę w dokumencie akademickim, proszę użyć następującego cytatu zgodnego z MLA:
"Iron." Chemicool Periodic Table. Chemicool.com. 06 Oct. 2012. Web. <https://www.chemicool.com/elements/iron.html>.
.