Określanie śladowych związków organicznych w analizie żywności ma duże znaczenie dla aspektów jakości i bezpieczeństwa żywności. Zarówno oddzielenie analitu od potencjalnych zanieczyszczeń w matrycy żywności, jak i jakościowe i ilościowe oznaczenie związku docelowego, są istotnymi etapami w analitycznej chemii żywności.
Definicja
Chromatografia cieczowa (LC, tutaj High Performance LC – HPLC) jest fizyczną techniką rozdzielania stosowaną w analizie śladowej. Opiera się na oddziaływaniu analitu z fazą stacjonarną (kolumna z cząsteczkami) i fazą ruchomą (ciekły eluent lub mieszanina eluentów). Spektrometria masowa (MS) jest narzędziem analitycznym do pomiaru składu próbki. MS generuje użyteczne informacje o masie cząsteczkowej i strukturze analitów oraz pomaga w identyfikacji nieznanych związków. Połączenie LC/MS, LC-MS jest potężną techniką, ze względu na bardzo wysoką czułość (do zakresu ppt) i specyficzność. W obszarze organicznej analizy śladowej, MS znajduje wiele zastosowań, ale w przeciwieństwie do GC/MS (Gas Chromatography, coupled with Mass Spectrometry), dedykowana jest do analizy próbek zawierających nielotne cele analityczne, zwykle o masie w przedziale 200 – 800u, które są termicznie labilne, wykazują wysoką polarność lub mają wysoką masę cząsteczkową.
Webinarium: Strategia zapobiegania oszustwom żywnościowym – globalna perspektywa w zakresie testowania, monitorowania i weryfikacji
W tym webinarium omówiono rolę, jaką testowanie autentyczności żywności może odegrać w strategii zapobiegania oszustwom żywnościowym. Podkreśla również potrzebę holistycznego podejścia, które obejmuje identyfikację ryzyka, wdrożenie planu zapobiegania oszustwom żywnościowym, zarządzanie łańcuchem dostaw, kulturę bezpieczeństwa żywności w firmie oraz badania laboratoryjne.
REGISTER NOW
Zasada działania
Zasadniczo urządzenie LC/MS musi wykonywać cztery kroki robocze, w tym:
- Chromatograficzne rozdzielenie analitów przez kolumnę rozdzielającą
- Ionizacja analitów
- Isolacja jonów i
- Identyfikacja jonów
Ogólnie rzecz biorąc, interfejs systemu HPLC ze spektrometrem mas nie jest trywialny, ponieważ trudność polega na przekształceniu solutu w jon w fazie gazowej. Wyzwaniem jest pozbycie się rozpuszczalnika przy jednoczesnym utrzymaniu odpowiedniego poziomu próżni w spektrometrze mas oraz wygenerowanie jonów w fazie gazowej. Dlatego składniki eluujące z kolumny chromatograficznej są wprowadzane do spektrometru mas poprzez wyspecjalizowany interfejs.
Dwa najczęściej stosowane systemy interfejsów jonizacyjnych, jonizacja chemiczna pod ciśnieniem atmosferycznym (APCI) i jonizacja elektrospray (ESI) są wybierane w zależności od właściwości fizykochemicznych analitów (tj. polarności i kwasowości). Jonizacja odbywa się przy ciśnieniu atmosferycznym i obie są uważane za miękką metodę jonizacji, tj. widmo masowe dostarcza głównie informacji o masie cząsteczkowej, chyba że stosowane są techniki fragmentacji.
Ponieważ związki częściowo współelastują z systemu chromatograficznego, jednoznaczne przypisanie poszczególnych fragmentów nie może być osiągnięte przy użyciu tylko LC-MS, gdzie dostępne są tylko masy jonów cząsteczkowych. Aby przezwyciężyć ten problem, stosuje się obecnie głównie tandemową spektrometrię mas (MS/MS), która obejmuje wiele etapów selekcji lub analizy mas (LC/MS/MS lub LC/MSn). Systemy te są w stanie oznaczać pozostałości w dolnym zakresie ppt. Do kwalifikacji cząsteczek organicznych konieczny jest inny techniczny układ MS. Jednym z możliwych podejść do kwalifikacji jest wykorzystanie MS, który generuje jony, prowadzi je do liniowej pułapki jonowej, a następnie przechowuje je w polu o częstotliwości radiowej. Następnie, różne możliwości techniczne umożliwiają kwalifikację jonów, a tym samym nieznanego związku.
Zastosowania
Od czasu wprowadzenia LC/MS do rutynowych analiz około dziesięć lat temu, LC/MS został ustanowiony w większości obszarów chemii analitycznej, np. kontrola jakości, badania podstawowe i stosowane oraz kontrola rządowa.
Następujące przykłady stanowią krótki przegląd:
a) Farmacja
- Badania farmakokinetyczne farmaceutyków, np. procesy degradacji leków
- Rozwój leków, np. identyfikacja metabolitów lub identyfikacja zanieczyszczeń
b) Biologia molekularna
- Proteomika, np. badania białek na dużą skalę, w szczególności ich struktury i funkcji
- Metabolomika, np.g. oznaczanie półproduktów metabolicznych, hormonów i innych cząsteczek sygnalizacyjnych
c) Środowisko
- Ścieki, np. związki endokrynne
- Gleba, np. metaloorganiczne
d) Żywność
- Składniki, np. aminokwasy, lipidy
- Zanieczyszczenia, np. analiza wielopozostałościowa pestycydów, toksyn z owoców morza, pozostałości weterynaryjnych, oznaczanie barwników, akrylamidu, analiza mikrocystyn
- Produkty naturalne, np. terpeny, steroidy
Tenzydy perfluorowane (PFC) jako przykład w analizie żywności
Tło
PFC jest doskonałym przykładem połączenia złożonego przygotowania próbki z zaawansowanymi urządzeniami LC/MS i głęboką wiedzą z zakresu chemii analitycznej. Unikalne właściwości PFT sprawiają, że są one użyteczne w wielu produktach przemysłowych i komercyjnych, takich jak płyny chłodzące, polimery oraz jako składniki farmaceutyków i pestycydów. W szczególności perfluorowane karboksylany (np. PFOA – kwas perfluorooktanowy) i perfluorowane sulfoniany (np. PFOS – kwas perfluorooktanosulfonowy) są stosowane jako środki powierzchniowo czynne, np. do impregnacji tekstyliów i dywanów, w piankach przeciwpożarowych oraz w impregnacji przeciwtłuszczowej w przemyśle papierniczym. PFC produkuje się od ponad 50 lat, a obecnie są one rozprowadzane na całym świecie. Jeśli wiązania C-H nie zostaną całkowicie zastąpione wiązaniami C-F, jednymi z najsilniejszych znanych wiązań chemicznych, degradacja jest nadal możliwa.
Tylko PFOA i PFOS są oceniane toksykologicznie (chronicznie toksyczne i rakotwórcze), wszystkie inne związki homologiczne, izomery itp. nie są jeszcze oceniane. Z fizycznego punktu widzenia PFC są zarówno trwałe (tj. nie ulegają rozkładowi), jak i mobilne (tj. mogą przenikać ze skażonych gleb do wód gruntowych). Stanowi to stałe zagrożenie w kontekście poboru i/lub uzdatniania wody pitnej. Ponadto transfery roślinne wprowadzają te związki do łańcucha pokarmowego.
Odkrycie wysokich poziomów zanieczyszczenia PFC w dwóch niemieckich rzekach w 2006 r. spowodowało zainteresowanie opinii publicznej tymi związkami.
Zanieczyszczenie z 2006 r. mogło pochodzić z osadów organicznych, stosowanych jako nawóz w celach rolniczych. Wykazano, że gleba zawiera do 600 µg PFC/kg, co spowodowało skażenie wody pitnej i zakładów wodociągowych. Do tej pory siedem niemieckich krajów związkowych zgłosiło skażenie PFC.
Fraunhofer IME
Jedną z podstawowych kompetencji Fraunhofer Institute for Molecular Biology and Applied Ecology jest opracowywanie wykonalnych i wiarygodnych metod identyfikacji i analizy zanieczyszczeń chemicznych w żywności i matrycach środowiskowych.
Od 1999 roku Fraunhofer IME realizuje projekty mające na celu pomiar skażenia PFC w różnych matrycach środowiskowych. Prace te były prowadzone w imieniu partnerów przemysłowych i koncentrowały się w szczególności na karboksylanach PFC i sulfonianach PFC. Dalsze badania przeprowadzono na zlecenie Programu Monitoringu Niemieckiego Federalnego Banku Wzorców Środowiskowych, które obejmowały również próbki krwi ludzkiej. W 2005 r. przeprowadzono pierwsze badania w zakresie produktów spożywczych, a w 2006 r. wyniki wybranych próbek żywności (np. mleko matki, frytki) były również omawiane w mediach. Większe projekty koncentrujące się na transferze roślin, ziemniakach i produktach, matrycach ludzkich (krew i mleko matki), jak również próbkach środowiskowych (np. ścieki, osady i gleba) zostały przeprowadzone w 2007 roku.
Rozwiązanie analityczne
W celu pokrycia wszystkich możliwych matryc próbek zastosowano trzy różne sposoby przygotowania próbek:
- IPE (Ion pair extraction). Użycie czynnika parującego jony – hydrogensiarczanu tetra-n-butyloamoniowego, po którym następuje ekstrakcja cieczą stałą (np. próbki środowiskowe)
- AAE (ekstrakcja kwasowo-zasadowa). Usuwanie lipidów heksanem o pH 14 (ciekły roztwór amoniaku), doprowadzenie do pH 1 kwasem solnym i ekstrakcja eterem tert-butylowo-metylowym (np. mleko matki)
- SPE (ekstrakcja do fazy stałej, obecnie najczęściej cytowana metoda) z wkładami o różnej polarności w zależności od charakteru jonowego PFC w zbuforowanym medium (np.
Ważnie zalecane jest stosowanie wewnętrznych wzorców do kalibracji; obecnie w naszych metodach stosujemy dziewięć wzorców PFC znakowanych masowo. Przed wprowadzeniem próbek do LC/MS, samo urządzenie musi być sprawdzone pod kątem części zamiennych pokrytych teflonem, ponieważ zawierają one emitujący PFC, który będzie wpływał na wyniki w sposób niereprodukowalny. Te części muszą być wymienione, co wymaga doskonałej znajomości komponentów LC/MS.
Przykład analityczny
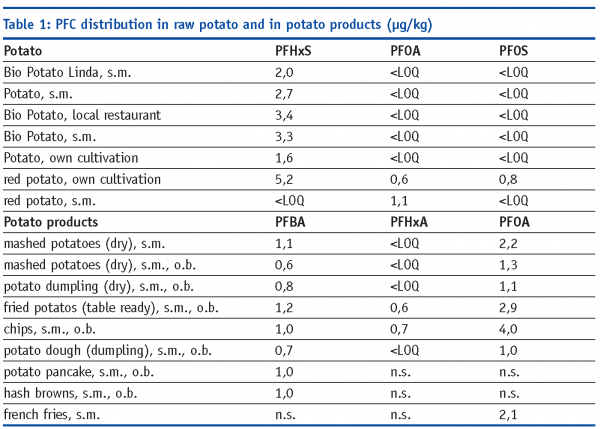
Do analiz surowego ziemniaka i produktów ziemniaczanych dostosowaliśmy nasze LC/MS/MS (HPLC Alliance 2695 z Quattro Ultima Pt w trybie negatywnym Electrospray, oba Waters; kolumna 150 x 2 mm Luna 3 µm C18(2), Phenomenex) dla mas docelowych 9 kwasów perfluorokarboksylowych (C4 – C12) i 3 kwasów perfluorosulfonowych (C4, C6, C8) przy użyciu materiałów odniesienia znakowanych 13C (LOQ 0.5 µg/Kg) po przygotowaniu próbki metodą SPE.
PFCs wykazały różną dystrybucję w surowym ziemniaku i w produktach ziemniaczanych, (Tabela 1) co pozwala przypuszczać, że zanieczyszczenie nastąpiło podczas przetwarzania, jak również zanieczyszczenie gleby. Potwierdzają to nasze badania frytek PFC z 2006 roku, gdzie analizowaliśmy frytki z restauracji typu fast food i stwierdziliśmy do 2,8 µg PFOA/kg i do 0,9 µg PFOS/kg.
Perspektywy analizy
Inżynieria Fraunhofera posiada znaczącą wiedzę i doświadczenie w analizie PFC, które mogą być zastosowane w wielu obszarach skażenia środowiska/żywności PFC, które nie zostały jeszcze zbadane. Ważne obszary przyszłych badań nad PFC mogą obejmować zwiększenie liczby analitów, wiele krótko- i długołańcuchowych PFC jest już uwzględnionych w naszym programie badawczym, ale nasze możliwości analityczne mogłyby zostać ulepszone poprzez włączenie dodatkowych PFC. Dodatkowe PFC muszą być identyfikowane za pomocą LC/MS, ponieważ komercyjne standardy nie są dostępne. Doprowadzi to do skonsolidowanych ustaleń dotyczących prekursorów, dróg skażenia żywności i degradacji podczas przetwarzania żywności.
.