Generic Name: プロパラカイン塩酸塩
剤形:点眼液
Drugs.comによる医療用医薬品レビュー。 最終更新日:2020年10月1日
- 概要
- 副作用
- プロフェッショナル
- 相互作用
- その他
Ophthalmic Solution, USP
0.5% Sterile
Rx Only
DESCRIPTION:
Proparacaine Ophthalmic Solution USP, 0.5% は眼科用局所麻酔剤です。 1mLの無菌水溶液に含まれています。 活性剤。 塩酸プロパラカイン 5 mg (0.5%)。 不活性剤。 安定剤としてのグリセリン、pH調整(3.5~6.0)のために塩酸および水酸化ナトリウムを添加することがある、および注射用水。 防腐剤。 9917>
Proparacaine hydrochlorideは、2-(Diethylamino)ethyl 3-amino-4-propoxybenzoate monohydrochlorideとして化学的にデザインされています。 有効成分は、構造式:
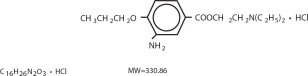
CLINICAL PHARMACOLOGY:
Proparacaine Hydrochloride Ophthalmic Solutionは、眼科用に適した速効性局所麻酔剤です。 プロパラカインの作用部位は神経細胞膜で、通常、膜のわずかな脱分極によって生じるナトリウムイオンに対する膜透過性の大きな一過性の上昇を阻害します。 神経で麻酔作用が徐々に発現すると、電気刺激に対する閾値が徐々に上昇し、伝導に対する安全係数が低下する。この作用が十分に発現すると、伝導の遮断が生じる。
プロパラカインおよび他の局所麻酔薬が細胞膜の透過性に影響を与える正確なメカニズムは不明であるが、いくつかの研究から、局所麻酔薬は神経細胞膜の脂質層でイオンが移動する孔を閉鎖してナトリウムイオン透過性を制限すると考えられている。
効能・効果:
プロパラカイン塩酸塩点眼液は、眼科領域における局所麻酔を適応としています。 眼科領域では、眼圧測定(眼圧計)、角膜異物・縫合糸の除去、診断における結膜の擦過、眼底鏡検査などで良好な局所麻酔が得られるほか、白内障手術などの外科的手術前の局所麻酔薬として使用することができる。
禁忌:
この製剤は、溶液のいずれかの成分に対して既知の過敏症を有する患者には禁忌である。
警告:
注射用としては使用しないこと。
局所眼科用麻酔薬の長期使用は、視力喪失を伴う永久的な角膜混濁を生じることがあります。
注意事項:
一般
プロパラカインは周知のアレルギー、心疾患または甲状腺機能亢進症の患者では慎重かつ控えめに使用する必要があります。 プロパラカインの長期毒性は不明であり、長期間の使用は創傷治癒を遅らせる可能性がある。 局所麻酔薬の眼科適用では非常にまれですが、全身毒性(中枢神経系の刺激とそれに続く抑圧によって示される)が発生する可能性があることを心に留めておく必要があります。
麻酔の期間中に刺激性の化学物質、異物および摩擦から目を保護することは、非常に重要です。 滅菌液や洗剤に浸した眼圧計は、使用前に滅菌蒸留水で十分に洗浄する必要がある。 麻酔が切れるまで、眼に触れないように患者に指導すること。
発がん性、変異原性、生殖能の障害
動物における長期的な研究では、発がん性、変異原性、雄または雌における生殖能力の障害の可能性は評価されていない
妊娠。
妊娠:催奇形性
区分C
プロパラカイン塩酸塩点眼液では、動物の繁殖に関する試験は実施されていません。 また、プロパラカイン塩酸塩を妊婦に投与した場合に胎児に害を及ぼす可能性があるか、または生殖能力に影響を及ぼす可能性があるかは分かっていません。 プロパラカイン塩酸塩は明らかに必要な場合のみ妊婦に投与してください。
授乳婦
この薬が母乳中に排泄されるかどうかは分かっていません。 多くの薬剤がヒト乳汁中に排泄されるため、プロパラカイン塩酸塩を授乳婦に投与する場合は注意すること。
小児用
プロパラカイン塩酸塩点眼液では、小児患者における安全性と有効性を確立するための対照臨床試験が行われていない。しかし、文献では小児患者の局所眼科麻酔剤としてプロパラカイン塩酸塩が用いられていることが引用されいる。
ADVERSE REACTIONS:
Pupillary dilatation or cycloplegic effects are rarely observed with Proparacaine hydrochloride. 他の局所麻酔薬に感受性のある患者への使用は安全であると思われるが、局所的または全身的な過敏症が時折発生する。 推薦された濃度および適量の目への Proparacaine の注入は通常最初の刺激、刺すような痛み、焼跡、結膜の赤み、流涙または増加のまばたきをほとんど作り出しません。
まれに、重度の即時型、明らかに過アレルギー性の角膜反応が起こることがあり、これには急性、強度、拡散性の上皮角膜炎、灰色、すりガラス状の外観、広範囲の壊死した上皮の剥離、角膜フィラメント、時には落屑性炎を伴う虹彩炎があります。
指先の乾燥と亀裂を伴うアレルギー性接触皮膚炎が報告されている。
角膜上皮の軟化と侵食、結膜充血と出血が報告されている。
用法・用量:
白内障摘出時のような深部麻酔:
5~10分ごとに1滴を5~7回に分けて眼に注入する。
抜糸:
抜糸の2~3分前に1~2滴を眼に点眼する。
異物除去:手術前に1~2滴を点眼する。
検眼:
検眼の直前に1~2滴点眼する。
プロパラカイン塩酸塩点眼液USP、0.5%は15mLプラスチックスポイトボトル(NDC 13985-611-15
)で供給されます。 ボトルはしっかり閉めて保管してください。 光から保護するため、空になるまでカートンで保管してください。
警告-これおよびすべての医薬品を子供の手の届かないところに保管してください。
apexa™
Manufactured by.S.A.A.T.S.社。
Lake Forest, IL 60045
製造元:Akorn Inc.
販売元:Akorn Inc: MWI
Boise, ID 83705
MWPR00N Rev. 08/14
容器ラベルの主要表示パネルテキスト:
NDC 13985-611-15
Proparacaine Hydrochloride
Ophthalmic Solution, USP 0.5%
局所用
眼科用のみ。
注射用ではない。
Apexa logo STERILE
Rx Only
AP 704013 15 mL

カートンラベル用主要表示パネルテキスト。
NDC 13985-611-15
Proparacaine
Hydrochloride
Ophthalmic
Solution
USP, 0.5%
外用
眼科用のみ。
注射用ではない。
STERILE
Rx Only
Apexa logo
AP 704013 15 mL
| Proparacaine HYDROCHLORIDE Proparacaine HhydrophluorIDE solution/ drops |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
| マーケティング情報 | |||||||||||||
| マーケティングカテゴリ | アプリケーション番号またはモノグラフ引用 | 販売開始日 | 販売終了日 | ||||||||||
| ANDA | 03/27/2015 | ||||||||||||
Labeler – (ラベル)。 MWI (019926120)
登録者-。 Akorn Operating Company LLC (117693100)
| Establishment | |||
| 名前 | 住所 | ID/FEI | オペレーション |
| Akorn, Inc | 117696790 | PACK(13985-611)。 LABEL(13985-611) | |
| Establishment | |||
| 名前 | 住所 | ID/FEI | 運営 |
| アコン株式会社 | |||
| 117696832 | 製造(13985-611)、分析(13985-611)、殺菌(13985-611) | ||