酸化リチウムの化学的性質、用途、生産
化学的性質
酸化リチウム(Li2O)は最も単純なイオン酸化物の一つでH2Oと等電荷であり、H2OはLi2Oに等しい。 2個のリチウム原子がそれぞれ1個の電子を酸素原子に与えることにより、リチウムと酸素の間にイオン結合が形成されます。 酸化リチウムの式はLi2Oです。
酸化リチウムは非常に腐食性が高いです。 水と反応して水酸化リチウムになる。 強いアルカリ性(塩基性)であるため毒性があります。
ガラス、光学、セラミック用途に適した、非常に不溶性の熱的に安定したリチウム源です。 酸化リチウムは、リチアとしても知られる白色の固体で、リチウム金属が酸素の存在下で燃焼したときに生成されます。 酸化物化合物は電気を通しません。 しかし、ペロブスカイト構造の酸化物は電気を通すため、固体酸化物形燃料電池のカソードや酸素発生システムに応用されている。 酸化リチウムは、少なくとも1つの酸素アニオンと1つの金属カチオンを含む化合物です。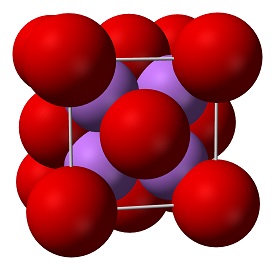
セラミック釉薬のフラックスとして使われ、銅で青色、コバルトでピンク色を作り出します。 酸化リチウムは水や蒸気と反応し、水酸化リチウムを形成するので、それらから分離する必要があります。 また、非破壊発光分光分析による評価や遮熱コーティングシステム内の劣化モニタリングへの利用が検討されている。 ジルコニアセラミックのトップコートにイットリアと共添加しても、コーティングの期待耐用年数を大きく低下させることはない。
用途 酸化リチウムを大量に消費するような工業的用途は現在ありません。
酸化リチウムはセラミック釉薬のフラックスとして使われ、銅で青色、コバルトでピンク色を作り出します。 酸化リチウムは水や蒸気と反応し、水酸化リチウムを形成するので、それらから分離する必要があります。その用途は、遮熱コーティングシステム内の非破壊発光分光評価および劣化監視のためにも研究されています。 ジルコニアセラミックのトップコートにイットリアと共添加しても、コーティングの期待耐用年数を大きく低下させることはない。
反応
酸化リチウムは溶解する際に水と反応し、水酸化リチウムの溶液を形成します。
酸化リチウムは強塩基で、通常は酸性のガスや液体と反応しリチウム塩を形成します。 高温では、酸化リチウムは多くの固体非金属酸化物(SiO2、B2O3など)および金属酸化物(A12O3、Fe2O3など)とも反応する。 酸化リチウム、水酸化リチウム、炭酸リチウムのフラックス作用の基本は高温反応である。 酸化リチウムは高温で反応容器と反応しないように注意する必要があります。
調製法
酸化リチウムは、乾燥酸素中で金属リチウムを100℃以上に加熱して調製する:
4Li + O2→2Li2O
純粋な酸化リチウムを得るもう一つの調製法には、過酸化リチウムの熱分解を含む。
2Li2O2→2Li2O+O2
また、純粋な水酸化リチウムを真空中で800℃に加熱すると酸化物ができる:
2LiOH→Li2O+H2O
健康被害
我々の知る限り、酸化リチウムの化学、物理、毒性は十分に調査、報告されたことがない。
リチウム化合物の毒性は、水への溶解度の関数である。 リチウムイオンは中枢神経系に毒性を示す。 リチウム曝露の初期効果は、手の震え、吐き気、排尿、滑舌、だるさ、眠気、めまい、口渇、尿量増加である。 継続的な暴露による影響は、無気力、食欲不振、疲労、無気力、筋力低下、心電図の変化などである。 長期にわたる暴露は、甲状腺機能低下症、白血球増加、浮腫、体重増加、多飲・多尿(水分摂取の増加による尿量の増加)、記憶障害、痙攣、腎障害、ショック、低血圧、不整脈、昏睡、死亡に至る。
化学的性質
細かく分割された白色の粉末または痂皮状の物質、大気中の二酸化炭素と水を容易に吸収する、LiOHを真空中で800℃まで加熱するか過酸化リチウムの熱分解によって作られる、セラミックス、特殊ガラス製剤、リチウム熱電池に使用
用途
酸化リチウムは強アルカリで大気中から二酸化炭素と水を吸収する。 セラミックスや特殊ガラスの製造に使用される。
用途
セラミックスおよび特殊ガラスの製剤、二酸化炭素吸収剤
調製法
工業用および実験室用調製品。 工業的には少量の材料しか調製されない。
過酸化リチウムLi202は、ヘリウムガス気流中で450°に加熱すると、酸化リチウムLi20と酸素に変換される。
水酸化リチウムの熱脱水は、銀箔を敷いたニッケル容器中で真空下675℃±10°で行われる。
炭酸リチウムは、白金ボート中で真空下700℃に加熱すると酸化リチウムと炭酸ガスに変換される。
酸化リチウムは水と反応して溶解し、水酸化リチウムの溶液を形成します。酸化リチウムは強塩基で、通常は酸性の気体や液体と反応してリチウム塩を形成します。 また、高温では、酸化リチウムは多くの固体非金属酸化物(Si02、B2O3など)および金属酸化物(A1203、Fe2C>3など)と反応します。 酸化リチウム、水酸化リチウム、炭酸リチウムのフラックス作用は、高温での反応が基本です。 酸化リチウムは高温で反応容器と反応しないように注意しなければならない。