Background
Artemisia annua egy kínai gyógynövény (más néven “qing hao” vagy “édes üröm”), amelynek maláriaellenes hatása jól bizonyított (1). Az Egészségügyi Világszervezet (WHO) az artemizinin-származék alapú kombinált terápiákat (ACT) ajánlja a szövődménymentes malária kezelésére, hatékony maláriaellenes szerekkel kombinálva (2). Az utazók kemoprofilaxisa a malária-endémiás úti céltól függ, és magában foglalja az atovaquon/proguanil, klorokin, doxiciklin, mefloquin vagy primaquin kombinációját (3, 4). Artemisinin-származék kemoprofilaxis mellett leírtak maláriafertőzéses eseteket (5), és a WHO nem javasolja az A. annua növényi anyag bármilyen formában, beleértve a teát is, használatát a malária kezelésére vagy megelőzésére (6).
A gyógynövény- és étrend-kiegészítőket (HDS) világszerte egyre gyakrabban használják, és a HDS-indukált májkárosodás egyre nagyobb aggodalomra ad okot (7). Az ACT-ok széles körű alkalmazása ellenére a malária-endémiás területeken az artemisinin-származékok májkárosodása ritka (8, 9). Kumar beszámolt egy beteg esetéről, akinél 6 héttel azután alakult ki kolesztatikus májkárosodás, hogy általános egészségmegőrzés céljából artemizinint tartalmazó gyógynövény-kiegészítőt szájon át szedett (10). Az Artemisia annua által kiváltott májkárosodással kapcsolatban néhány más közlemény is megjelent (9, 11-14). A Kínai Kínai Orvostudományi Társaság a közelmúltban javasolt egy klinikai iránymutatást a gyógynövények okozati összefüggéseinek értékelésére és a gyógynövények okozta májkárosodás diagnózisának felállítására (15). Egy Etiópiából hazatérő betegnél kemoprofilaxisként fogyasztott Artemisia tea miatt kialakult akut kolesztatikus májgyulladás esetét mutatjuk be.
Az eset leírása
Egy 51 éves férfi 4 napja tartó rossz közérzettel, hasi panaszokkal, lebegő sárga széklettel, sárgasággal és choluriával, valamint az elmúlt 6 hétben 6-8 kg-os súlyvesztéssel jelentkezett a bázeli egyetemi kórház sürgősségi osztályán. Az orvosi ellátás igénybevétele előtt 3 héttel tért vissza egy 4 hetes etiópiai utazásról. Etiópiai tartózkodása alatt naponta 1,25 g Artemisia annua porteát fogyasztott malária kemoprofilaxisként. Az esetek 90%-ában a port forró vízben hígította, a maradék 10%-ban a port étellel keverve fogyasztotta. A kiegészítőt az interneten keresztül vásárolta. A beteg rendelkezésünkre bocsátotta a tartályt, amely eredetileg 50 g sötétzöld port tartalmazott (1. ábra). A bemutatáskor 2 g volt a tartályban, ami azt jelzi, hogy összesen 48 g-ot fogyasztott el. Etiópiai tartózkodása alatt más teaszerű készítményeket is fogyasztott. Tudomásunk szerint ezekkel az anyagokkal kapcsolatban nem írtak le hepatotoxicitást. Tagadta, hogy bármilyen más vényköteles, vény nélkül kapható vagy növényi gyógyszert szedne. Korábban vagy a családjában nem volt májbetegség, alkohol- vagy drogfogyasztás, illetve vírusos hepatitis kockázati tényezője. Elmondta, hogy felesége, aki elkísérte őt az etiópiai útjára, szintén fogyasztott Artemesia annua teát malária megelőzés céljából. Az asszony mindvégig jól maradt.

1. ábra. Artemisia annua por tea.
A kifejezett sárgaságtól eltekintve jó általános állapotban volt, és az életjelei nem voltak feltűnőek (lázmentes, normális vérnyomással, pulzusszámmal és légzésszámmal).
A laboratóriumi vizsgálatok a következőket mutatták: alanin-aminotranszferáz (ALAT) 91 U/L (normál, 9-59); aszpartát-aminotranszferáz (ASAT) 42 U/L (normál, 9-34); alkalikus foszfatáz (ALP) 151 U/L (normál, 40-130); gamma-glutamil-transzferáz (GGT) 416 U/L (normál, 12-68); teljes bilirubin 186 U/L.6 μmol/l (normális, 0-24) (konjugált bilirubin 168,5 μmol/l); és nemzetközi normalizált arány (INR) 0,9 (normális, 0,9-1,3). Az epesavszint 460,5 μmol/L-es al-szintre emelkedett (normális, 0-8,0). A differenciál vérkép és a c-reaktív fehérje normális volt. Enyhe hyponatremia és hypochloremia volt jelen, ami összhangban volt a beteg előző napokban megnövekedett vízbevitelével. Az akut hepatitis A, B, C és E, az Epstein-Barr-vírus és a citomegalovírus fertőzés szerológiai tesztjei negatívak voltak. A koeruloplazmin normális volt. A májspecifikus autoantitestek (anti-nukleáris antitest, anti-nutrofil antitest, anti-simaizom antitest, anti-mitokondriális antitest, anti-proteináz 3 antitest és anti-myeloperoxidáz antitest) negatívak voltak, és az IgA, IgM és IgG a normál tartományon belül volt. A hasi ultrahangvizsgálat normális májparenchimát, ereket és epeutakat mutatott. A máj elasztográfiája emelkedett volt (FibroScan, 12,7 kPa, normál tartomány <5 kPa).
A beteget a Svájci Trópusi és Közegészségügyi Intézetben is megvizsgálták különböző lehetséges fertőző alapbetegségek szempontjából. A rickettsia foltos láz elleni antitestek pozitívak voltak, azonban ezt nem tekintették a klinikai megjelenéssel összefüggőnek, és nem kezdtek antibiotikus terápiát.
A kezdeti májbiopszia portális hepatitist mutatott az epevezetékek lymphocytás infiltrációjával és diffúz intra-canalicularis és intra-cytoplasmatikus bilirubinostasisszal. Sem fibrózis, sem parazita anyag nem volt látható (2A,B ábra). A perifériás vérből származó leukociták DNS-ének következő generációs szekvenálási elemzése az epesav-homeosztázis 3 legfontosabb májtranszporterét, nevezetesen a BSEP-t, az MDR3-at és a FIC1-et kódoló gének genetikai variánsaira nem talált az örökletes cholestatikus májbetegségekhez jellemzően társuló variánsokat.
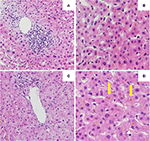
2. ábra. Az első (A,B) és a második (C,D) májbiopszia szövettana. (A) A májbiopszia kis teljesítményű nézete, melyen portális limfocita infiltrátum látható . (B) Májparenchima intracelluláris bilirubinosztázissal (HE, 20x). (C) A májbiopszia kis teljesítményű nézete jelentős portális gyulladás nélkül (HE, 10x). (D) Májparenchima jelentős intracelluláris és extracelluláris (nyíl) bilirubinosztázissal (HE, 20x).
Az Artemisia tea toxikológiai elemzése folyadékkromatográfia-tömegspektrometriával és gázkromatográfia-tömegspektrometriával a következő összetevőket mutatta ki: arteannuin b, dezoxiartemizin, kámfor és szkopoletin.
Naponta kétszer 20 mg prednizonnal és naponta kétszer 500 mg ursodeoxikolsavval kezdték meg a kezelést. A tartós sárgaság, valamint a kezelés ellenére 4 hét alatt emelkedő bilirubin miatt második májbiopsziát végeztek. A második biopszia súlyos intracitoplazmatikus, valamint intrakanalikuláris bilirubinosztázist mutatott, az első biopsziához képest csak minimális gyulladással (2C,D ábra). A kortikoszteroid-kezelést abbahagyták, az ursodeoxikolsavat a sárgaság megszűnéséig és a bilirubin (15,3 μmol/l) normalizálódásáig (3. ábra), valamint az epesavak releváns csökkenéséig (19,5 μmol/l) folytatták, ami három hónappal a betegség kezdete után következett be.
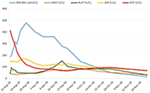
3. ábra. A bilirubin és a májenzimek időbeli alakulása.
Az esetet jelentették a svájci nemzeti gyógyszerkészítmény-felügyeleti hatóság (Swissmedic) farmakovigilanciai egységének. A résztvevőtől írásbeli beleegyezést kaptunk az esetről szóló beszámoló közzétételéhez.
Diszkusszió
Az artemisinin-származékok a malária kezelésének, de nem a kemoprevenciójának sarokkövei (2). Kiterjedt alkalmazásuk ellenére az artemisinin-származékok májkárosodását ritkán írták le (8, 10). Tudomásunk szerint ez az első esetismertetés egy akut cholestatikus májgyulladásról, amelyet Artemisia annua tea fogyasztása okozott.
A gyógynövények és étrend-kiegészítők által kiváltott májkárosodás egyre nagyobb érdeklődésre tart számot, mivel a HDS-eket világszerte egyre gyakrabban használják (7). A HDS-ek fogyasztását gyakran ártalmatlannak tekintik, azonban egyre több, a használatuk mellett fellépő mellékhatásról számoltak be (16). Továbbá, mivel a HDS-ek koncentrációja és összetétele gyakran nem szerepel a termékek címkéjén, a termék összetevőinek minősége és mennyisége ismeretlen marad. Esetünkben az Artemisia annua tea fogyasztása miatti HDS-indukált májkárosodás diagnózisát az expozíció és a mellékhatás kialakulása közötti szoros időbeli kapcsolat, valamint az egyéb lehetséges etiológiák hiánya indokolta. A RUCAM (Roussel Uclaf Causality Assessment Method) (17) szerint kiszámítottuk az ok-okozati értékelési pontszámot, és 6-os pontszámot kaptunk, ami az inkriminált gyógyszer “valószínűsíthető” okozati összefüggésének felel meg. A különböző tételeket a következőképpen pontozták: a betegség kezdetéig eltelt idő (+2), lefolyás (+1), kockázati tényezők (+1), egyidejűleg alkalmazott gyógyszerek (-1), a májkárosodás egyéb okainak kizárása (+2), a gyógyszer hepatotoxicitására vonatkozó korábbi információk (+1), az ismételt adagolásra adott válasz (0). A májbetegségnek nem volt más azonosítható etiológiája.
A korábban Kumar által leírt eset a májkárosodás hepatocelluláris mintázatát mutatta, amelyet elhúzódó kolesztatikus fázis követett (10). A mi betegünknél az Artemisia annua tea első fogyasztása után 5 héttel a májkárosodás túlnyomórészt cholestatikus mintázata jelentkezett. Feltételezzük, hogy a természetes lefolyás hasonló volt a Kumar esetéhez, de a mi betegünknél a májkárosodás kialakulásának későbbi szakaszában jelentkezett. Az elfogyasztott gyógynövénytea toxikológiai elemzése során ezen kívül szkopoletint és kámfort azonosítottunk, amelyek természetesen előfordulnak az Artemisia annua-ban (18, 19), és hozzájárulhattak a kolesztatikus májkárosodás kialakulásához.
Az artemisinin-származékok által kiváltott májkárosodás mechanizmusa továbbra is tisztázatlan. Az Artemisiae spp. kémiai összetevői közé tartoznak az illóolajok, flavonoidok, tanninok, triterpének és poliszacharidok. Az Artemisiae spp-ből származó illóolajok erős farmakológiai aktivitással és toxicitással rendelkeznek, és egy nemrégiben végzett bioinformatikai megközelítés különböző útvonalakat azonosított, amelyek részt vehetnek a májkárosodás kialakulásában (20). A gyógyszer okozta kolesztatikus májkárosodásra való hajlamot összefüggésbe hozták az epesó-export pumpa polimorfizmusával (21, 22). Ezért újgenerációs szekvenálással az epesavtranszporterek variánsait kerestük. A BSEP-t, a FIC1-et, illetve az MDR3-at kódoló ABCB11, ATP8B1 és ABCB4 génszekvenciákban (kódoló és flankáló régiókban) nem detektáltunk deléciót, duplikációt vagy patológiás variánst (4. ábra). Számos közös szekvencia-változatot azonosítottak azonban. Betegünk homozigóta hordozta az ABCB11 gén egy variánsát . Vitatott, hogy ez a polimorfizmus összefüggésbe hozható-e a jóindulatú, visszatérő és/vagy progresszív familiáris intrahepatikus cholestasisszal és a terhesség intrahepatikus cholestasisával (23, 24). Ezenkívül az ABCB11 génben egy másik gyakori variánst is kimutattak heterozigóta állapotban . Ezt a variánst csökkent fehérjeexpresszióval (25) és primer epeúti cirrózissal hozták összefüggésbe (26, 27). Mindkét genetikai variáns azonban túlságosan gyakori az általános populációban ahhoz, hogy ok-okozati összefüggésben álljon a kolesztatikus májbetegségekkel (28). A transzkriptom szisztematikus szekvenálása ilyen esetekben a génszekvenciák más régióiban vagy más, más májtranszportereket vagy az epeképződésben részt vevő fehérjéket kódoló génekben, például az ABCC2, ABCC3, ABCC4, illetve a tight junction protein 2 (TJP2) génekben azonosíthat variánsokat (21).
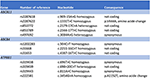
4. ábra. Az ABCB11, ABCB4 és ATP8B1 gének molekuláris genetikai elemzése.
Végeredményben egy olyan súlyos HDS indukálta kolesztatikus májkárosodás esetét írjuk le, amely összeegyeztethető az Artemisia annua tea fogyasztásával. Törekedni kell az artemisinin-származékok malária megelőzésre történő használatának visszaszorítására, amely a WHO ajánlásai szerint hatástalan, és ráadásul károsodást is okozhat. Ezen túlmenően az eset rámutat a HDS által kiváltott májkárosodás patofiziológiájának és fogékonyságának még nem megfelelő megértésére.
Adatok hozzáférhetőségi nyilatkozata
A tanulmány összes adatkészlete megtalálható a kéziratban/kiegészítő fájlokban.
Etikai nyilatkozat
Etikai felülvizsgálat és jóváhagyás nem volt szükséges az itt bemutatott egyetlen klinikai eset beszámolójához a helyi jogszabályoknak és intézményi követelményeknek megfelelően. A beteg/résztvevő írásbeli tájékozott beleegyezését adta a részvételhez.
A szerzők hozzájárulása
FR-R írta a kézirat első tervezetét. SH, CB, AL-T, MZ és AJ írták a kézirat egyes részeit. FR-R, SH, SR, MZ, KR, JB, AJ, MH, AL-T, LT és CB hozzájárult a beteg klinikai kezeléséhez, a kézirat átdolgozásához, elolvasta és jóváhagyta a benyújtott változatot.
Érdekütközés
A szerzők kijelentik, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális érdekellentétként értelmezhetők.
1. Klayman DL. Qinghaosu (artemisinin): maláriaellenes gyógyszer Kínából. Science. (1985) 228:1049-55. doi: 10.1126/science.3887571
PubMed Abstract | CrossRef Full Text | Google Scholar
2. Egészségügyi Világszervezet. WHO irányelvek a malária kezelésére, 2. kiadás. (2010). Elérhető online a következő címen: http://www.who.int/malaria/publications/atoz/9789241547925/en/index.html (hozzáférés: 2018. november 23.).
Google Scholar
3. SafeTravel.ch. Reismedizinische Beratung. Malariavorbeugung (Chemoprophylaxe) (2016). Elérhető online a következő címen: http://www.safetravel.ch/safetravel2/servlet/ch.ofac.wv.wv204j.pages.Wv204ConseilsSanteListeCtrl?action=afficheDetail&elementCourant=1 (hozzáférés: 2018. november 23.).
Google Scholar
4. Google Scholar
. Centers for Disease Control and Prevention. Gyógyszer kiválasztása a malária megelőzésére (2018). Elérhető online a következő címen: https://www.cdc.gov/malaria/travelers/drugs.html
Google Scholar
5. Shahinas D, Lau R, Khairnar K, Hancock D, Pillai DR. Artesunate visszaélés és Plasmodium falciparum malária Afrikából hazatérő utazóknál. Emerg Infect Dis. (2010) 16:1608-10. doi: 10.3201/eid1610.100427
PubMed Abstract | CrossRef Full Text | Google Scholar
6. Gyógyszerészi szakvélemény | CrossRef Full Text | Google Scholar
. Egészségügyi Világszervezet. WHO, állásfoglalás. Az Artemisia annua L. nem gyógyszeres formáinak hatékonysága a malária ellen. Genf: World Health Organization (2012).
Google Scholar
7. Navarro VJ, Khan I, Björnsson E, Seeff LB, Serrano J, Hoofnagle JH. Gyógynövény- és étrend-kiegészítők okozta májkárosodás. Hepatology. (2017) 65:363-73. doi: 10.1002/hep.28813
PubMed Abstract | CrossRef Full Text | Google Scholar
8. Hepatológiai tanulmányok. Guevart E, Aguemon A. Két fulmináns hepatitis esete artesunát-amodiaquin kombinációval végzett gyógyító kezelés alatt. Med Mal Infect. (2009) 39:57-60. doi: 10.1016/j.medmal.2008.09.024
PubMed Abstract | CrossRef Full Text | Google Scholar
9. Hosszú távú orvosi vizsgálat a fertőzésekkel kapcsolatban. Centers for Disease Control and Prevention (CDC). Artemizinint tartalmazó gyógynövény-kiegészítővel időlegesen összefüggésbe hozott hepatitis – Washington, 2008. Morb Mortal Wkly Rep. (2009) 58:854-6.
Google Scholar
10. Kumar S. Kolesztatikus májkárosodás másodlagos artemisinin hatására. Hepatology. (2015) 62:973-4. doi: 10.1002/hep.27900
PubMed Abstract | CrossRef Full Text | Google Scholar
11. Stebbings S, Beattie E, McNamara D, Hunt S. Egy randomizált, placebo-kontrollált klinikai kísérleti vizsgálat az Artemisia annua 12 héten át alkalmazott kivonatának hatékonyságának és biztonságosságának vizsgálatára a csípő- és térdízületi artritiszhez társuló fájdalom, merevség és funkcionális korlátozás kezelésére. Clin Rheumatol. (2016) 35:1829-36. doi: 10.1007/s10067-015-3110-z
PubMed Abstract | CrossRef Full Text | Google Scholar
12. Gyógyszerészi vizsgálat. Medsafe. Arthrem – A májkárosodás lehetséges kockázata -nyilatkozat az 1981. évi gyógyszertörvény 98. szakasza alapján (2018). Elérhető online a következő címen: http://www.medsafe.govt.nz/safety/EWS/2018/Arthrem.asp
Google Scholar
13. A gyógyszeres kezeléssel kapcsolatos információk. National Institutes of Health, LiverTox, Klinikai és kutatási információk a gyógyszerek okozta májkárosodásról. Artemisinin származékok. (2019). Elérhető online a következő címen: https://livertox.nih.gov/ArtemisininDerivatives.htm
Google Scholar
14. Savage RL, Tatley MV, Barnes J. Hepatotoxicitás egy természetes étrend-kiegészítővel, az Artemisia annua L. szőlőmagolajban lévő kivonattal. Új-Zélandi Gyógyszerfelügyeleti Központ jelentései. Drug Safety (2018). In: 18. ISoP éves találkozó “Farmakovigilancia határok nélkül”. Genf (elérés: 2018. november 11-14.).
Google Scholar
15. Wang JB, Zhu Y, Bai ZF, Wang FS, Li XH, Xiao XH, et al. Guidelines for the Diagnosis and Management of Herb-Induced Liver Injury. Chin J Integr Med. (2018) 24:696-706. doi: 10.1007/s11655-018-3000-8
PubMed Abstract | CrossRef Full Text | Google Scholar
16. Clarke TC, Black LI, Stussman BJ, Barnes PM, Nahin RL. A kiegészítő egészségügyi megközelítések használatának tendenciái a felnőttek körében: Egyesült Államok, 2002-2012. Natl Health Stat Rep. (2015) 79:1-16.
Google Scholar
17. Natl Health Stat Rep (2015) 79:1-16. Danan G, Teschke R. RUCAM a gyógyszerek és gyógynövények okozta májkárosodásban: a frissítés. Int J Mol Sci. (2015) 17:E14. doi: 10.3390/ijms17010014
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Int. Zhang X, Zhao Y, Guo L, Qiu Z, Huang L, Qu X. Kína különböző földrajzi régióiból származó Artemisia annua L kémiai összetevőinek különbségei. PLoS ONE. (2017) 12:e0183047. doi: 10.1371/journal.pone.0183047
PubMed Abstract | CrossRef Full Text | Google Scholar
19. The Artemisia Artemisia. Ogwang Engeu P, Omujal F, Agwaya M, Kyakulaga H, Obua C. Variációk az Artemisia annua Linn maláriaellenes összetevőiben Uganda három régiójából. Afr Health Sci. (2015) 15:828-34. doi: 10.4314/ahs.v15i3.17
CrossRef Full Text | Google Scholar
20. Afrika Egészségügyi Tudományok. Liu H, Zhan S, Zhang Y, Ma Y, Chen L, Chen L, et al. Az Artemisiae argyi foliumból származó illóolajok által kiváltott májkárosodás mechanizmusának molekuláris hálózat alapú elemzése. BMC Complement Altern Med. (2017) 17:491. doi: 10.1186/s12906-017-1997-4
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Google Scholar
. Morgan RE, Trauner M, van Staden CJ, Lee PH, Ramachandran B, Eschenberg M, et al. Az epesó-export pumpa működésének zavarása a humán májkárosodás egyik érzékenységi tényezője a gyógyszerfejlesztésben. Toxicol Sci. (2010) 118:485-500. doi: 10.1093/toxsci/kfq269
PubMed Abstract | CrossRef Full Text | Google Scholar
22. toxicol Sci. Kubitz R, Dröge C, Stindt J, Weissenberger K, Häussinger D. The bile sal export pump (BSEP) in health and disease. Clin Res Hepatol Hepatol Gastroenterol. (2012) 36:536-53. doi: 10.1016/j.clinre.2012.06.006
PubMed Abstract | CrossRef Full Text | Google Scholar
23. Az epebántalmak és az epehólyagok kezelését és kezelését célzó kutatások, valamint az epehólyagok és az epehólyagok kezelését és kezelését célzó kutatások. Alissa FT, Jaffe R, Shneider BL. A progresszív familiáris intrahepatikus cholestasis aktualizálása. J Pediatr Gastroenterol Nutr. (2008) 46:241-52.21. doi: 10.1097/MPG.0b013e318151596060
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Dixon PH, Williamson C. A terhesség intrahepatikus cholestasisának molekuláris genetikája. Obstet Med. (2008) 1:65-71. doi: 10.1258/om.2008.080010
PubMed Abstract | CrossRef Full Text | Google Scholar
25. Stieger B. A nátrium-taurokolát kotranszportáló polipeptid (NTCP) és az epesó-export pumpa (BSEP) szerepe az epeképződés fiziológiájában és patofiziológiájában. Handb Exp Pharmacol. (2011) 201:205-59. doi: 10.1007/978-3-642-14541-4_5
CrossRef Full Text | Google Scholar
26. Google Scholar
. Pauli-Magnus C, Kerb R, Fattinger K, Lang T, Anwald B, Kullak-Ublick GA, et al. BSEP és MDR3 haplotípus struktúra egészséges kaukázusiaknál, primer epeúti cirrózisban és primer szklerotizáló cholangitisben. Hepatology. (2004) 39:779-91. doi: 10.1002/hep.20159
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Hepatológiai és hepatológiai vizsgálatok. Pan S, Li X, Jiang P, Jiang Y, Shuai L, He Y, et al. Az ABCB4 és ABCB11 gének variációi összefüggnek a primer intrahepatikus kövekkel. Mol Med Rep. (2015) 11:434-46. doi: 10.3892/mmr.2014.2645
PubMed Abstract | CrossRef Full Text | Google Scholar
28. A Mol Med Rep. Dröge C, Bonus M, Baumann U, Klindt C, Lainka E, Kathemann S, et al. A FIC1, BSEP és MDR3 szekvenálása nagyszámú kolestázisos betegcsoportban nagyszámú különböző genetikai változatot mutatott ki. J Hepatol. (2017) 67:1253-64. doi: 10.1016/j.jhep.2017.07.004
PubMed Abstract | CrossRef Full Text | Google Scholar